Clear Sky Science · es
Hidrogenación altamente selectiva y práctica de (hetero)arenos funcionalizados
De moléculas planas a bloques constructores 3D
Los medicamentos modernos, los plásticos y muchos productos químicos cotidianos se construyen a partir de pequeños “ladrillos” moleculares. La mayoría de estos ladrillos son estructuras planas en forma de anillo llamadas arenos, que atraen a los químicos porque son fáciles de sintetizar y modificar. Pero los buscadores de fármacos y los científicos de materiales reclaman cada vez más formas tridimensionales, que con frecuencia presentan mejor comportamiento en el organismo y proporcionan a los plásticos un rendimiento mejorado. Este artículo describe una forma nueva y práctica de convertir anillos planos en estructuras 3D precisas utilizando un catalizador de platino robusto, abriendo una vía más simple hacia fármacos de próxima generación y aditivos plásticos más seguros.
Por qué la forma importa en las moléculas
Los anillos aromáticos planos están en todas partes: en productos farmacéuticos, agroquímicos, vitaminas y polímeros. Su popularidad los hace baratos y de amplia disponibilidad. En cambio, sus homólogos “saturados”, es decir, anillos a los que se han eliminado las dobles ligaduras, son mucho menos comunes comercialmente, aunque ofrecen ventajas importantes. Cuando un anillo se satura y adquiere forma tridimensional, los químicos obtienen un control mucho más fino sobre propiedades como el encaje de un fármaco en el bolsillo de una proteína o la flexibilidad de un plástico. Por ejemplo, ajustando la proporción entre dos disposiciones 3D especulares (llamadas formas cis y trans), los fabricantes de polímeros pueden modular la temperatura de transición vítrea, que determina si un material es rígido o flexible a una temperatura dada.
El reto de curvar anillos planos
Convertir un anillo aromático plano en un anillo saturado 3D parece sencillo: solo hay que añadir hidrógeno. En la práctica, es muy difícil. Los anillos aromáticos son inusualmente estables, por lo que romper su “aromaticidad” requiere mucha energía. Al mismo tiempo, las moléculas del mundo real suelen llevar grupos químicos adicionales, como ésteres o amidas, que deben permanecer intactos durante el proceso. Un catalizador debe por tanto hacer tres cosas a la vez: activar anillos resistentes en condiciones suaves, ignorar otras partes sensibles de la molécula y colocar los nuevos átomos de hidrógeno de modo que una forma 3D sea fuertemente preferida sobre la otra. Los catalizadores existentes que logran esto suelen ser complejos, sensibles y difíciles de reciclar, lo que los hace poco atractivos para uso industrial a gran escala.
Un catalizador de platino robusto sobre un soporte conocido
Los investigadores informan de un catalizador heterogéneo sencillo: partículas diminutas de platino depositadas sobre dióxido de titanio (Pt/TiO2). Con este material pueden hidrogenar una amplia variedad de arenos y heteroarenos polisustituidos—anillos que además contienen átomos como nitrógeno u oxígeno—bajo condiciones relativamente suaves de temperatura y presión de hidrógeno. Sorprendentemente, las reacciones favorecen con fuerza una disposición 3D, alcanzando a menudo una relación de diastereómeros de hasta 99 a 1 a favor de la forma cis. A diferencia de muchos sistemas anteriores, el catalizador es sólido, fácil de filtrar y reutilizable. Además, deja intactos grupos delicados como ésteres, ésteres borónicos y amidas, lo cual es crucial cuando el anillo forma parte de un fármaco complejo o de un material funcional.
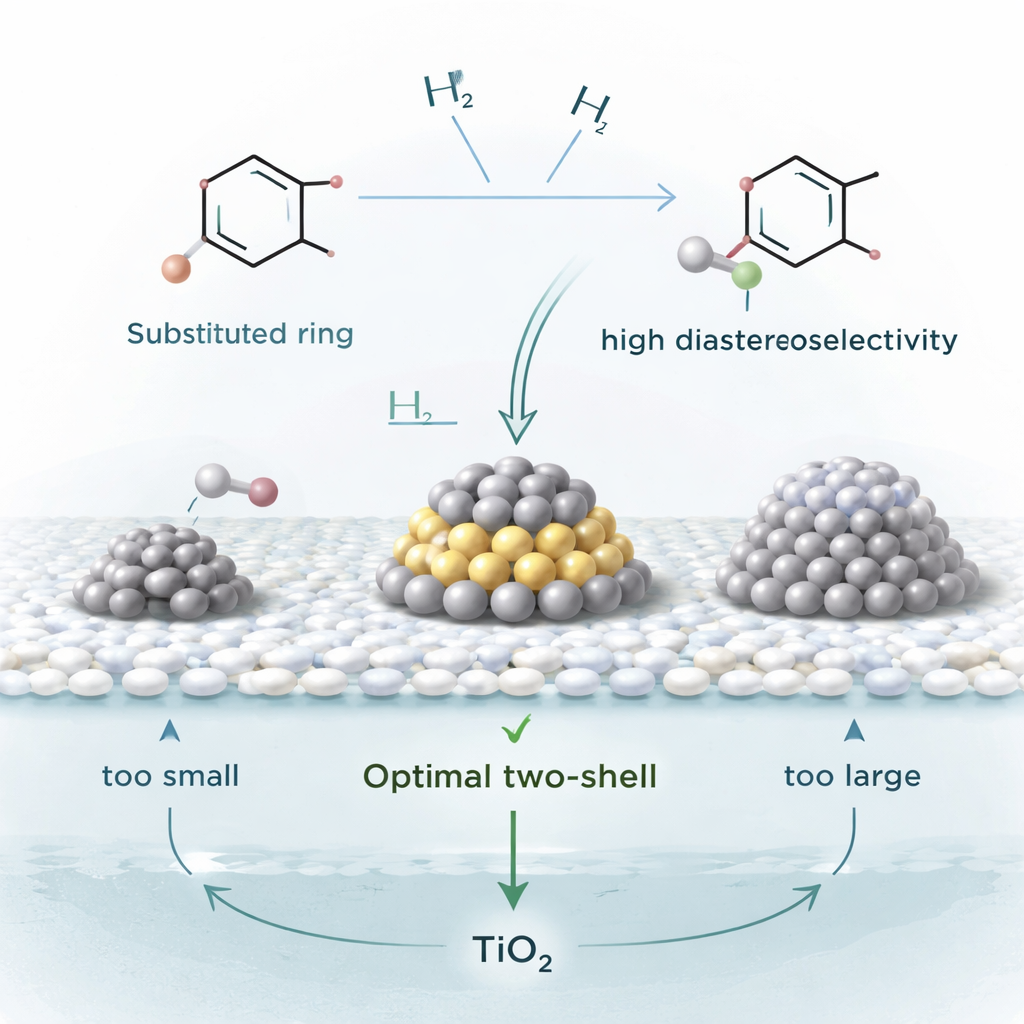
Descubriendo el punto óptimo
Para entender por qué este catalizador funciona tan bien, el equipo estudió una reacción de referencia: convertir ftalato de dimetilo, un químico industrial común, en su equivalente saturado. Preparando Pt/TiO2 con diferentes cargas de platino y midiendo las velocidades de reacción, descubrieron que la mayor actividad se da cuando las partículas de platino tienen un tamaño intermedio muy específico. Imágenes por microscopía electrónica y simulaciones por ordenador mostraron que las partículas con una estructura de “dos capas” —lo bastante grandes para alojar simultáneamente el anillo plano y el hidrógeno, pero no tan grandes que el anillo se una demasiado débilmente— son el verdadero punto óptimo. Los cúmulos más pequeños se taponan por el fuerte agarre del anillo, mientras que las partículas mucho mayores no sujetan el anillo con suficiente firmeza para reproducir el comportamiento observado.
De reacciones modelo a productos del mundo real
Con este conocimiento, los científicos exploraron la amplitud de aplicación del catalizador. Transformaron con éxito muchos derivados del benceno sustituidos y sistemas de anillos fundidos o tensos, usualmente con altos rendimientos y marcada preferencia por los productos cis. De gran importancia para la química medicinal, también aplicaron el método a heteroarenos que contienen nitrógeno y que sirven como bloques constructores para fármacos importantes, incluidos intermedios relacionados con el antibiótico moxifloxacino. Para demostrar la relevancia industrial, llevaron a cabo una reacción a escala de kilogramo que convierte un plastificante de ftalato comercial en una alternativa libre de ftalato en condiciones sin disolventes, obteniendo casi exclusivamente la forma cis deseada y mostrando que el catalizador puede reciclarse varias veces.
Qué significa esto para la química cotidiana
En términos sencillos, este trabajo proporciona a los químicos una herramienta resistente y reutilizable para transformar anillos planos comunes en formas más tridimensionales y finamente definidas, sin desvíos sintéticos largos. Al identificar con precisión qué estructuras de platino hacen el trabajo pesado, el estudio abre la puerta al diseño racional de catalizadores aún mejores. El impacto inmediato podría ser rutas más rápidas hacia nuevos candidatos farmacológicos, plastificantes más seguros y ajustables, y un uso más eficiente del hidrógeno en la fabricación química—todo ello logrado con un catalizador sólido relativamente simple que encaja bien en los procesos industriales existentes.
Cita: Qu, R., Jena, S., Xiao, L. et al. Highly selective and practical hydrogenation of functionalized (hetero)arenes. Nat Commun 17, 2015 (2026). https://doi.org/10.1038/s41467-026-68537-7
Palabras clave: hidrogenación de arenos, catalizador de platino, andamios moleculares 3D, heteroarenos, síntesis de plastificantes