Clear Sky Science · es
La palmitoilación de B7H3 inducida por ácido palmítico promueve la evasión inmunitaria
Por qué esta investigación importa para los pacientes con cáncer
La mayoría sabe que los nuevos fármacos de inmunoterapia pueden ayudar al sistema inmunitario a atacar el cáncer, pero muchos pacientes con cáncer colorrectal común obtienen poco beneficio. Este estudio descubre un truco bioquímico oculto que los tumores colorrectales utilizan para protegerse del ataque inmunitario y señala un nuevo tipo de fármaco—un péptido corto—que podría mejorar la eficacia de la inmunoterapia en esos pacientes.
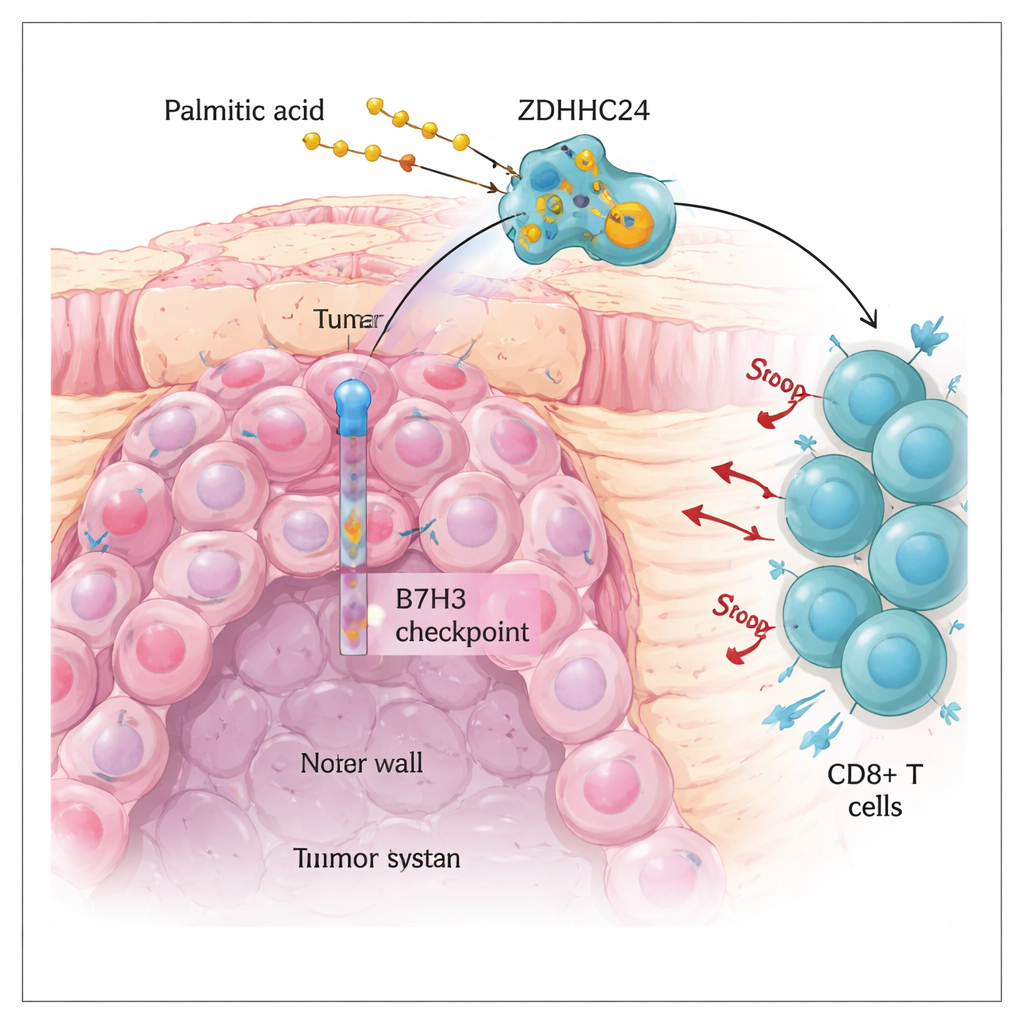
Un obstáculo en la inmunoterapia actual del cáncer de intestino
El cáncer colorrectal es uno de los cánceres más frecuentes en todo el mundo. Los fármacos de inmunoterapia que liberan los “frenos” inmunitarios, como los inhibidores de PD‑1 y PD‑L1, han transformado el tratamiento de una minoría de pacientes cuyos tumores acumulan muchos errores en el ADN (los llamados tumores MSI‑H). Desafortunadamente, la mayoría de los cánceres colorrectales son microsatélite‑estables (MSS) y responden mal a estos tratamientos. Los autores se centraron en otra molécula de freno llamada B7H3, que se ubica en la superficie de las células tumorales y reduce la actividad de las células inmunitarias asesinas, especialmente las T CD8+. Encontraron que la proteína B7H3 está fuertemente elevada en los tumores MSS y se asocia con peor supervivencia, aunque el gen subyacente de B7H3 no está más activo. Esa discrepancia planteó una pregunta importante: ¿qué mantiene la proteína B7H3 tan abundante en las células tumorales?
Cómo una grasa común ayuda a los tumores a esconderse
El equipo sospechó que el metabolismo tumoral podría estar estabilizando B7H3. Al comparar la actividad génica y los perfiles de pequeñas moléculas de tumores colorrectales MSS y MSI‑H, descubrieron que muchas vías relacionadas con los lípidos difieren, destacando un ácido graso concreto: el ácido palmítico. Cuando expusieron células de cáncer de colon a varios productos de degradación de grasas en el laboratorio, solo el ácido palmítico provocó un claro aumento de los niveles de la proteína B7H3. Experimentos adicionales mostraron por qué: el ácido palmítico alimenta un proceso químico llamado palmitoilación, en el que una cadena grasa se une a puntos específicos de las proteínas. Esta modificación, realizada por una enzima denominada ZDHHC24 en una única cisteína dentro de B7H3, hizo que B7H3 fuera más estable y más abundante en la superficie de la célula tumoral.
Bloquear la ruta de eliminación de un freno inmunitario
Las células normalmente eliminan proteínas no deseadas o dañadas mediante sistemas que funcionan como reciclaje y disposición de residuos. Los investigadores demostraron que B7H3 se degrada principalmente por una vía de “autodigestión” celular llamada autofagia, que utiliza una proteína receptor llamada SQSTM1/p62 para etiquetar la carga para su destrucción. Cuando B7H3 estaba palmitoilada, se unía débilmente a este receptor y escapaba de la degradación por autofagia, lo que llevaba a niveles persistentes y elevados del freno inmunitario. Cuando el sitio de palmitoilación se mutó para que ya no pudiera llevar la etiqueta grasa, o cuando se eliminó la enzima ZDHHC24, B7H3 fue dirigida con más eficacia a las “bolsas de basura” celulares y degradada. En ratones, los tumores que carecían de B7H3 palmitoilada crecieron más despacio, no cambiaron su tasa de crecimiento intrínseca en animales inmunodeficientes y mostraron notablemente más células T CD8+ y una actividad citotóxica tumoral más fuerte. Esto demostró que la modificación actúa principalmente desactivando la inmunidad, no alterando la velocidad de división de las células cancerosas.
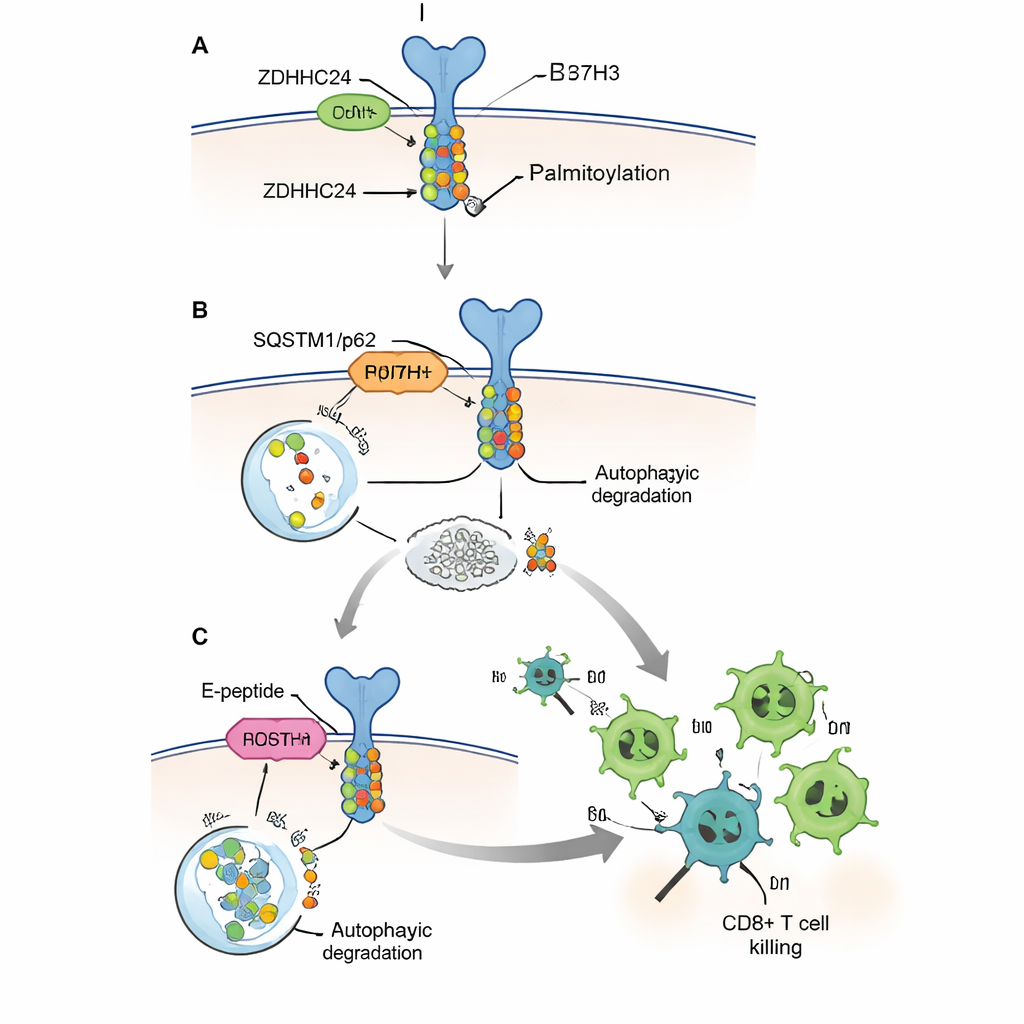
Reducir el escudo y potenciar las T
Como eliminar por completo ZDHHC24 o B7H3 mediante genética no es un tratamiento práctico en pacientes, los autores diseñaron un péptido corto que penetra en las células al que llaman péptido E. Imita un pequeño tramo de la proteína B7H3 que normalmente se une a ZDHHC24, actuando como señuelo que evita que la enzima modifique las moléculas reales de B7H3. En células en cultivo, el péptido E redujo la palmitoilación y los niveles de B7H3, restauró su reconocimiento por la maquinaria de autofagia y permitió que las células T CD8+ humanas mataran las células tumorales con mayor eficiencia. En varios modelos de ratón, incluido un ratón humanizado con células inmunitarias humanas y tumores colorrectales humanos, las inyecciones del péptido E redujeron los tumores, aumentaron el número de células T CD8+ en su interior y elevaron la producción de moléculas clave asesinas como la granzima B y el interferón gamma.
Un nuevo compañero para la inmunoterapia existente
Finalmente, los investigadores preguntaron si esta estrategia podría funcionar junto con el bloqueo estándar de PD‑1. En modelos de ratón de cáncer colorrectal, tanto el péptido E solo como el anticuerpo anti‑PD‑1 solo ofrecieron cierto control tumoral. Pero cuando se combinaron, los dos tratamientos produjeron una supresión tumoral mucho más fuerte y duradera, en algunos casos haciendo desaparecer los tumores y duplicando con creces la supervivencia media en comparación con los controles. Esto sugiere que desactivar el escudo B7H3 al cortar su “ancla” grasa puede complementar los fármacos de punto de control existentes que actúan sobre la vía PD‑1.
Qué significa esto para el tratamiento futuro del cáncer
En términos sencillos, este estudio muestra que una grasa dietaria común, el ácido palmítico, puede ser aprovechada por los tumores colorrectales para blindar químicamente una proteína que bloquea la inmunidad (B7H3) y ayudar al cáncer a ocultarse. Al bloquear esa única unión química, los autores pudieron despojar esa armadura, permitir que los sistemas de eliminación de la propia célula degradaran B7H3 y reabrir el acceso de las células T CD8+ para atacar. Aunque el péptido E es por ahora una herramienta experimental en fase temprana, el trabajo identifica la palmitoilación de B7H3—y su enzima ZDHHC24—como dianas farmacológicas prometedoras. Si agentes similares resultan seguros y eficaces en humanos, podrían algún día convertir más cánceres colorrectales de tumores “fríos” que ignoran la inmunoterapia en tumores “calientes” que el sistema inmunitario puede reconocer y destruir.
Cita: Rao, Z., Huang, C., Wu, Q. et al. Palmitic acid-triggered B7H3 palmitoylation promotes immune escape. Nat Commun 17, 1810 (2026). https://doi.org/10.1038/s41467-026-68525-x
Palabras clave: inmunoterapia del cáncer colorrectal, punto de control B7H3, metabolismo del ácido palmítico, palmitoilación de proteínas, inmunidad tumoral de células T CD8