Clear Sky Science · es
Los macrófagos de pez cebra convierten las señales físicas de la herida en una rápida permeabilización vascular
Cómo un pez diminuto nos enseña sobre la hinchazón de las heridas
Cuando te raspas la rodilla, la zona se enrojece, se hincha y se vuelve permeable al líquido con rapidez. Este cambio rápido en los vasos sanguíneos cercanos es crucial para combatir infecciones e iniciar la reparación, pero ver en tiempo real cómo el cuerpo detecta el daño y responde en cuestión de segundos ha sido difícil. Al usar larvas de pez cebra translúcidas y técnicas avanzadas de imagen en vivo, este estudio revela cómo células inmunitarias especializadas, envueltas alrededor de los vasos, convierten el choque físico de una herida en una fuga casi instantánea de los vasos, ofreciendo nuevas perspectivas sobre la inflamación, la curación e incluso el daño pulmonar humano.
Observando cómo la lesión se propaga por el cuerpo
Los investigadores trabajaron con peces cebra jóvenes, cuyos cuerpos transparentes permiten a los científicos observar células y vasos sanguíneos en acción bajo el microscopio. Cortaron la punta de la aleta caudal y llenaron la circulación con un tinte luminoso que permanece dentro de los vasos sanos. Cuando los peces heridos se devolvieron al agua dulce normal, la entrada súbita de agua en los tejidos creó un "choque osmótico" alrededor de la herida. En cuestión de minutos, los vasos cercanos se dilataron y comenzaron a filtrar el tinte fluorescente hacia el tejido circundante, imitando la hinchazón y el supurado que ocurren alrededor de las heridas humanas. Al mover los peces entre soluciones salinas o azucaradas especialmente balanceadas y agua normal, el equipo demostró que esta rápida permeabilización vascular depende en gran medida de cambios osmóticos más que del simple desgarro tisular.
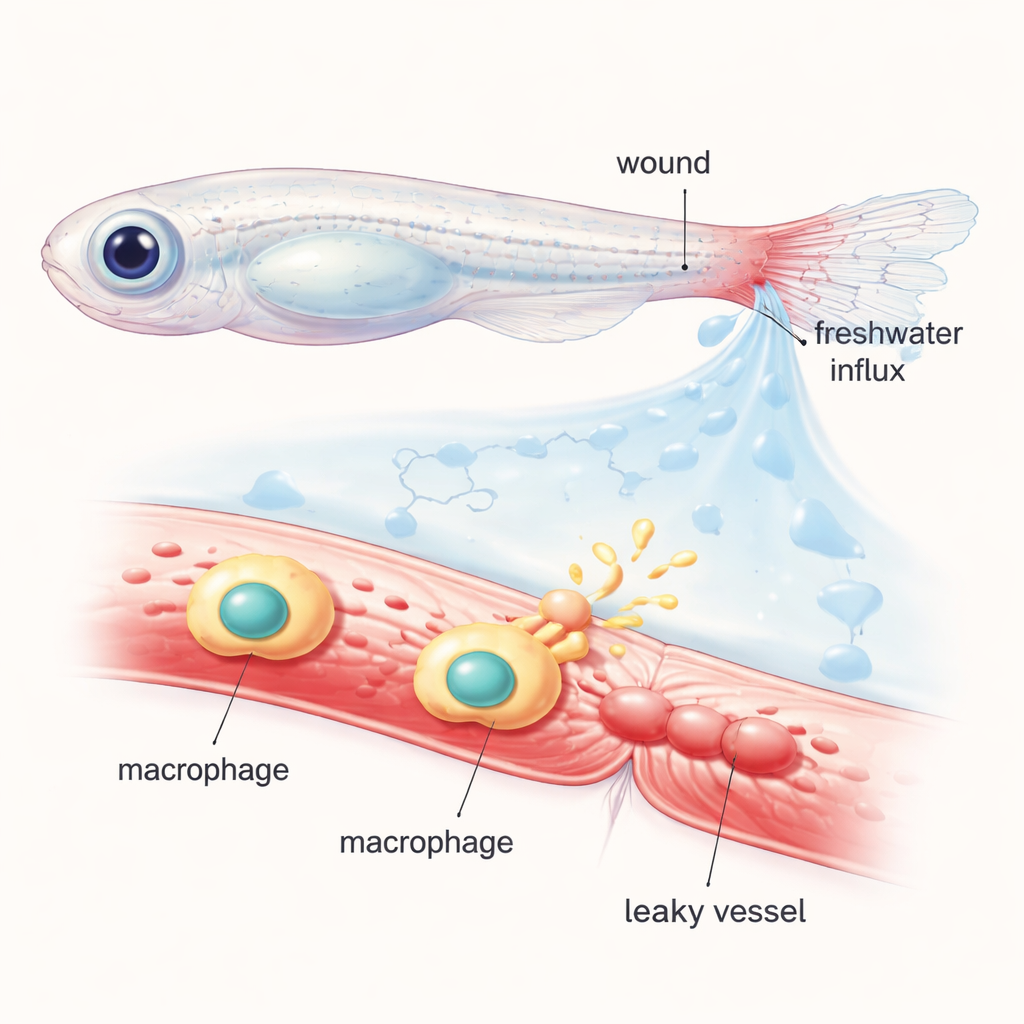
Rastreando los mensajeros químicos detrás de la fuga
Para averiguar qué moléculas convierten el choque físico en una señal de fuga, los científicos examinaron una familia de compuestos grasos llamados eicosanoides, derivados del ácido araquidónico. Estos lípidos son bien conocidos por sus papeles en la inflamación y el flujo sanguíneo. Usando mutantes genéticos y fármacos, desactivaron selectivamente enzimas individuales en la vía de los eicosanoides. Bloquear una enzima clave llamada Alox5a (5-lipoxigenasa) o su socia Lta4h redujo drásticamente la cantidad de tinte que escapaba de los vasos tras el choque osmótico, sin detener el cierre de la herida en sí. En contraste, interferir con otras enzimas relacionadas tuvo poco efecto. Esto apuntó a una rama específica de la vía lipídica como el principal impulsor de la respuesta de fuga rápida, actuando casi como una válvula química que puede abrirse o cerrarse a demanda.
El sorprendente papel de las células inmunitarias que abrazan los vasos
La sangre contiene distintos tipos de células inmunitarias y, en las larvas de pez cebra, los neutrófilos y los macrófagos son los protagonistas principales. El equipo usó un truco genético ingenioso para destruir selectivamente neutrófilos o macrófagos antes de causar la herida. Eliminar neutrófilos apenas modificó la fuga vascular. Pero cuando se eliminaron los macrófagos, la respuesta de fuga disminuyó en aproximadamente la mitad, reflejando el efecto de bloquear la vía lipídica Alox5a–Lta4h. Es importante que estas manipulaciones no impidieron que la herida se cerrara rápidamente, lo que muestra que el reclutamiento de leucocitos y la fuga vascular pueden controlarse de manera algo independiente. Esto puso de manifiesto a los macrófagos perivasculares —macrófagos situados a lo largo del exterior de los vasos— como traductores clave entre la lesión física y el comportamiento vascular.
Del estiramiento nuclear a la señal química
¿Cómo detectan estos macrófagos perivasculares una herida que puede estar a cierta distancia? La respuesta reside en la manera en que sus núcleos responden al estrés mecánico. Cuando el choque osmótico de la herida se propaga por el tejido cercano, la entrada de agua provoca un sutil hinchamiento celular y deformación nuclear. Los investigadores etiquetaron una enzima mecanosensible llamada cPla2 con un marcador fluorescente y la expresaron específicamente en macrófagos. Tras la herida en agua dulce normal, cPla2 se desplazó rápidamente hacia la superficie interna de la membrana nuclear en macrófagos en una onda que barrió el tejido a unos 50 micrómetros por segundo, coincidiendo con la propagación de las sales disueltas. Esta translocación dependía de condiciones hipotónicas y fue mucho más débil en soluciones isotónicas. Los macrófagos cercanos a los vasos mostraron pulsos especialmente nítidos y reversibles de unión nuclear de cPla2, lo que a su vez libera ácido araquidónico para su conversión en los lípidos que inducen la fuga.
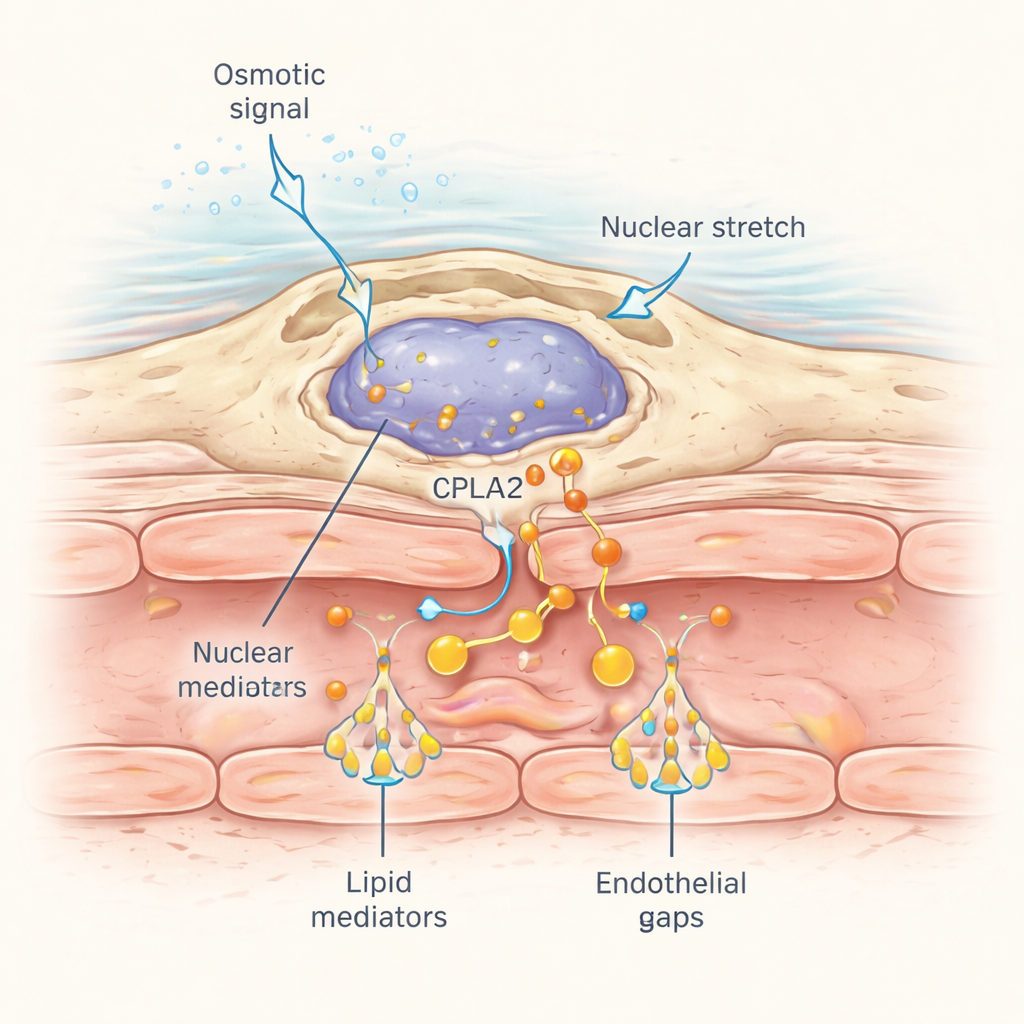
Por qué esto importa más allá de los peces
En pocas palabras, este estudio muestra que ciertos macrófagos actúan como centinelas físicos: sienten el estiramiento de los tejidos y de las membranas nucleares causado por cambios osmóticos en una herida, activan cPla2 en la superficie nuclear y producen rápidamente mensajeros lipídicos que indican a los vasos sanguíneos cercanos que "abran las compuertas" y permitan la entrada de líquidos y factores inmunitarios. Aunque el pez cebra vive en agua dulce y afronta desafíos osmóticos únicos, vías mecanosensibles similares probablemente operan en tejidos humanos expuestos a cambios de presión y flujo, como los pulmones durante la ventilación mecánica. Entender cómo el estiramiento nuclear y las señales lipídicas controlan la permeabilidad vascular en tiempo real podría, en última instancia, orientar tratamientos que modulen la inflamación—ya sea para reducir fugas dañinas en condiciones como la lesión pulmonar aguda o para potenciar respuestas útiles que aceleren la reparación tisular.
Cita: Gelashvili, Z., Shen, Z., Ma, Y. et al. Zebrafish macrophages convert physical wound signals into rapid vascular permeabilization. Nat Commun 17, 1807 (2026). https://doi.org/10.1038/s41467-026-68520-2
Palabras clave: curación de heridas, vasos sanguíneos, macrófagos, inflamación, pez cebra