Clear Sky Science · es
Celdas líquidas ultrafinas para criomicroscopía electrónica con resolución temporal de microsegundos
Observar las proteínas en acción en tiempo real
Muchas de las máquinas que mantienen vivas a nuestras células están hechas de proteínas, y con frecuencia sabemos cómo se ven esas proteínas cuando están congeladas en un lugar. Pero lo que realmente queremos ver es cómo se mueven mientras hacen su trabajo. Este estudio presenta una nueva forma de observar esos movimientos en escalas de tiempo increíblemente cortas —microsegundos— sin sacrificar el detalle nítido que la criomicroscopía electrónica (crio-EM) moderna puede ofrecer.
Una nueva ventana al mundo microscópico
La crio-EM ha revolucionado la biología estructural al captar proteínas congeladas por congelación instantánea con resolución casi atómica. Sin embargo, los métodos tradicionales muestran solo imágenes fijas. Para capturar movimiento, los investigadores desarrollaron la “crio-EM con resolución temporal de microsegundos”, en la que un láser funde brevemente una muestra congelada para que las proteínas puedan moverse y luego la muestra se vuelve a congelar rápidamente para inmovilizarlas en nuevas posiciones. El problema ha sido que la delgada película líquida creada por el láser tiende a romperse después de unas pocas decenas de microsegundos, limitando el tiempo durante el cual se pueden observar las proteínas. El trabajo nuevo resuelve este cuello de botella encerrando la muestra en una celda líquida ultrafina, manteniéndola estable el tiempo suficiente para observar movimientos más lentos y complejos.
Construyendo una celda líquida ultrafina
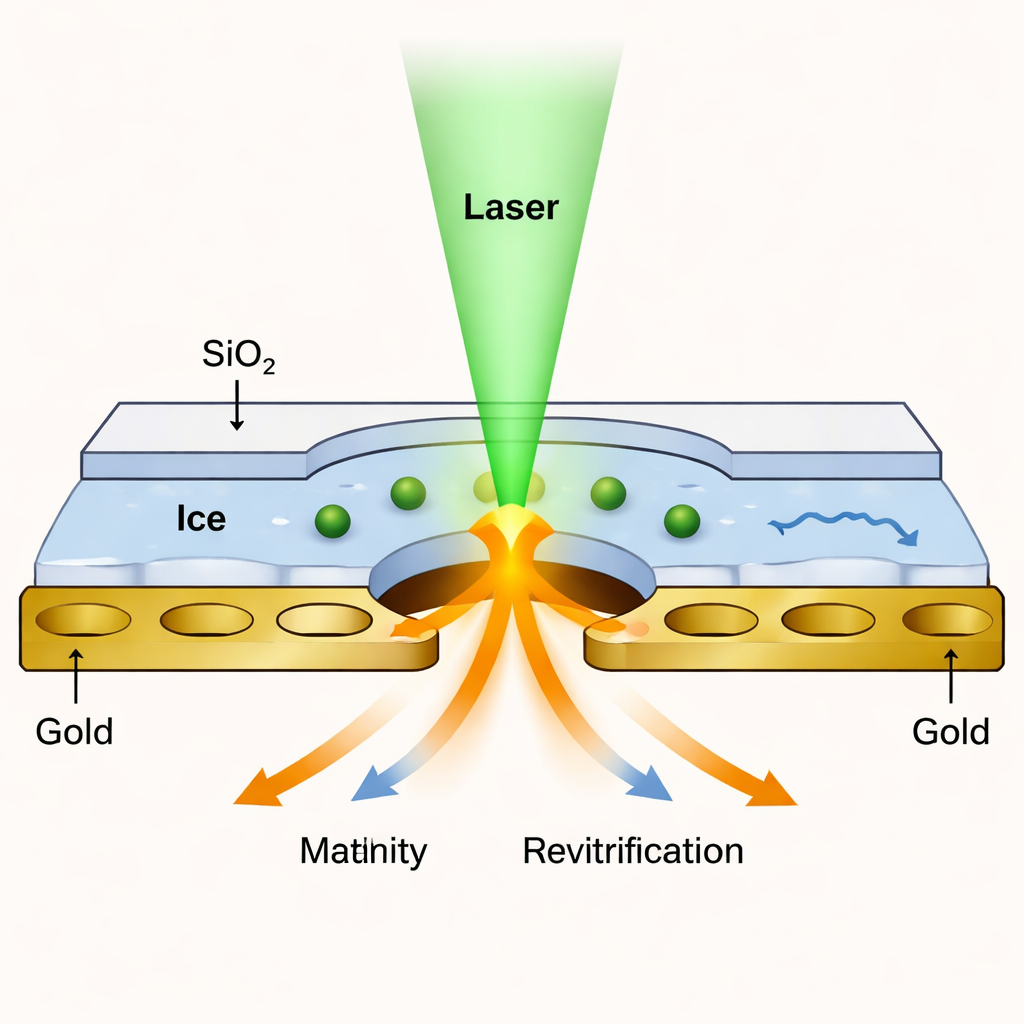
El equipo creó una especie de sándwich nanoscópico: la solución proteica se congela sobre una rejilla de oro perforada estándar, y luego ambos lados se recubren con capas de dióxido de silicio de solo unos 1,4 nanómetros de espesor —apenas unos pocos átomos. Estas capas vítreas actúan como tapas transparentes que evitan que el líquido se evapore cuando el láser funde el hielo. Pulsos láser cortos calientan la muestra sellada a una temperatura controlada y luego permiten que se vuelva a congelar en microsegundos. Como las membranas son tan delgadas, siguen permitiendo el paso suficiente de electrones para que el microscopio produzca imágenes con casi la misma resolución que en la crio-EM convencional, hasta aproximadamente 1,7–1,8 Ångström en una proteína de prueba llamada apoferritina.
Vistas más nítidas y ángulos más equitativos
Un desafío oculto en la crio-EM es que las proteínas tienden a adherirse a la interfaz aire-agua en la delgada capa de hielo, alineándose en orientaciones similares y dificultando la reconstrucción completa en 3D. Los recubrimientos de dióxido de silicio en estas celdas líquidas transforman la superficie de agua-aire a agua-sólido y la hacen más favorable para el agua. Como resultado, las proteínas tienen menos probabilidades de quedarse pegadas en una única pose. Cuando los autores probaron una gran maquinaria celular llamada subunidad ribosómica 50S, encontraron que la distribución angular de las partículas se volvió casi perfectamente uniforme, eliminando esencialmente el problema de larga data de la “orientación preferente” mientras se mantenía una alta resolución en las reconstrucciones finales.
Cronometrando el movimiento de una palanca molecular
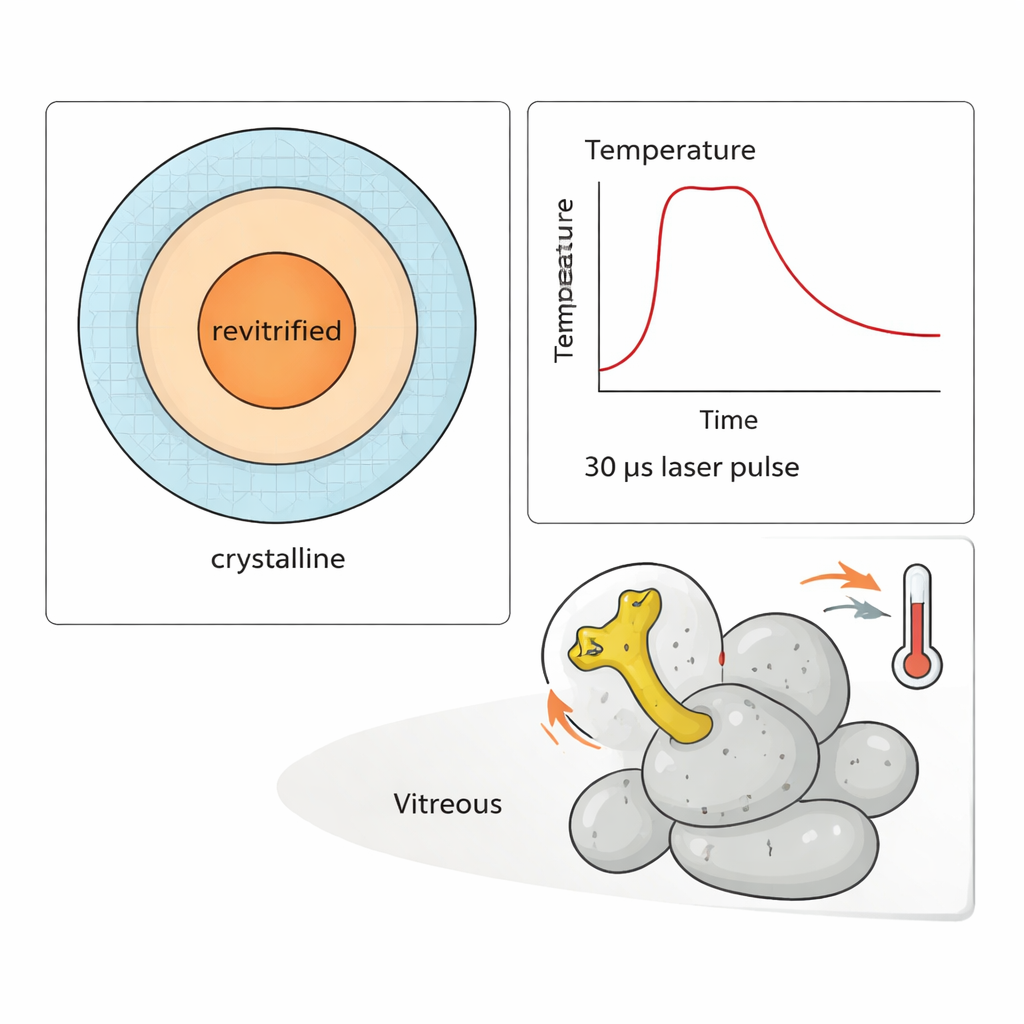
Para mostrar la potencia de su método, los investigadores llevaron a cabo un experimento de “salto térmico” en la subunidad 50S. Un brazo flexible de esta partícula, conocido como la punta L1, oscila como una palanca durante la síntesis proteica. Al administrar trenes de pulsos láser de 30 microsegundos, pudieron calentar la muestra a distintas temperaturas durante hasta unos 300 microsegundos y luego volver a congelarla. Simulaciones y mediciones de qué regiones se vuelven a congelar como vidrio les permitieron estimar la temperatura de cada partícula observada. Analizando miles de imágenes, mostraron que la amplitud del movimiento de la punta L1 aumenta claramente con la temperatura —pero solo después de que han transcurrido cientos de microsegundos. En tiempos tempranos, la distribución de conformaciones todavía refleja el estado original a temperatura ambiente antes del recongelado.
Por qué esto importa para la biología futura
Para quienes no son especialistas, el mensaje clave es que este diseño de celda líquida ultrafina amplía dramáticamente el tiempo durante el cual se pueden observar las proteínas en movimiento sin difuminar los detalles estructurales. Desplaza la crio-EM con resolución temporal de microsegundos de captar solo los eventos más rápidos a sondear reordenamientos más lentos y biológicamente importantes, como la respuesta retardada de la punta L1 a un pulso térmico. Con refinamientos adicionales, este enfoque podría cerrar la brecha hasta la escala de milisegundos y más allá, y también ofrece nuevas formas de preparar muestras, reducir artefactos de imagen y desencadenar reacciones directamente en la rejilla. En términos prácticos, esto significa que los científicos están cada vez más cerca de hacer “películas moleculares” que vinculen las formas de las proteínas con lo que realmente hacen dentro de las células vivas.
Cita: Curtis, W.A., Wenz, J., Krüger, C.R. et al. Ultrathin liquid cells for microsecond time-resolved cryo-EM. Nat Commun 17, 1799 (2026). https://doi.org/10.1038/s41467-026-68515-z
Palabras clave: crio-EM con resolución temporal, dinámica de proteínas, microscopía electrónica de celdas líquidas, palanca L1 del ribosoma, membranas ultrafinas de dióxido de silicio