Clear Sky Science · es
Las fuerzas mecánicas de la autoensamblación peptídica intercelular impulsan la formación de esféroides
Construir pequeños tejidos en el laboratorio
Los científicos compiten por crear versiones en miniatura de tejidos humanos que se comporten como los reales. Estos modelos vivientes pueden hacer que las pruebas de fármacos contra el cáncer sean más seguras y acercar nuevos tratamientos para la diabetes y otras enfermedades a la práctica clínica. Este estudio presenta una forma ingeniosa de inducir a las células a formar cúmulos tridimensionales realistas, completos con sus propias redes primitivas “tipo vasos sanguíneos” que mejoran el suministro de nutrientes y la función.
Ayudar a las células a sentir su entorno
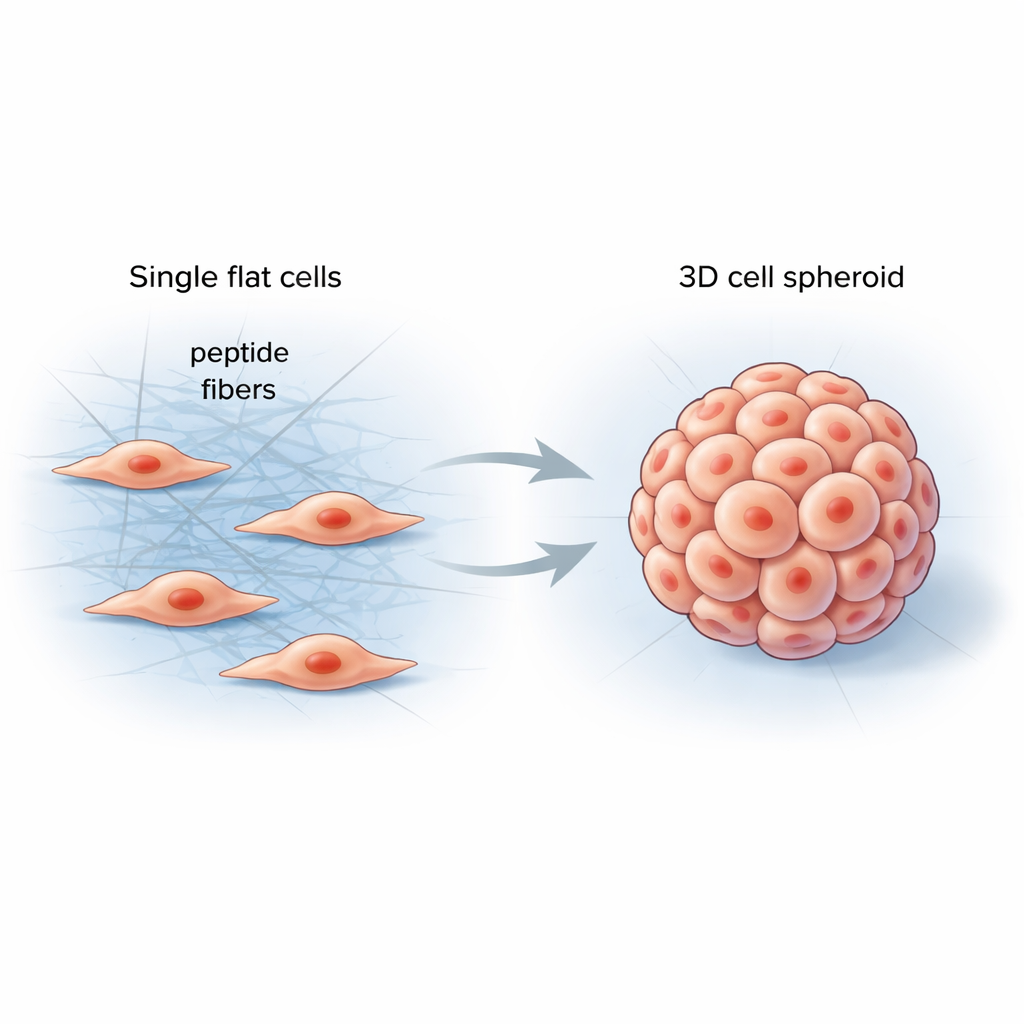
Dentro de nuestro cuerpo, las células viven en un entorno blando pero estructurado llamado matriz extracelular: una malla de proteínas que sostiene los tejidos y envía señales mecánicas constantes a las células. Los materiales convencionales de laboratorio tienen problemas para imitar esta complejidad y con frecuencia producen capas celulares planas que se comportan de forma muy diferente a los órganos o tumores reales. Los investigadores se propusieron diseñar un material sencillo y programable que se formara directamente entre las células, rigidizara su entorno de forma controlada y las empujara hacia formas tridimensionales más naturales.
Péptidos inteligentes que se ensamblan entre células
El equipo creó fragmentos cortos de proteína, llamados péptidos, que pueden unirse en fibras largas y delgadas cuando encuentran enzimas específicas en la superficie celular. Cuando estos péptidos se añadieron a células cancerosas, permanecieron inactivos al principio, como una solución clara. Una vez que las propias enzimas de las células recortaron una parte de la molécula, los péptidos se autoensamblaron rápidamente en una red fibrosa que envolvió y se extendió entre las células vecinas. Esta nueva malla de fibras cambió las fuerzas mecánicas locales, animando a las células a tironearse entre sí, remodelar su armazón interno y reunirse en esféroides esféricos 3D en lugar de expandirse en una lámina.
De cúmulos celulares a redes tipo vasos
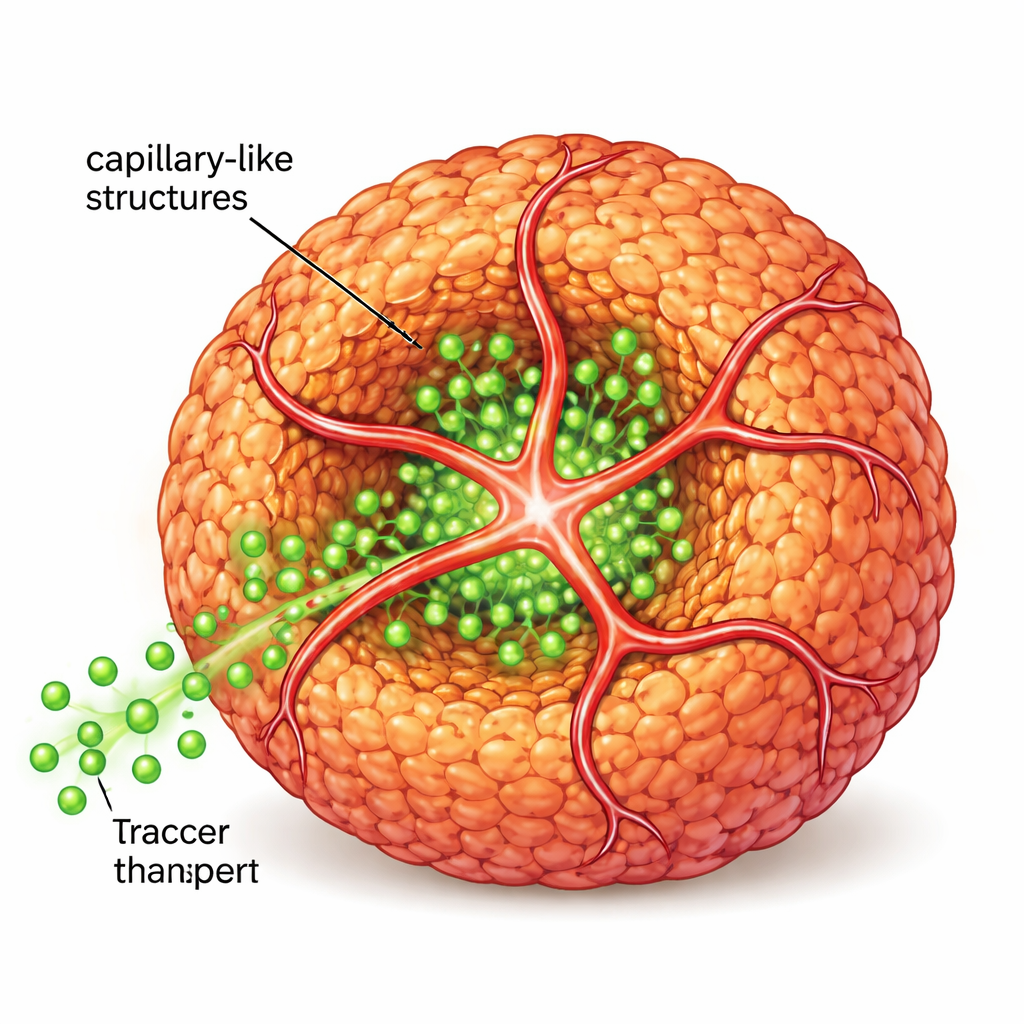
Para acercarse más al tejido real, los científicos introdujeron a continuación células endoteliales humanas —el tipo que normalmente recubre los vasos sanguíneos— junto con un segundo péptido que llevaba una pequeña “etiqueta de dirección” que atraía a estas células. Juntos, los péptidos original y modificado formaron un andamiaje de nanofibras compartido. Las células endoteliales usaron este andamiaje para brotar en extensiones tubulares que envolvieron y penetraron los esféroides, creando estructuras semejantes a capilares. Cuando el equipo hizo fluir moléculas fluorescentes similares a azúcares alrededor de estas estructuras, observaron una penetración mucho más profunda en el núcleo del esféroide en comparación con esféroides sin estos tubos internos, lo que mostró que el transporte de nutrientes y señales mejoró notablemente.
MÁS parecido a tumores reales y a islotes funcionales
El perfilado de la actividad génica reveló que los esféroides tumorales con estructuras tipo capilar se parecían más a muestras de glioblastoma de pacientes que los cultivos tradicionales en plano o los esféroides no vascularizados. En ratones, los esféroides que contenían estas redes vasculares primitivas crecieron hasta formar tumores más grandes y vascularizados, lo que indica que el modelo in vitro captura características clave del comportamiento tumoral real. La misma estrategia se aplicó a células beta pancreáticas, que normalmente viven en islotes muy vascularizados y secretan insulina en respuesta a la glucosa. Cuando los esféroides de células beta se equiparon con estructuras tipo capilar usando el sistema de péptidos y células endoteliales, mostraron una liberación de insulina mucho más fuerte y afinada, lo que sugiere una herramienta potente para la investigación de la diabetes y la medicina regenerativa.
Por qué esto importa para terapias futuras
Al permitir que péptidos sencillos se autoensamblen entre células vivas, este trabajo ofrece una receta general para construir tejidos en miniatura vascularizados que se sienten y funcionan más como los del interior del cuerpo. Los esféroides resultantes reflejan mejor los tumores de pacientes y los islotes funcionales, lo que los hace valiosos para probar fármacos, estudiar mecanismos de enfermedad y diseñar nuevas terapias basadas en células. Para el público general, la conclusión clave es que dar a las células cultivadas en laboratorio la “sensación adecuada” y pequeñas redes tipo vasos puede mejorar drásticamente el grado en que imitan los tejidos humanos, acelerando potencialmente el camino desde la investigación básica hasta tratamientos efectivos.
Cita: Lu, H., Li, Y., Yang, X. et al. Mechanical forces from intercellular peptide self-assembly drive spheroid formation. Nat Commun 17, 1801 (2026). https://doi.org/10.1038/s41467-026-68513-1
Palabras clave: ingeniería de tejidos, modelos de cáncer, angiogénesis, organoides, autoensamblaje de péptidos