Clear Sky Science · es
El ayuno intermitente inhibe el glioma impulsado por Tp53 mediante la regulación metionina-m6A mediada por la microbiota intestinal
Por qué darle un respiro al intestino podría frenar tumores cerebrales mortales
El glioblastoma es uno de los cánceres cerebrales más agresivos, y los tratamientos actuales —cirugía, radioterapia y quimioterapia— a menudo solo conceden a los pacientes un poco más de tiempo. Este estudio plantea una pregunta simple pero con implicaciones importantes para la vida cotidiana: ¿puede la forma de comer, en concreto el ayuno intermitente, cambiar nuestras bacterias intestinales y la química sanguínea lo suficiente como para ralentizar de manera significativa ciertos tumores cerebrales?
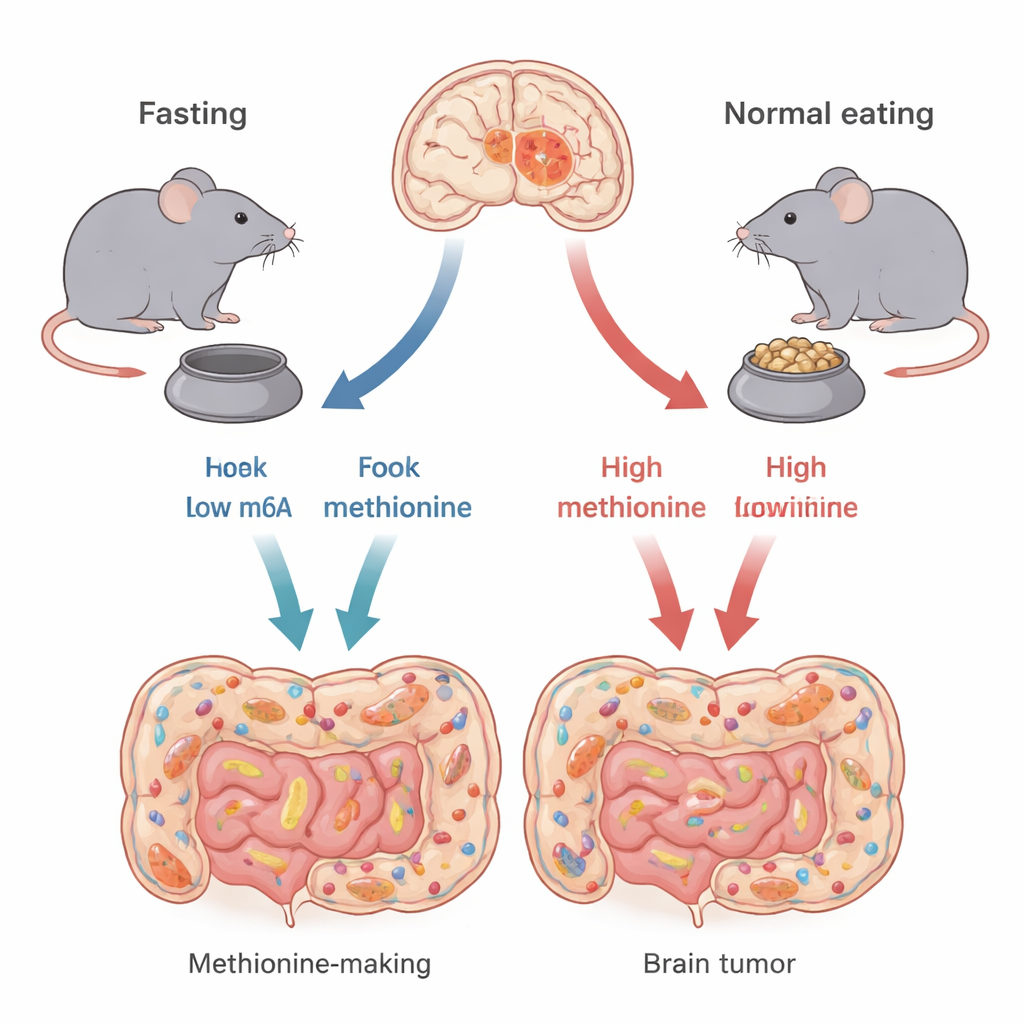
Diferentes tipos del “mismo” cáncer cerebral
No todos los glioblastomas son iguales. Los autores se centran en dos tipos genéticos principales, definidos por alteraciones en genes llamados TP53 y CDKN2A. Estos genes ayudan a controlar cómo las células crecen o mueren. Usando modelos murinos que imitan de cerca cada subtipo humano, los investigadores muestran que el ayuno intermitente —24 horas sin comer seguidas de 24 horas con comida— no beneficia por igual a todos los tumores cerebrales. Los ratones con tumores de tipo TP53 vivieron más tiempo y tuvieron tumores más pequeños cuando ayunaban, mientras que los ratones con tumores de tipo CDKN2A mostraron poco beneficio. Esto sugiere que la eficacia del ayuno puede depender en gran medida del cableado genético del tumor.
Del patrón alimentario a los microbios intestinales y a la química cerebral
El equipo preguntó entonces cómo ejerce el ayuno su efecto selectivo. Dado que la cantidad total de alimento se mantuvo igual entre los grupos, la diferencia clave fue el momento de comer. Ese timing remodeló de forma potente la microbiota intestinal —la vasta comunidad de bacterias en el intestino. En los ratones TP53 en ayuno, ciertos grupos bacterianos que fabrican eficientemente el aminoácido metionina, como cepas específicas de Alistipes y Prevotella, disminuyeron en abundancia. Como la metionina es un bloque de construcción esencial que los animales deben obtener de la dieta o de los microbios intestinales, este cambio microbiano supuso menos metionina fluyendo desde el intestino hacia la sangre y, en última instancia, hacia el cerebro.
Cómo un único nutriente ajusta señales que impulsan el cáncer
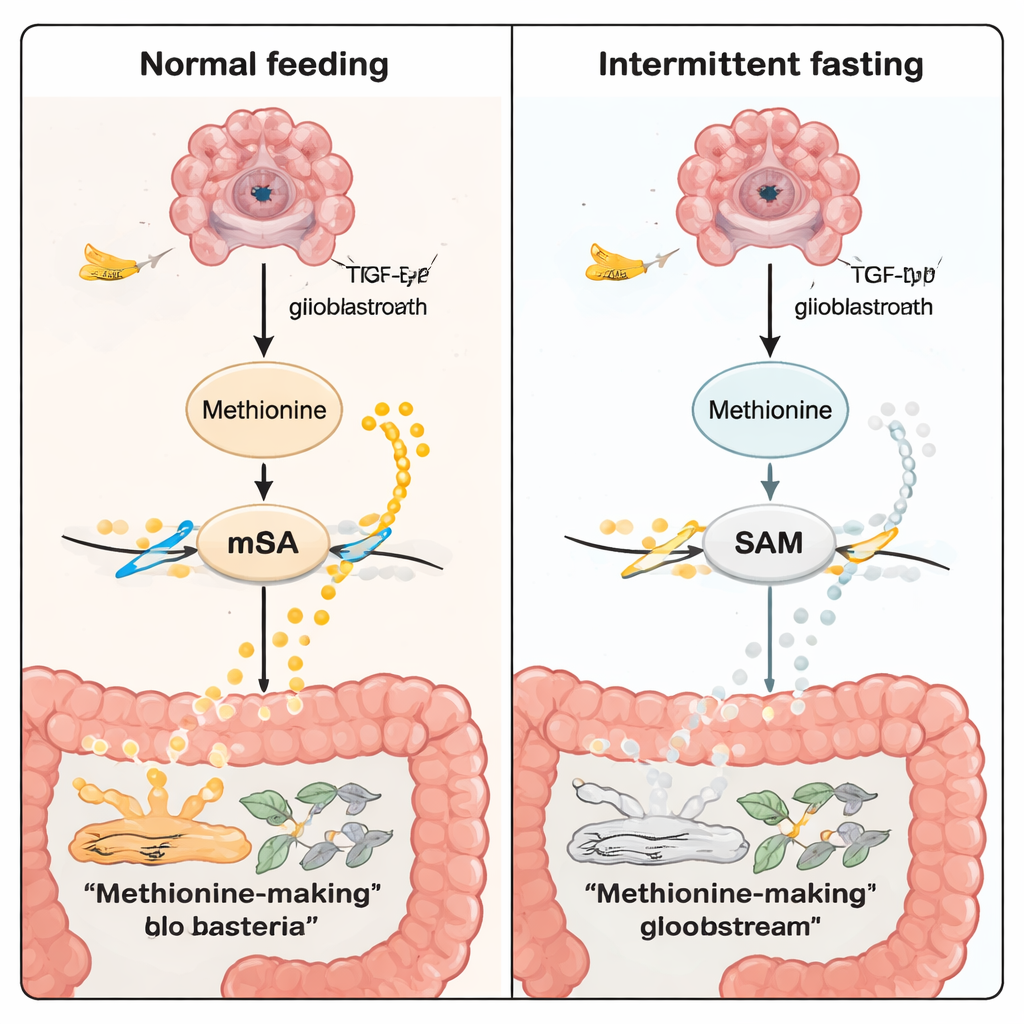
La metionina no es solo un nutriente; también es materia prima para la S-adenosilmetionina (SAM), el “donante de metilos” universal de la célula. La SAM alimenta un proceso químico de marcado sobre el ARN llamado m6A. Estas marcas ayudan a controlar la intensidad con que se expresan ciertos genes. En el modelo tumoral TP53, el ayuno redujo los niveles de metionina y de SAM en sangre y en regiones del tumor cerebral. Empleando varias capas de tecnologías ómicas —secuenciación de ARN estándar, perfilado de ARN a célula única y mapas espaciales tanto de actividad génica como de metabolitos— los investigadores encontraron menos marcas m6A en ARN vinculados al cáncer bajo ayuno. Un objetivo importante fue TGFB2, un gen de la vía de señalización TGF‑β, conocida por impulsar el crecimiento y la invasión tumoral. Con el ayuno, tanto la enzima METTL3 (que escribe las marcas m6A) como TGFB2 se redujeron, y la señalización TGF‑β se debilitó.
Demostrar causa y efecto con intervenciones dirigidas
Para ir más allá de la correlación, los científicos realizaron experimentos de “rescate”. Bloquearon METTL3 con un fármaco o transfirieron bacterias intestinales de ratones en ayuno a ratones alimentados normalmente, y observaron que el crecimiento tumoral se ralentizaba incluso sin ayuno —lo que respalda la idea de que tanto la microbiota como la maquinaria m6A son actores clave. A la inversa, cuando a ratones en ayuno se les administró metionina adicional o se trató con un fármaco que aumenta las marcas m6A, sus tumores crecieron más como los de ratones alimentados normalmente y la ventaja de supervivencia desapareció. De manera importante, alterar las bacterias intestinales con antibióticos de amplio espectro borró muchos de los cambios relacionados con el ayuno, subrayando que la comunidad intestinal es un eje central en esta cadena de eventos.
Qué significa esto para las personas y las terapias futuras
Para un lector no especializado, el mensaje principal es que no todos los cánceres, ni siquiera todos los glioblastomas, responderán igual a una estrategia dietética como el ayuno intermitente. En los gliomas tipo TP53, el ayuno parece “hablar” con el cerebro a través del intestino: remodela las bacterias intestinales, lo que a su vez reduce la producción de metionina, disminuye el marcado químico del ARN y atenúa señales potentes de crecimiento dentro de las células tumorales. Aunque este trabajo se ha realizado en ratones y requiere una traducción clínica cuidadosa, apunta hacia un futuro en el que patrones de vida simples, tratamientos basados en la microbiota intestinal y fármacos que apunten a la metionina o a las vías m6A puedan adaptarse al subtipo genético del tumor de cada paciente.
Cita: Lin, Y., Li, S., Xu, X. et al. Intermittent fasting inhibits Tp53-driven glioma through gut microbiota-mediated methionine-m6A regulation. Nat Commun 17, 1804 (2026). https://doi.org/10.1038/s41467-026-68512-2
Palabras clave: ayuno intermitente, glioblastoma, microbioma intestinal, metabolismo de la metionina, modificación de ARN m6A