Clear Sky Science · es
TET1 como regulador maestro que controla la vigilancia de la ferroptosis dependiente e independiente de GPX4 en la leucemia mieloide aguda
Por qué esta investigación importa para el tratamiento del cáncer
Muchos fármacos oncológicos nuevos intentan forzar a las células malignas a entrar en un modo de autodestrucción llamado ferroptosis, un tipo de muerte celular impulsada por el hierro y el daño lipídico. Sin embargo, algunos tumores resisten obstinadamente este enfoque. Este estudio revela cómo una proteína que modifica el ADN, llamada TET1, ayuda a las células leucémicas a eludir la ferroptosis mediante dos sistemas bioquímicos de defensa separados, y muestra que bloquear estas defensas puede volver vulnerables incluso a los cánceres resistentes.
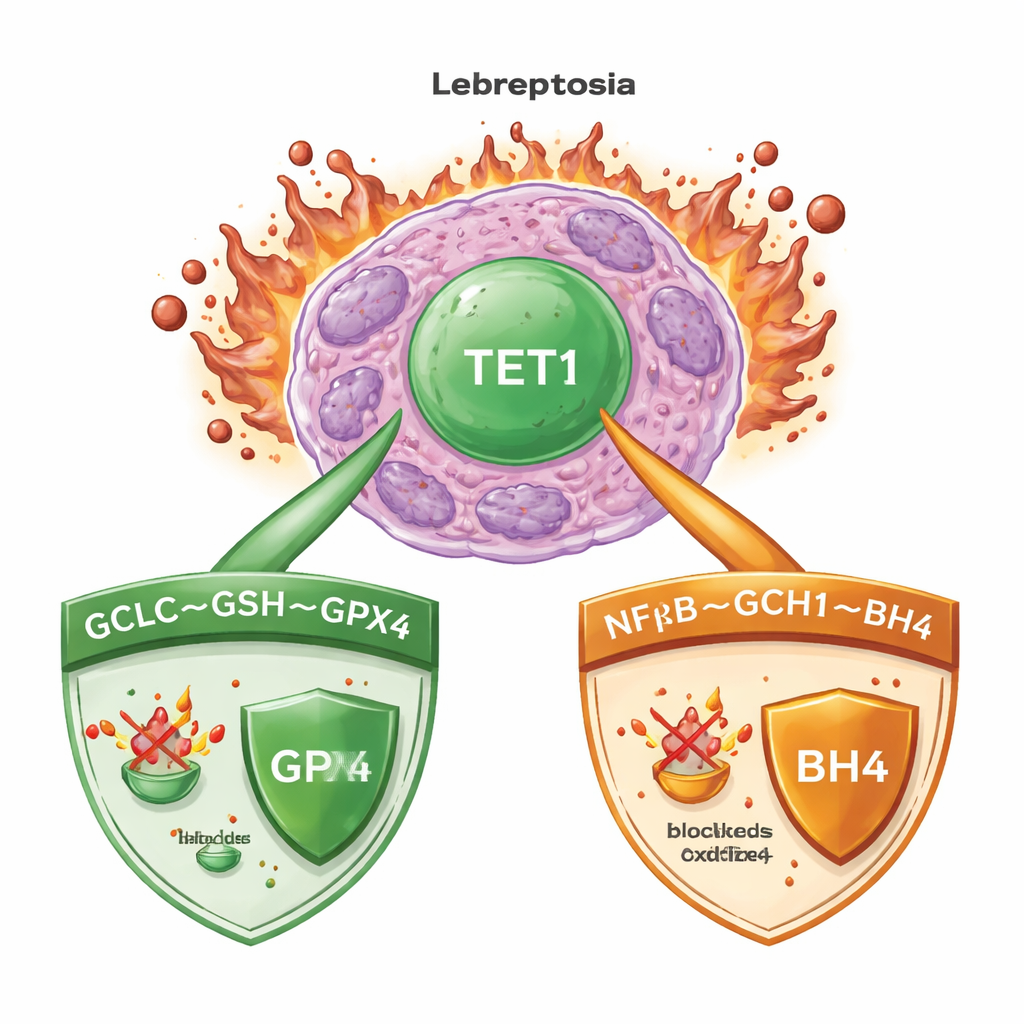
Una mezcla letal de hierro y lípidos dañados
La ferroptosis ocurre cuando el hierro alimenta la oxidación descontrolada de lípidos en las membranas celulares, lo que acaba provocando la ruptura de las células. En la leucemia mieloide aguda (LMA), como en muchos cánceres, las células despliegan potentes sistemas de vigilancia para mantener este proceso bajo control. Un guardián clave es la enzima GPX4, que utiliza una pequeña molécula llamada glutatión para neutralizar los peróxidos lipídicos dañinos. Otros sistemas de respaldo generan moléculas antioxidantes que pueden atrapar radicales peligrosos incluso cuando GPX4 está comprometida. Entender qué interruptores maestros coordinan estas defensas es crucial para diseñar terapias que desencadenen de forma fiable la ferroptosis en células cancerosas mientras preservan el tejido sano.
TET1 emerge como un centro de control central
Los investigadores compararon docenas de muestras de células cancerosas, incluidas muchas líneas de LMA y células derivadas de pacientes, y observaron un patrón claro: las células que resistían la ferroptosis mostraban niveles más altos de TET1, una enzima que modifica marcas químicas del ADN e influye en la actividad génica. Cuando redujeron los niveles de TET1 mediante herramientas genéticas o inhibieron su actividad con una pequeña molécula, las células cancerosas se volvieron notablemente más sensibles a fármacos inductores de ferroptosis. Esto se verificó tanto en placas de cultivo como en modelos murinos de LMA. Por el contrario, aumentar la expresión de TET1 protegía a las células de la muerte ferroptótica y limitaba la acumulación de especies reactivas de oxígeno, los subproductos químicamente agresivos que impulsan el daño a las membranas.
Fortaleciendo el principal escudo antioxidante
Al profundizar, el equipo mapeó dónde actúa TET1 en el genoma y descubrió que activa directamente un gen llamado GCLC. GCLC codifica una enzima crítica que inicia la producción de glutatión, el combustible de GPX4. Al aumentar una marca de ADN específica (5-hidroximetilcitosina) en el promotor de GCLC, TET1 incrementa la síntesis de glutatión. En condiciones nutricionales normales, esto refuerza la reserva antioxidante principal de la célula. Bajo esterilidad de cistina, el mismo complejo enzimático también produce péptidos γ-glutamil inusuales que ayudan a eliminar el exceso de glutamato, otra forma de atenuar la ferroptosis. Tanto en células en cultivo como en ratones, la pérdida de TET1 o la inhibición farmacológica de la síntesis de glutatión redujeron drásticamente los niveles de glutatión y de estos péptidos protectores, haciendo que las células leucémicas fueran mucho más vulnerables a los desencadenantes de la ferroptosis.
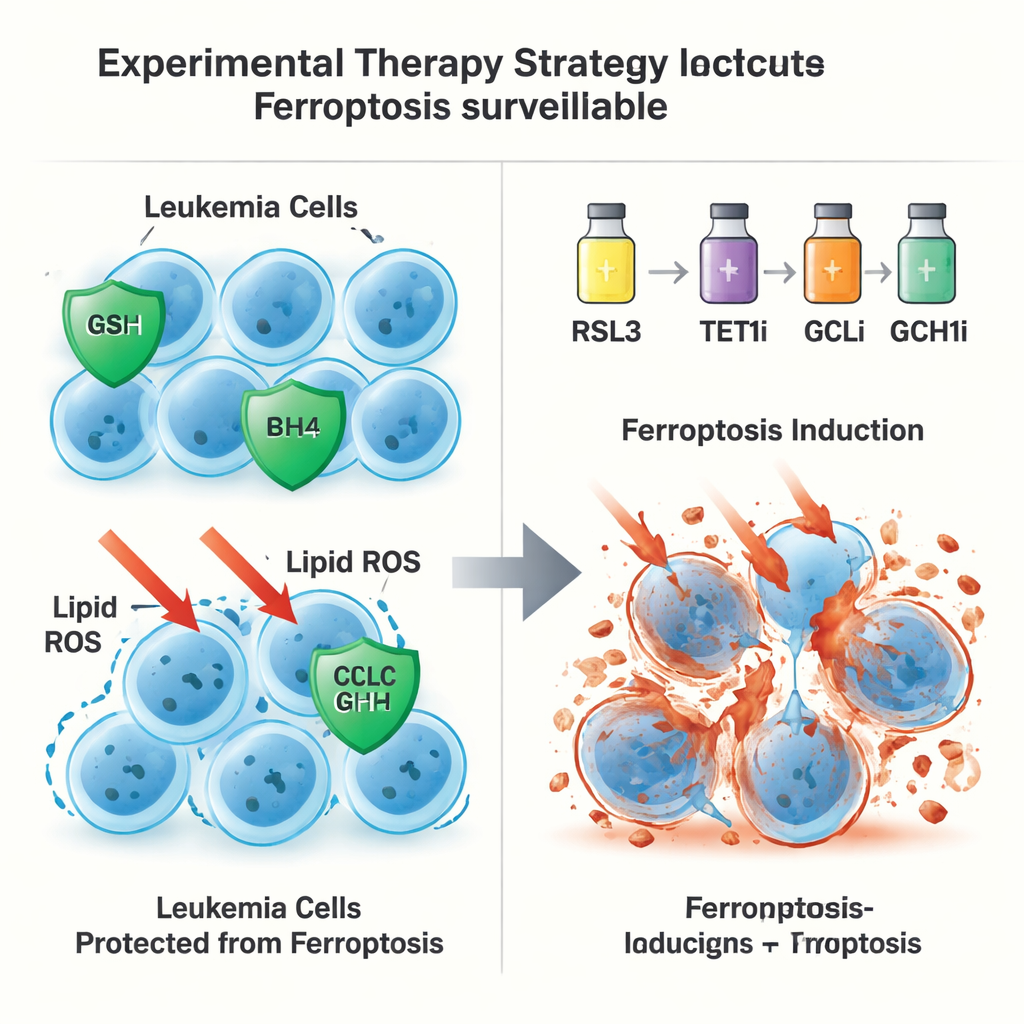
Una segunda vía de escape independiente de GPX4
Sorprendentemente, el papel protector de TET1 no terminó con el eje glutatión–GPX4. Incluso cuando GPX4 fue eliminada de las células leucémicas, un exceso de TET1 aún podía prevenir la muerte ferroptótica, lo que sugiere una segunda línea de defensa. Los autores rastrearon esto hasta la activación por TET1 de la vía de señalización NFκB, en particular de un componente llamado NFKB2. Esto, a su vez, aumenta la expresión de GCH1, una enzima que produce la molécula antioxidante BH4. BH4 puede proteger los lípidos de la membrana de la oxidación sin depender de GPX4. Cuando GCH1 fue silenciado genéticamente o bloqueado químicamente, la capacidad de TET1 para proteger a las células frente a la ferroptosis se perdió parcialmente. En conjunto, estos hallazgos definen una ruta TET1–NFKB2–GCH1 que constituye un sistema de vigilancia de la ferroptosis independiente de GPX4.
Convertir una debilidad en una oportunidad terapéutica
Con este mapa de dos vías, los investigadores probaron si estimular simultáneamente la ferroptosis y debilitar las defensas controladas por TET1 podría ofrecer una ventaja terapéutica. En modelos murinos de LMA y en injertos de leucemia derivados de pacientes en ratones, dosis bajas de un fármaco inductor de ferroptosis combinadas con inhibidores de TET1, de la síntesis de GSH (vía GCLC) o de GCH1 redujeron drásticamente la carga leucémica, prolongaron la supervivencia y agotaron las poblaciones de células iniciadoras de leucemia. Es importante destacar que el inductor de ferroptosis se usó en una fracción de las dosis reportadas en estudios previos, lo que reduce las preocupaciones sobre la toxicidad para las células madre sanguíneas normales.
Qué significa esto para las terapias contra el cáncer en el futuro
Para no especialistas, el mensaje clave es que las células leucémicas sobreviven manteniendo dos sistemas antioxidantes superpuestos, ambos coordinados por TET1: uno centrado en el glutatión y GPX4, y otro basado en GCH1 y BH4. Este trabajo muestra que, activando modestamente la ferroptosis mientras se bloquean TET1 y sus socios aguas abajo, los médicos podrían algún día superar la resistencia y empujar selectivamente a las células cancerosas al límite sin sobrecargar los tejidos sanos. Aunque estas estrategias aún no están listas para la clínica, el estudio identifica a TET1 como un potente nodo de control y un objetivo prometedor para terapias combinadas en LMA y potencialmente en otros cánceres difíciles de tratar.
Cita: Yang, L., Lu, J., Yun, W. et al. TET1 as a master regulator controlling GPX4-dependent and -independent ferroptosis surveillance in acute myeloid leukemia. Nat Commun 17, 1800 (2026). https://doi.org/10.1038/s41467-026-68509-x
Palabras clave: ferroptosis, leucemia mieloide aguda, TET1, glutatión, epigenética del cáncer