Clear Sky Science · es
Oxidación simultánea de sulfuros y reducción de sulfato para la homeostasis redox intracelular en condiciones fuertemente ácidas
Por qué limpiar gases tóxicos requiere microbios ingeniosos
Muchas industrias emiten sulfuro de hidrógeno, un gas venenoso con olor a huevos podridos que puede corroer equipos, contaminar el aire y dañar a los trabajadores. Para eliminarlo, los ingenieros recurren cada vez más a microbios que transforman el sulfuro en formas de azufre más seguras. Este artículo revela una estrategia microbiana inesperada: un Mycobacterium recién identificado que ejecuta dos vías químicas normalmente opuestas al mismo tiempo para detoxificar el sulfuro rápidamente y protegerse del daño interno, incluso en condiciones extremadamente ácidas.
Una lucha por el control en el ciclo del azufre
En la naturaleza, el ciclo del azufre lo impulsan dos reacciones opuestas. Algunos microbios oxidan el sulfuro (la forma más reducida y tóxica) hacia productos menos dañinos, como azufre elemental o sulfato, obteniendo energía en el proceso. Otros hacen lo contrario, reduciendo el sulfato de vuelta a sulfuro para poder sintetizar componentes celulares esenciales, como aminoácidos que contienen azufre. Porque estas reacciones se contrarrestan, los biólogos supusieron durante mucho tiempo que una sola célula evitaría ejecutar ambas simultáneamente; hacerlo parecería un despilfarro, como calentar y enfriar una casa con las ventanas abiertas. 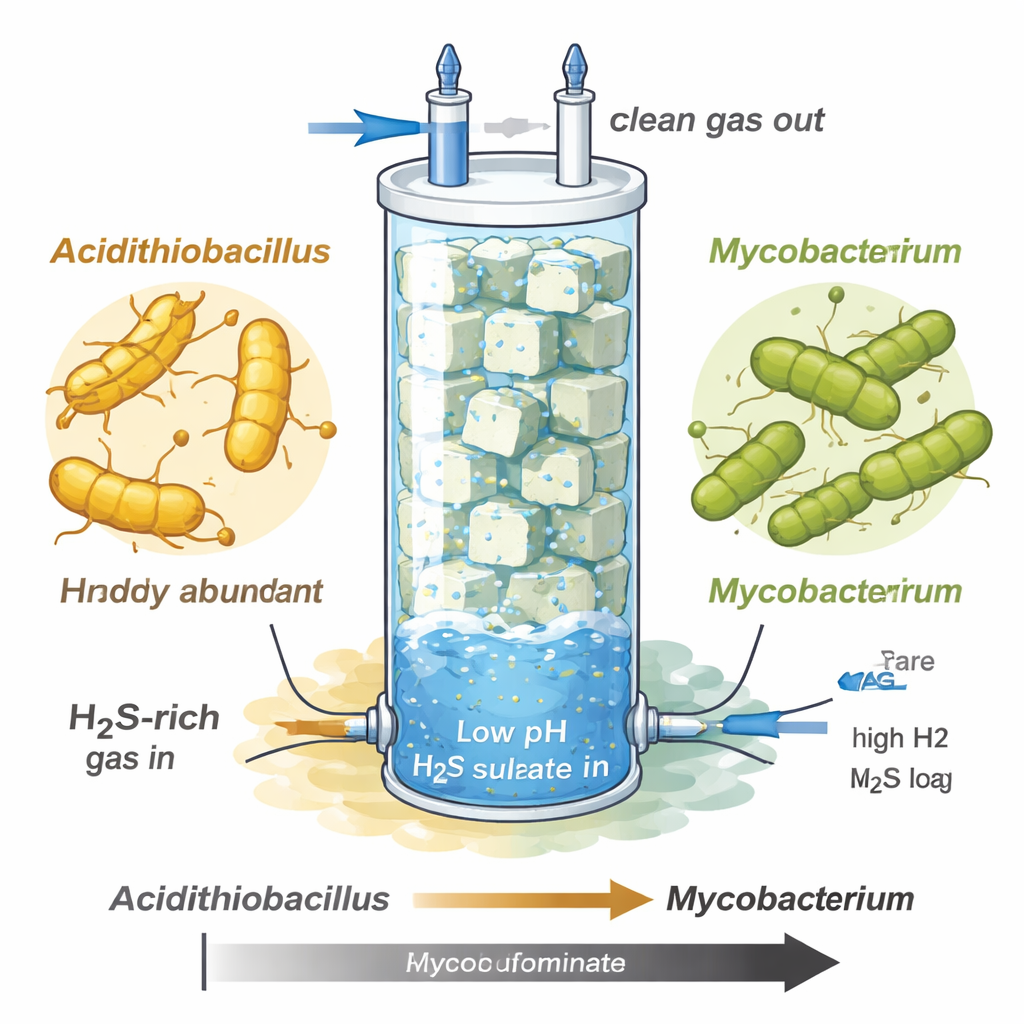
Encontrando un superviviente en un reactor extremo
Los investigadores estudiaron un filtro biotrickling—una columna de vidrio alta rellena de cubos de espuma—diseñado para depurar sulfuro de hidrógeno de corrientes de gas similares al biogás crudo o al gas natural. A medida que aumentaron la carga de sulfuro y mantuvieron el sistema muy ácido (pH alrededor de 1–1,5), la comunidad microbiana cambió de forma drástica. Al principio prosperó un conocido oxidante de sulfuro llamado Acidithiobacillus y transformó gran parte del sulfuro en sulfato, pero posteriormente colapsó bajo el extremo estrés por sulfuro. En su lugar, una especie de Mycobacterium previamente no caracterizada, etiquetada MAG-M116, pasó a dominar casi toda la comunidad, a pesar de crecer más lentamente en la fase temprana y menos severa.
Un microbio que rompe las reglas habituales
Los análisis genéticos y a nivel de proteínas mostraron que MAG-M116 posee una configuración metabólica inusual. Tiene una enzima clave, sulfuro:quinona oxidorreductasa, que oxida el sulfuro solo hasta azufre elemental sólido, que se acumula como partículas diminutas. Al mismo tiempo, el microbio dispone de un conjunto completo de genes para la reducción asimilatoria de sulfato, la vía que incorpora sulfato en la célula y lo reduce para sintetizar aminoácidos como cisteína y metionina. Bajo condiciones de alto sulfuro, ambas vías se activaron simultáneamente. La oxidación del sulfuro inyectó electrones en la maquinaria energética de la célula, mientras que la reducción de sulfato absorbió parte de ese flujo electrónico, conectando las dos direcciones del ciclo del azufre dentro de una sola célula.
Convertir un ciclo “derrochador” en una válvula de seguridad
Ejecutar ambas vías a la vez podría, en teoría, ser fútil—consumir energía sin ganancia neta. Pero el equipo demuestra que para MAG-M116 actúa como una válvula de seguridad frente al exceso de electrones. La oxidación de grandes cantidades de sulfuro libera una avalancha de electrones en la cadena respiratoria de la célula, que pueden filtrarse y generar especies reactivas del oxígeno (ROS), moléculas dañinas que atacan el ADN, las proteínas y las membranas. Al reducir activamente sulfato para fabricar aminoácidos, la célula desvía entre el 10 % y el 14 % de esos electrones hacia trabajo constructivo, reduciendo la acumulación de un estado sobremedido propenso a fugas. Experimentos comparando condiciones con y sin sulfato mostraron que la reducción activa de sulfato disminuyó la producción de ROS hasta en aproximadamente un 60 % y evitó la acumulación de cofactores reducidos que de otro modo alimentarían el daño oxidativo. 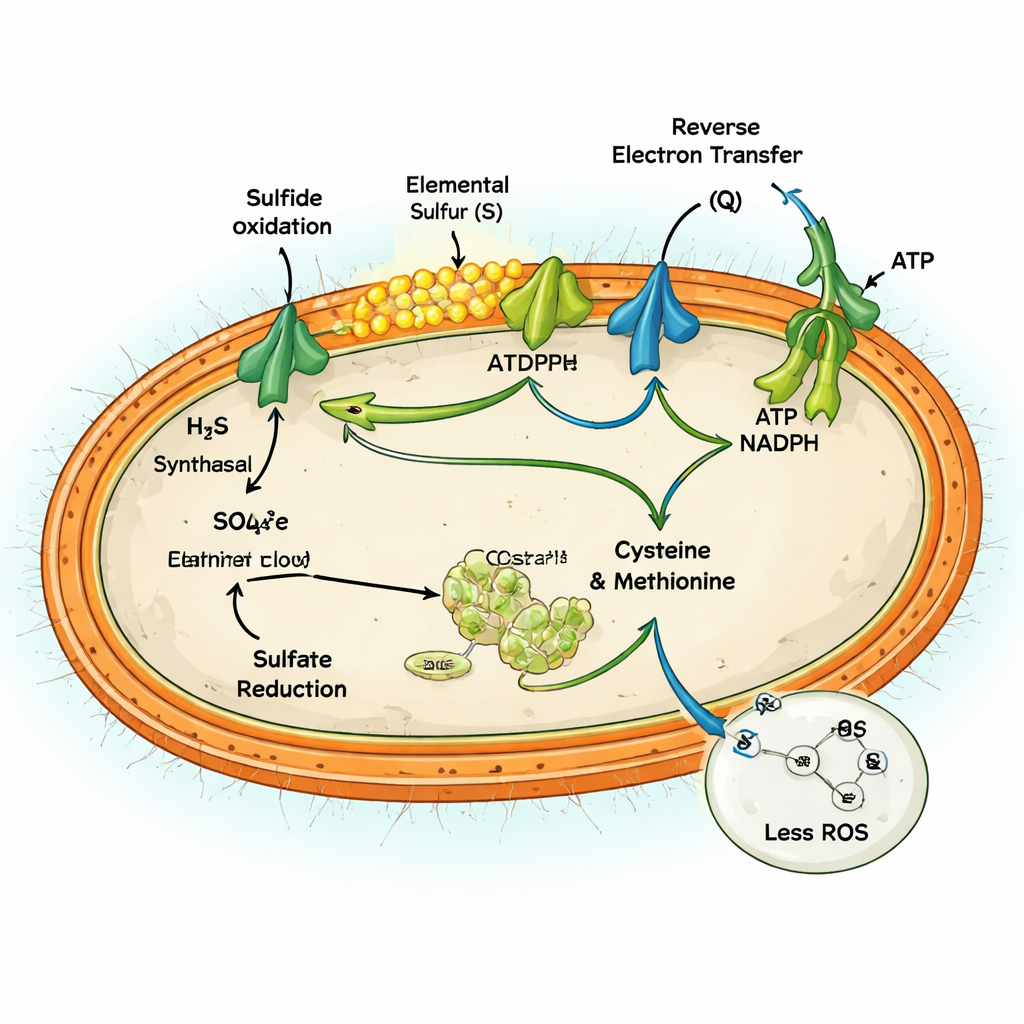
De gas tóxico a productos útiles
En las etapas posteriores de la operación del reactor, cuando MAG-M116 dominaba, casi todo el sulfuro de hidrógeno entrante se convirtió en azufre elemental sólido, en lugar de sulfato. Al mismo tiempo, los investigadores detectaron niveles crecientes de cisteína y metionina en la fase líquida, lo que sugiere que el microbio liberaba aminoácidos ricos en azufre en su entorno. Esta combinación—azufre elemental estable más compuestos orgánicos de azufre valiosos—convierte lo que antes era un contaminante peligroso en una mezcla de productos recuperables con usos en agricultura, materiales y sistemas energéticos.
Qué significa esto para la salud y la tecnología
Para un público no especializado, el mensaje clave es que este Mycobacterium ha resuelto un doble problema: puede depurar altos niveles de un gas tóxico mientras mantiene en equilibrio su propia química interna. Lo hace ejecutando reacciones de azufre de “empuje–tirón” que normalmente se mantendrían separadas, usando el ciclo supuestamente derrochador como un amortiguador incorporado para el exceso de electrones y los radicales de oxígeno dañinos. Este descubrimiento no solo sugiere nuevas formas de diseñar biorreactores robustos y de bajo pH para la eliminación de sulfuros y sulfatos, sino que también insinúa que microbios relacionados, incluidas especies de Mycobacterium patógenas, podrían emplear trucos similares para sobrevivir a ataques oxidativos dentro del cuerpo humano.
Cita: Jia, T., Peng, Y., Niu, L. et al. Simultaneous sulfide oxidation and sulfate reduction for intracellular redox homeostasis under highly acidic conditions. Nat Commun 17, 1797 (2026). https://doi.org/10.1038/s41467-026-68508-y
Palabras clave: ciclo del azufre, sulfuro de hidrógeno, Mycobacterium, homeostasis redox, biodesulfurización