Clear Sky Science · es
Una célula artificial capaz de la transducción de señales mediada por ADRB2 para la regulación de la glucogenólisis
Enseñar a las burbujas diminutas a comunicarse
Imagine una burbuja microscópica de jabón que puede detectar una señal semejante a una hormona en el exterior y luego “decidir” quemar el combustible almacenado en su interior, muy parecida a una célula humana real. Este estudio construye exactamente ese tipo de célula artificial, mostrando cómo imitaciones celulares hechas por el hombre pueden recibir un mensaje químico y convertirlo en una química energética controlada. Este trabajo nos acerca a portadores de fármacos inteligentes, tejidos fabricados en laboratorio y formas de vida sintéticas sencillas que pueden reaccionar ante su entorno.
Construir una célula de afuera hacia adentro
Las células reales escuchan constantemente su entorno a través de receptores en su membrana externa. Los autores se propusieron copiar una de estas vías naturales usando solo componentes purificados y simples burbujas lipídicas, llamadas vesículas gigantes. Se centraron en un receptor humano común, el receptor β2‑adrenérgico (ADRB2), que en nuestro cuerpo ayuda a controlar la frecuencia cardíaca, la función pulmonar y el uso de combustibles. Cuando este receptor encuentra un fármaco como la isoproterenol (ISO), normalmente desencadena una cadena interna de eventos que produce una molécula mensajera llamada AMP cíclico (cAMP), que a su vez controla cómo las células degradan el glucógeno, la forma de almacenamiento de glucosa del organismo. Reproducir toda esta secuencia en una célula artificial no se había logrado previamente.
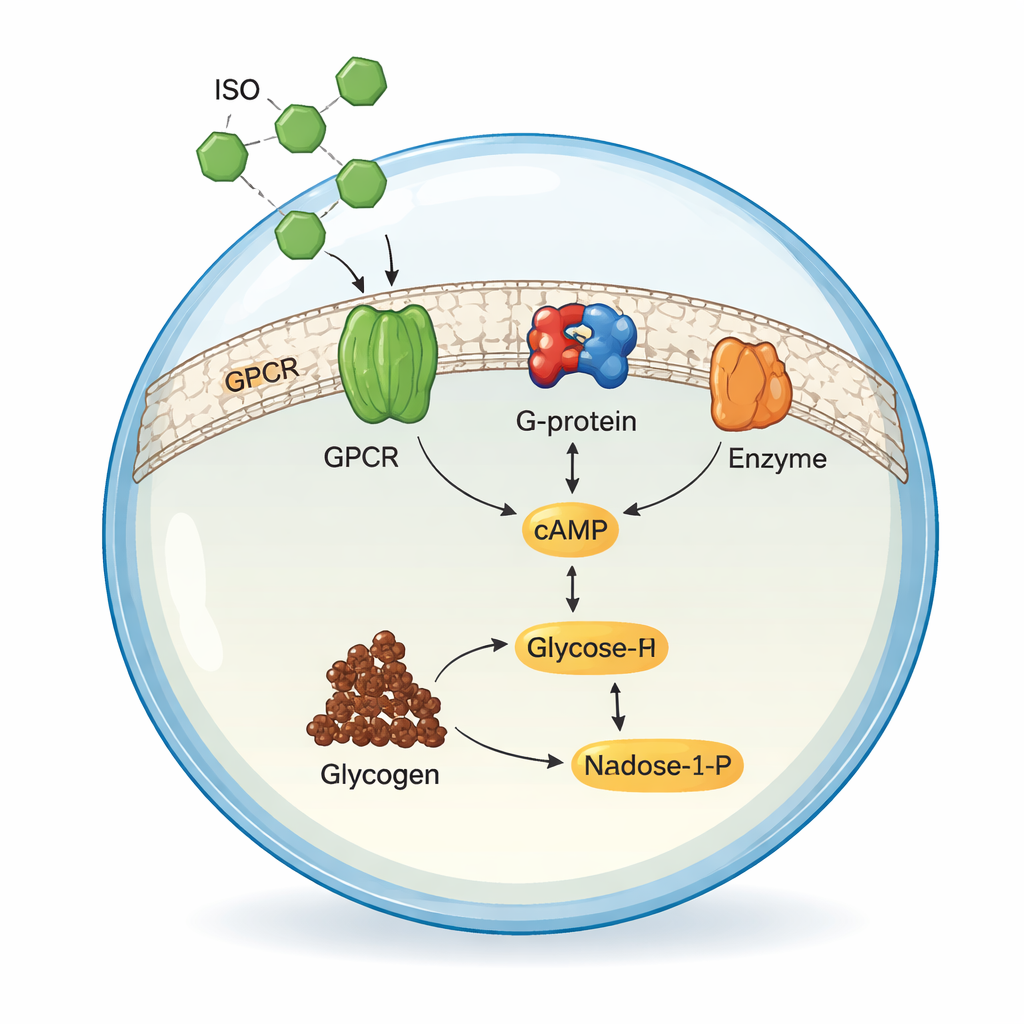
Recrear el primer relevo de la señal
El equipo primero reconstruyó las etapas tempranas de la vía de señalización en solución, fuera de cualquier membrana. Produjeron tres proteínas humanas en células de insecto: ADRB2, su subunidad asociada de proteína G (Gsα) y una enzima llamada adenilato ciclasa V (ADCY5), que produce cAMP a partir de ATP. Cuando mezclaron estas piezas con ISO bajo condiciones cuidadosamente ajustadas, la activación del receptor adrenérgico llevó a que ADCY5 convirtiera ATP en cAMP. Midiendo cAMP mediante cromatografía líquida de alta resolución, los investigadores optimizaron pH, temperatura y niveles de magnesio y encontraron que su sistema reconstituido funcionaba tan eficientemente como, o mejor que, muchas preparaciones previas, confirmando que la química central de la señalización estaba presente.
Instalar receptores reales en membranas artificiales
A continuación, los autores integraron las tres proteínas en las membranas de vesículas unilamelares gigantes—burbujas lipídicas de tamaño celular que sirven de chasis para las células artificiales. Etiquetaron fluorescente ADRB2 y ADCY5 para verificar que las proteínas se situaban en la membrana, se movían libremente y estaban presentes en gran número, con aproximadamente 1,8 millones de receptores por vesícula. Un tratamiento enzimático mostró que más del 94% de estos receptores miraban en la orientación correcta, con sus sitios de unión expuestos al exterior. Una sonda fluorescente de GTP confirmó que la unión de ISO en la membrana realmente activaba proteínas G dentro de las vesículas. Esto significaba que, en principio, las células artificiales podían transmitir una señal exterior de ISO a través de su membrana tal como lo hacen las células naturales.
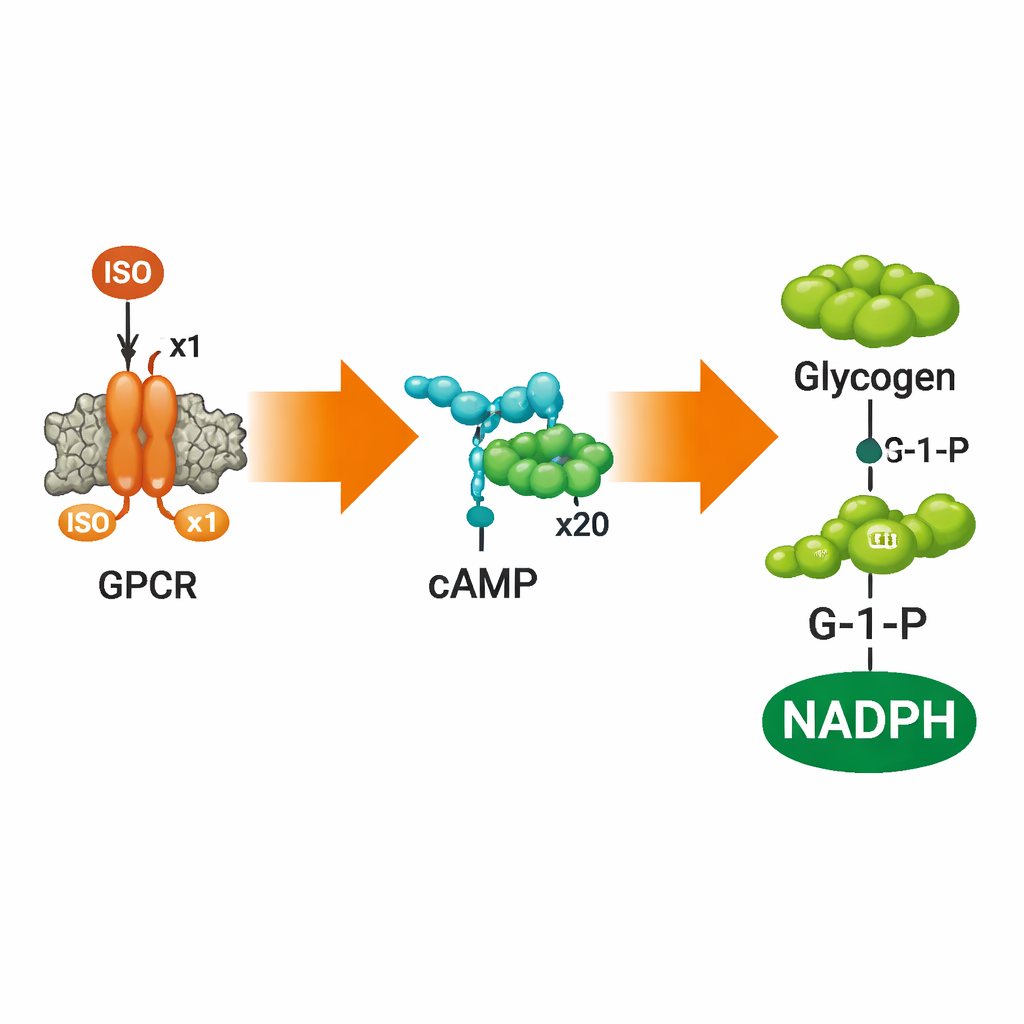
Convertir señales en degradación de combustible
Para ver si estas células sintéticas podían hacer algo útil con la señal, el equipo añadió un sensor de cAMP y luego una vía completa de degradación del glucógeno dentro de las vesículas. Usando una sonda de cAMP basada en FRET, mostraron que añadir ISO fuera de las vesículas provocaba un aumento de cAMP en el interior dependiente de la dosis y luego se estabilizaba a medida que los receptores se saturaban, reflejando el comportamiento clásico de los receptores acoplados a proteína G naturales. Fármacos que bloquean o silencian ADRB2—alprenolol y carazolol—apagaron esta respuesta exactamente como se esperaba. Cuando los autores también encapsularon cinco enzimas que normalmente convierten el glucógeno en glucosa‑1‑fosfato (G‑1‑P) y luego en NADPH, la estimulación con ISO condujo a la producción medible tanto de G‑1‑P como de NADPH dentro de las células artificiales, seguida por espectrometría de masas, cromatografía y fluorescencia.
Amplificar un susurro hasta un grito
Un hallazgo clave es la fuerte amplificación de la respuesta interna. Una cantidad modesta de ISO fuera de las vesículas produjo aproximadamente 22 veces más moléculas de cAMP que moléculas de ISO, y esta amplificación creció aún más a lo largo de la vía. Para cuando la señal había impulsado la degradación del glucógeno y su conversión a 6‑fosfogluconolactona acompañado de NADPH, la amplificación global superó el centenar de veces. Este impulso escalonado es un sello de la señalización hormonal natural y demuestra que el sistema artificial hace más que detectar ISO: procesa y amplifica el mensaje hasta producir una salida metabólica robusta.
Por qué esto importa para la vida sintética futura
Para un no especialista, los detalles técnicos se reducen a una idea simple: los investigadores han enseñado a una célula mínima hecha por el hombre a escuchar y reaccionar como una célula viva. Una molécula de fármaco externa se acopla a un receptor humano realista, una señal se transmite a través de una membrana sintética y una red enzimática interna responde movilizando energía química almacenada. Demostrar esta cadena completa—desde la activación del receptor hasta el metabolismo controlado—en un sistema artificial simplificado es un paso importante hacia células sintéticas autónomas que puedan detectar, decidir y actuar de formas útiles, por ejemplo ajustando su propio suministro de energía o liberando terapias solo cuando detecten las señales químicas adecuadas.
Cita: Liu, Y., Zhao, W., Zhao, Y. et al. An artificial cell capable of signal transduction mediated by ADRB2 for the regulation of glycogenolysis. Nat Commun 17, 1795 (2026). https://doi.org/10.1038/s41467-026-68503-3
Palabras clave: células artificiales, transducción de señales, GPCR, glucogenólisis, biología sintética