Clear Sky Science · es
Liberación de fármacos controlada espaciotemporalmente mediante un sistema click-release que utiliza mono-alquil-hidroxilamina y química de ciclooctino
Activar medicamentos potentes solo donde se necesitan
Muchos fármacos modernos son extremadamente potentes, lo cual es útil para combatir el cáncer o aliviar el dolor, pero conlleva riesgos para el resto del organismo. Este estudio describe un “interruptor” químico que permite mantener los medicamentos en una forma inactiva e inocua y activarlos únicamente en un lugar y momento elegidos, por ejemplo dentro de un tumor o en una pequeña zona que requiere anestesia local.
Un nuevo tipo de interruptor químico
Los investigadores parten del concepto de la “química click”, una familia de reacciones valoradas por ser rápidas, precisas y compatibles con ambientes biológicos. Las reacciones click clásicas unen dos moléculas de manera permanente. Aquí, el equipo invierte esa lógica: su reacción click está directamente ligada a la rotura de un enlace y a la liberación de un fármaco o una molécula señal. Los protagonistas son una molécula en forma de anillo llamada ciclooctino y una socia pequeña denominada mono-alquil-hidroxilamina. Cuando ambas se encuentran, se enlazan rápidamente y luego se reorganizan de modo que la “carga” unida se desprende. Al adjuntar distintos fármacos o tintes fluorescentes como carga, la misma reacción básica puede reutilizarse para múltiples propósitos. 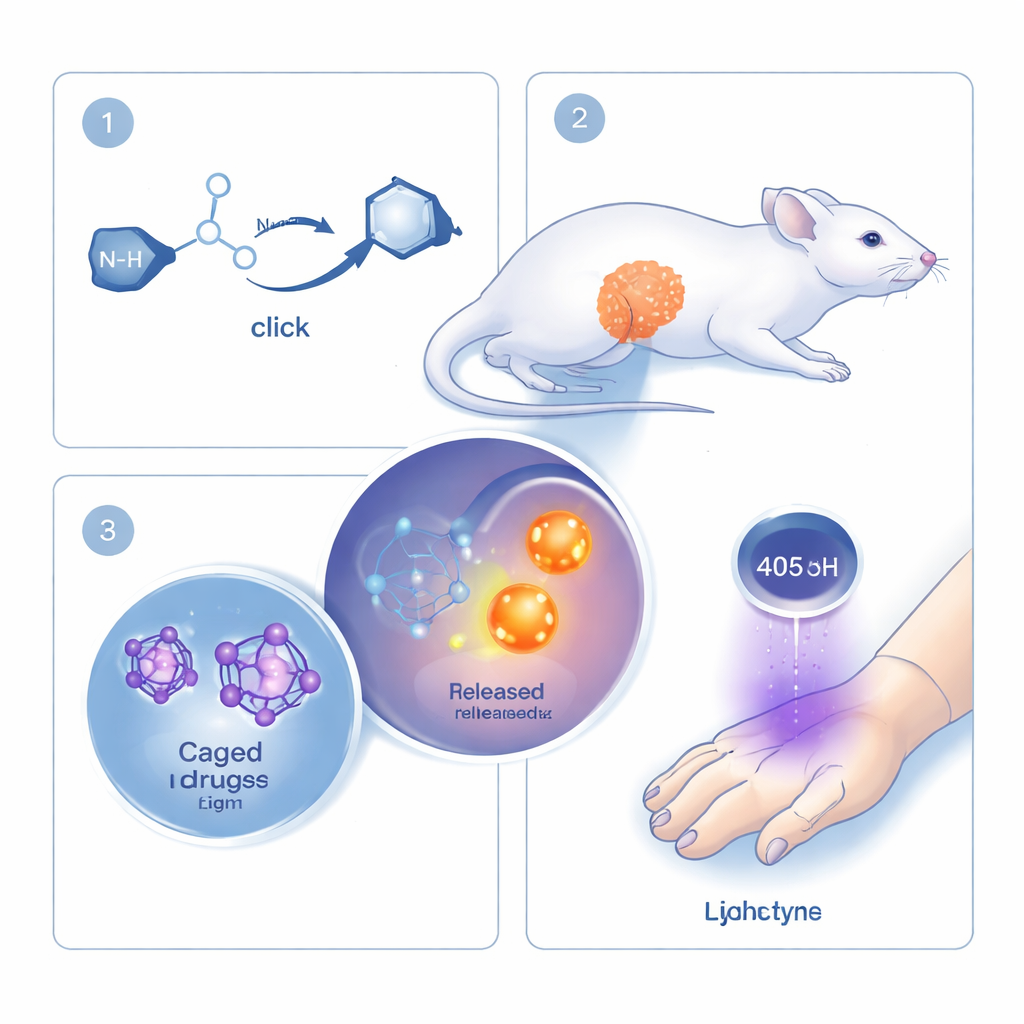
Liberación rápida y limpia dentro y fuera de las células
Para comprobar la practicidad de este interruptor, el equipo midió la velocidad de la reacción y el grado de liberación de la carga. Descubrieron que mono-alquil-hidroxilaminas cuidadosamente seleccionadas reaccionan mucho más rápido que la hidroxilamina simple, alcanzando conversiones cercanas al completo en minutos u horas, según la estructura. Es importante que los pasos químicos que liberan realmente la carga son tan rápidos y selectivos que casi toda la molécula unida se libera, con apenas subproductos residuales. Los autores probaron una gama de cargas, incluidos tintes fluorescentes e incluso un ion fluoruro, y mostraron que el sistema puede romper varios tipos de enlaces comunes en el diseño de fármacos, como carbamatos y éteres.
Iluminar células y activar fármacos contra el cáncer bajo demanda
A continuación, los investigadores avanzaron a células vivas. Primero ocultaron tintes fluorescentes brillantes tras el interruptor químico y añadieron estas sondas “encerradas” a células cancerosas. Por sí solas, las sondas permanecieron oscuras, lo que demuestra que las células no las activan accidentalmente. Cuando se añadió la pareja mono-alquil-hidroxilamina, los tintes se liberaron y las células se iluminaron en azul, verde o en el cercano infrarrojo, confirmando que la reacción funciona de manera fiable en un entorno biológico. Luego aplicaron la misma idea a la doxorrubicina, un fármaco quimioterapéutico muy utilizado. En su forma “encerrada”, el profármaco de doxorrubicina fue mucho menos tóxico para las células. Pero cuando estuvo presente la pareja click, el fármaco activo se liberó eficientemente, recuperando su capacidad para matar células cancerosas casi con la misma intensidad que la doxorrubicina libre.
Construir disparadores inteligentes para sitio y momento
Una limitación de muchos sistemas click existentes es que las partes reactivas están siempre “activas”, lo que dificulta controlar con precisión dónde y cuándo actúan. Para resolver esto, el equipo bloqueó temporalmente la reactividad de la mono-alquil-hidroxilamina con pequeñas tapas protectoras que solo se eliminan mediante disparadores específicos. Crearon versiones que responden a altos niveles de glutatión (una molécula abundante en muchos tumores), a enzimas y a destellos de luz violeta. En células y en ratones con tumores, la versión sensible al glutatión permaneció silenciosa en condiciones normales pero se activó en el entorno químicamente reductor del tumor, liberando tintes fluorescentes o activando el profármaco de doxorrubicina justo donde crecía el cáncer. Los ratones tratados con la combinación de profármaco más disparador mostraron una reducción tumoral mayor que los tratados con doxorrubicina estándar, mientras que experimentaron menor exposición al fármaco en órganos sensibles como el corazón.
Anestesia local controlada a distancia con luz
Para demostrar el control temporal, los autores diseñaron una segunda aplicación: anestesia local guiada por luz. Unieron el anestésico tetracaína a su andamiaje de ciclooctino, dejándolo inactivo, y mezclaron este profármaco con una versión foto-sensible de la hidroxilamina en un gel termorresponsive. Inyectada en la pata de una rata, la mezcla no tuvo efecto hasta que la piel fue iluminada con luz de 405 nanómetros. La iluminación activó la reacción click-release, liberando tetracaína y produciendo un entumecimiento comparable al de una inyección directa de tetracaína. Al variar la duración e intensidad de la luz, los investigadores pudieron ajustar la duración del bloqueo nervioso, e incluso desencadenar oleadas repetidas de anestesia a partir de una sola inyección. 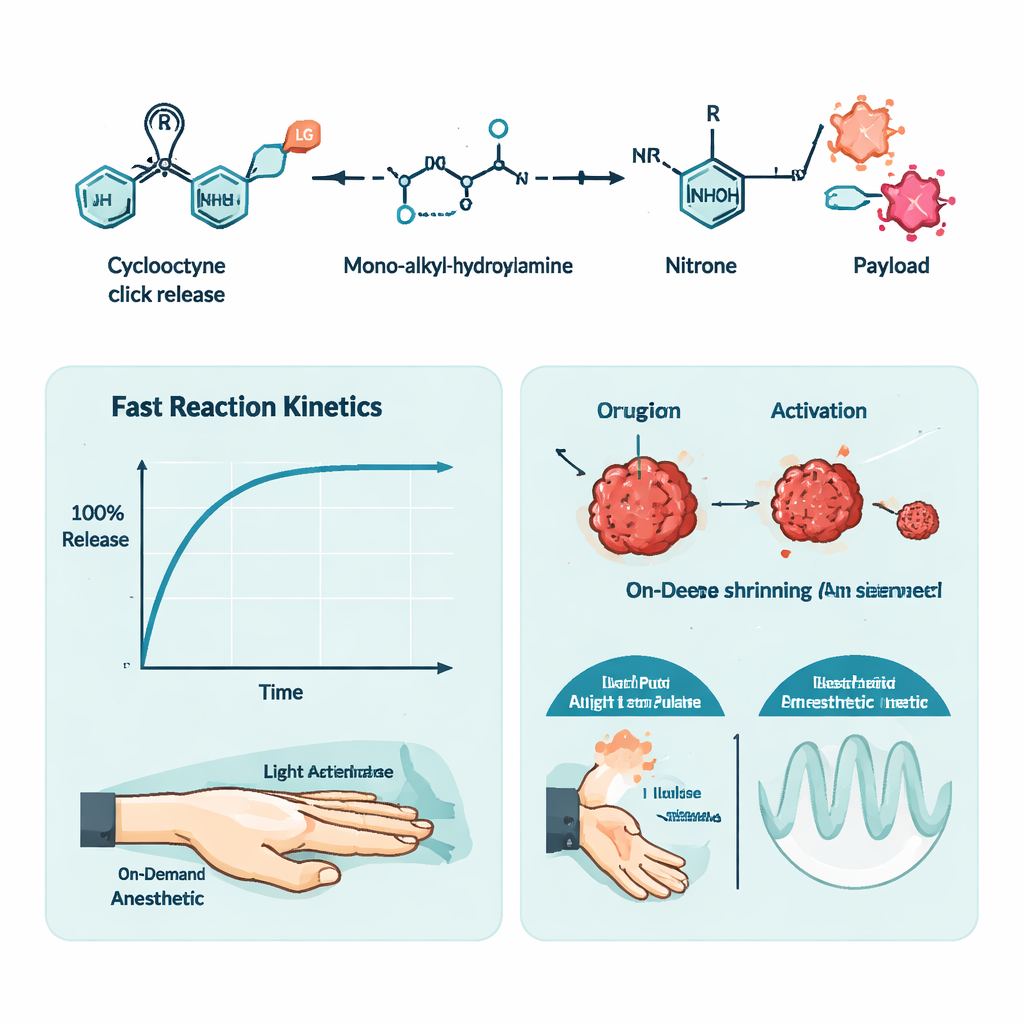
Qué podría significar esto para tratamientos futuros
Para lectores no especialistas, el mensaje clave es que este trabajo ofrece un control químico remoto y flexible para medicamentos: los fármacos pueden entregarse en una forma segura y silenciosa y luego activarse solo en el lugar y momento adecuados, usando señales procedentes del propio organismo o de una fuente de luz externa. Aunque se requieren más pruebas antes del uso clínico, el enfoque podría, con el tiempo, hacer que los tratamientos contra el cáncer sean más dirigidos y menos tóxicos, permitir un control del dolor personalizable tras cirugías y respaldar otras terapias que se benefician de un control espaciotemporal preciso.
Cita: Xu, X., Tong, X., Shi, Y. et al. Spatiotemporally controlled drug release via a click-release system utilizing mono-alkyl-hydroxylamine and cyclooctyne chemistry. Nat Commun 17, 1794 (2026). https://doi.org/10.1038/s41467-026-68502-4
Palabras clave: química click, administración dirigida de fármacos, profármacos, microambiente tumoral, anestesia controlada por fotoestimulación