Clear Sky Science · es
Electrosíntesis selectiva de urea a partir de nitrato y dióxido de carbono con bajo sobretensión
Convertir residuos en fertilizante
La agricultura moderna depende en gran medida del fertilizante de urea, pero su fabricación convencional consume mucho combustible fósil y libera grandes cantidades de dióxido de carbono. Este estudio explora una vía más limpia: usar electricidad y materiales diseñados específicamente para transformar directamente dióxido de carbono y nitrato —ambos contaminantes comunes— en urea en condiciones suaves. Si se escala, un proceso así podría ayudar a alimentar a la población al tiempo que reduce las emisiones de gases de efecto invernadero y aprovecha mejor los flujos de residuos.
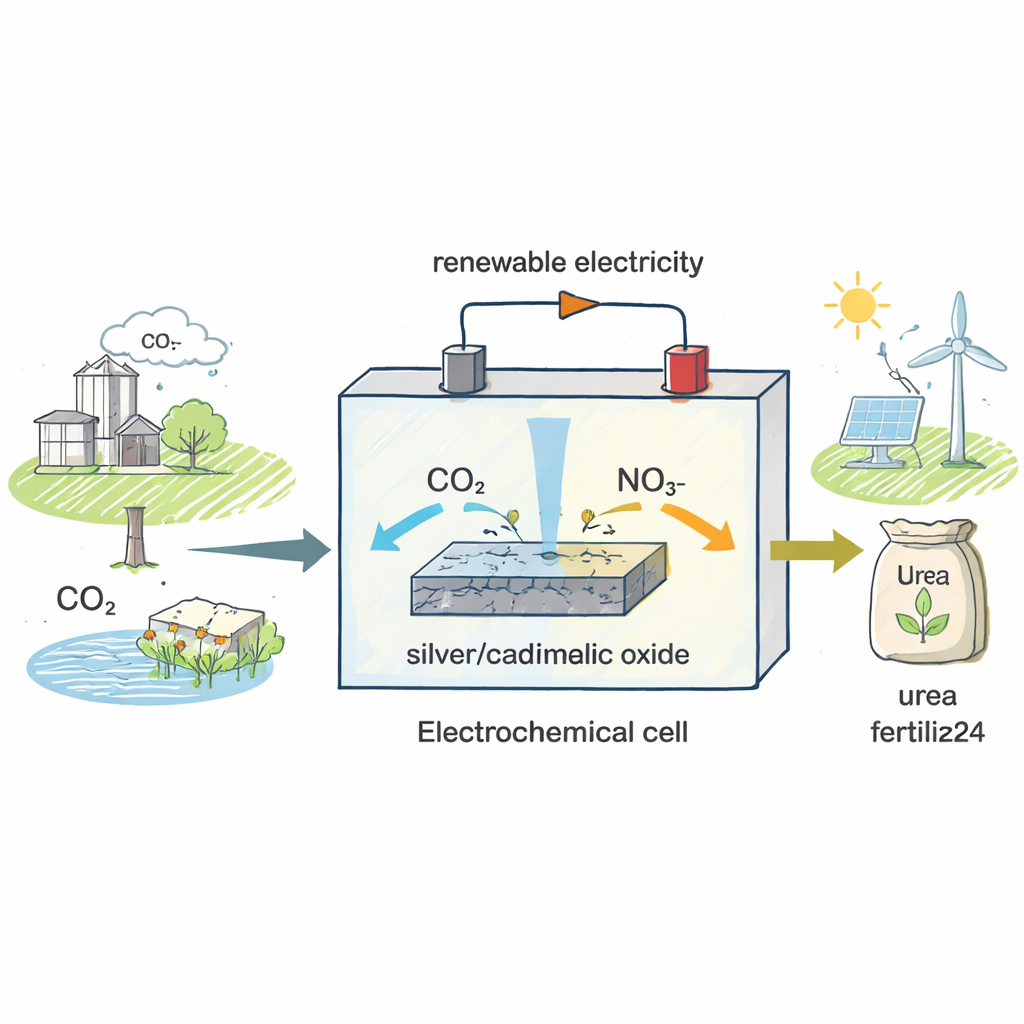
Una nueva forma de fabricar un fertilizante antiguo
Las fábricas de urea actuales operan a altas temperaturas y presiones y dependen de que primero se produzca amoníaco a partir del nitrógeno gaseoso, un paso que por sí solo consume más del 2% de la energía mundial. Los autores se propusieron sortear esta vía intensiva en energía. En lugar de partir del nitrógeno gaseoso, usan nitrato, un compuesto nitrogenado presente en escorrentías agrícolas y aguas residuales industriales, y lo combinan con dióxido de carbono, el principal gas de efecto invernadero. Ambas sustancias se introducen en una celda electroquímica —un dispositivo en el que la electricidad impulsa reacciones químicas— de manera que, con el catalizador adecuado, puedan unirse para formar urea a temperatura ambiente y voltajes relativamente bajos.
Diseñar una superficie útil
El núcleo del dispositivo es un catalizador sólido formado por diminutas partículas que combinan plata (Ag) con óxido de cadmio (CdO). Técnicas de microscopía y de rayos X muestran que estas partículas forman “heteroestructuras” íntimas, donde la plata metálica y el CdO se contactan a escala nanométrica y se intercambian electrones. Esta interacción electrónica modifica sutilmente cómo cada componente enlaza con las moléculas entrantes. En condiciones de trabajo, la porción de CdO se transforma en carbonato de cadmio (CdCO₃) que contiene átomos de oxígeno ausentes, conocidos como vacantes de oxígeno. Estos huecos actúan como pequeños puntos de anclaje que ayudan a capturar y activar el dióxido de carbono, mientras que las regiones próximas de plata son especialmente eficaces para atraer especies con nitrógeno derivadas del nitrato.
Producir urea de forma eficiente y selectiva
Cuando dióxido de carbono y nitrato fluyen por este catalizador Ag/CdO en una celda de laboratorio, el material los convierte en urea con una “sobretensión” inusualmente baja, es decir, el voltaje extra respecto al requerimiento termodinámico ideal es pequeño. En una celda en forma de H simple, la composición optimizada, llamada Ag₀.₀₇/CdO, alcanza una selectividad hacia urea de aproximadamente el 50% a apenas −0,10 voltios frente a una referencia estándar, y produce poco amoníaco o monóxido de carbono como subproductos. En una celda de flujo más avanzada, donde gases y líquidos se suministran continuamente, ese mismo catalizador logra una alta tasa de producción de urea de alrededor de 112 milimoles por gramo de catalizador por hora a −0,15 voltios. Mediante más optimización del diseño del reactor y de las condiciones de operación, el equipo eleva la tasa de producción hasta unos 427 milimoles por gramo por hora a corrientes más altas, manteniendo el rendimiento durante 1.000 horas de operación continua, una señal importante de estabilidad.
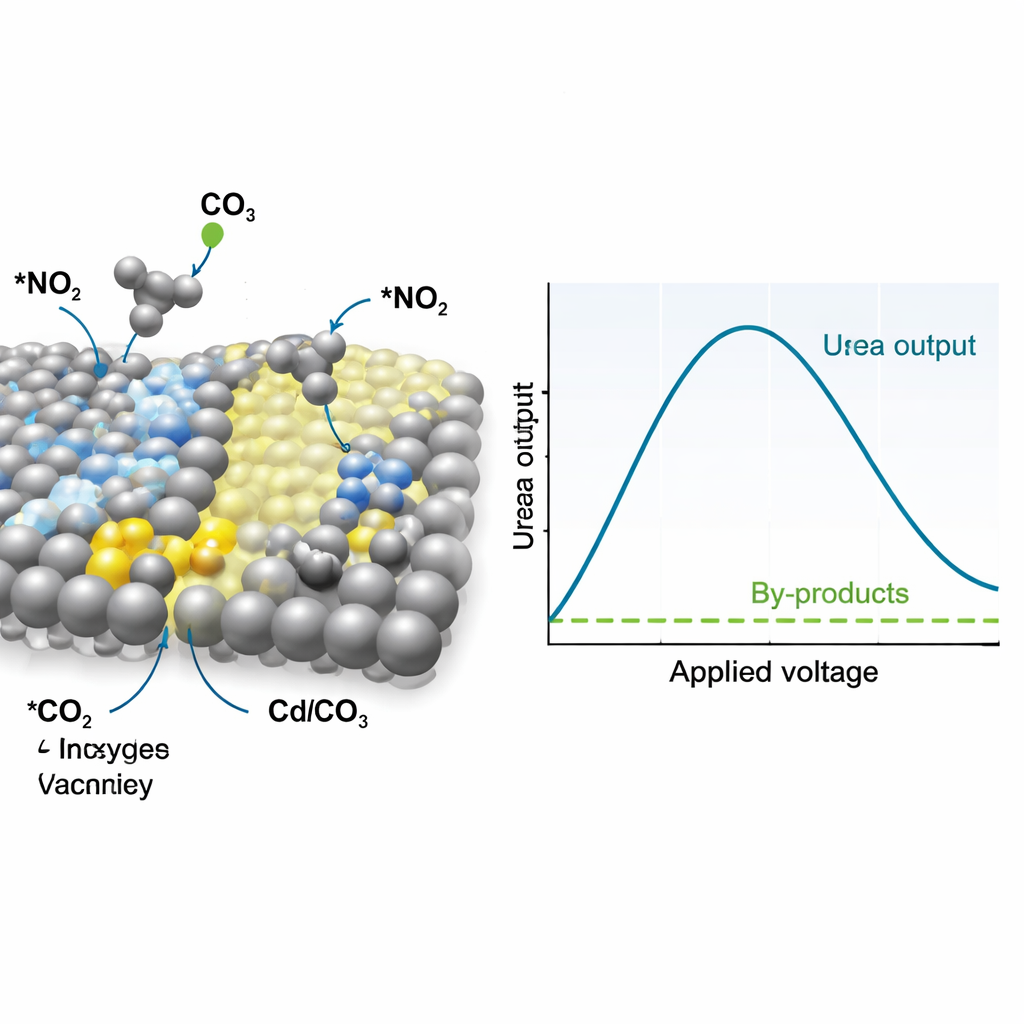
Cómo el catalizador orienta la reacción
Para entender por qué este material funciona tan bien, los investigadores siguieron en tiempo real el catalizador y los intermedios de reacción mediante espectroscopía Raman e infrarroja, junto con sondas avanzadas de rayos X. Estas medidas indican que los sitios de plata convierten preferentemente el nitrato en un intermedio reactivo descrito con frecuencia como *NO₂, mientras que el CdCO₃ reconstruido con vacantes de oxígeno enlaza el dióxido de carbono y lo convierte en *CO, otro intermedio de corta duración. Aparecen señales asociadas a enlaces carbono–nitrógeno en los voltajes de operación, mostrando que *NO₂ y *CO se acoplan temprano en el proceso para formar una especie similar a la urea en lugar de desviarse hacia la formación separada de amoníaco o monóxido de carbono. Simulaciones por ordenador respaldan este panorama, revelando que la interfaz entre la plata y el CdCO₃ rico en vacantes reduce la barrera energética para este paso clave de acoplamiento C–N y lo hace más favorable que las reacciones competidoras.
Qué podría significar para los fertilizantes y el clima
En conjunto, el trabajo demuestra que superficies catalíticas cuidadosamente diseñadas pueden guiar moléculas residuales sencillas como el dióxido de carbono y el nitrato por una vía energéticamente eficiente hacia la urea, en condiciones suaves y con larga vida útil. Para un lector no especialista, la conclusión clave es que el equipo ha construido una especie de “filtro electrónico” que prefiere unir carbono y nitrógeno en urea en lugar de permitir que escapen como otros productos. Aunque la implementación real exigirá abordar cuestiones como el coste del material, la ingeniería del reactor y el abastecimiento seguro de cadmio, el estudio ofrece un plano para la futura producción de fertilizantes que podría alimentarse con electricidad renovable y alinearse con un ciclo del carbono y del nitrógeno más sostenible.
Cita: Liu, S., Wang, T., Liu, J. et al. Selective electrosynthesis of urea from nitrate and carbon dioxide with low overpotential. Nat Commun 17, 1787 (2026). https://doi.org/10.1038/s41467-026-68497-y
Palabras clave: electrosíntesis de urea, utilización de dióxido de carbono, reducción de nitratos, diseño de electrocatalizadores, fertilizante verde