Clear Sky Science · es
Identificación de péptidos antimicrobianos en microbiomas intestinales antiguos
Excavar pistas antiguas para combatir gérmenes modernos
A medida que la resistencia a los antibióticos aumenta en todo el mundo, a los médicos se les acaban las opciones para tratar infecciones peligrosas. Este estudio adopta un enfoque inusual: no mira a laboratorios químicos de alta tecnología, sino a los restos fosilizados de heces humanas —«cápsulas del tiempo» intestinales antiguas— para descubrir moléculas naturales que combaten gérmenes y que podrían seguir siendo eficaces frente a las bacterias actuales.
Microbios antiguos como botiquines escondidos
Mucho antes de la medicina moderna, el intestino humano ya era un campo de batalla donde microbios beneficiosos y gérmenes invasores competían por espacio y alimento. Muchas bacterias intestinales amistosas producen péptidos antimicrobianos—fragmentos proteicos cortos que perforan las células bacterianas o las desactivan de otras maneras. La investigación moderna ha buscado principalmente en los microbiomas actuales estos péptidos letales para gérmenes. Pero nuestras comunidades intestinales contemporáneas han evolucionado junto al uso de antibióticos y los estilos de vida modernos, lo que ha dado a las bacterias dañinas muchas oportunidades para desarrollar resistencia. En contraste, las comunidades intestinales antiguas, preservadas en heces secas llamadas coprolitos, se formaron en un mundo sin antibióticos recetados. Eso las convierte en una fuente prometedora de defensas «olvidadas» que los patógenos modernos quizá aún no sepan cómo eludir.
Una herramienta de IA ligera para leer ADN fosilizado
Para explorar esta farmacia antigua, los investigadores construyeron una nueva herramienta informática llamada AMPLiT (AMP Lightweight Identification Tool). En lugar de necesitar grandes superordenadores, AMPLiT funciona de forma eficiente en un portátil corriente y mantiene al mismo tiempo alta precisión. Escanea enormes conjuntos de datos de ADN de muestras del microbioma y marca las secuencias cortas que probablemente codifican péptidos antimicrobianos. El equipo afinó el diseño de AMPLiT para que pudiera manejar millones de fragmentos de ADN dañado, con siglos de antigüedad, en cuestión de horas, reduciendo el tiempo de entrenamiento aproximadamente un 80% en comparación con métodos anteriores, y conservando a la vez un rendimiento cercano al estado del arte en la detección de candidatos probables contra gérmenes.
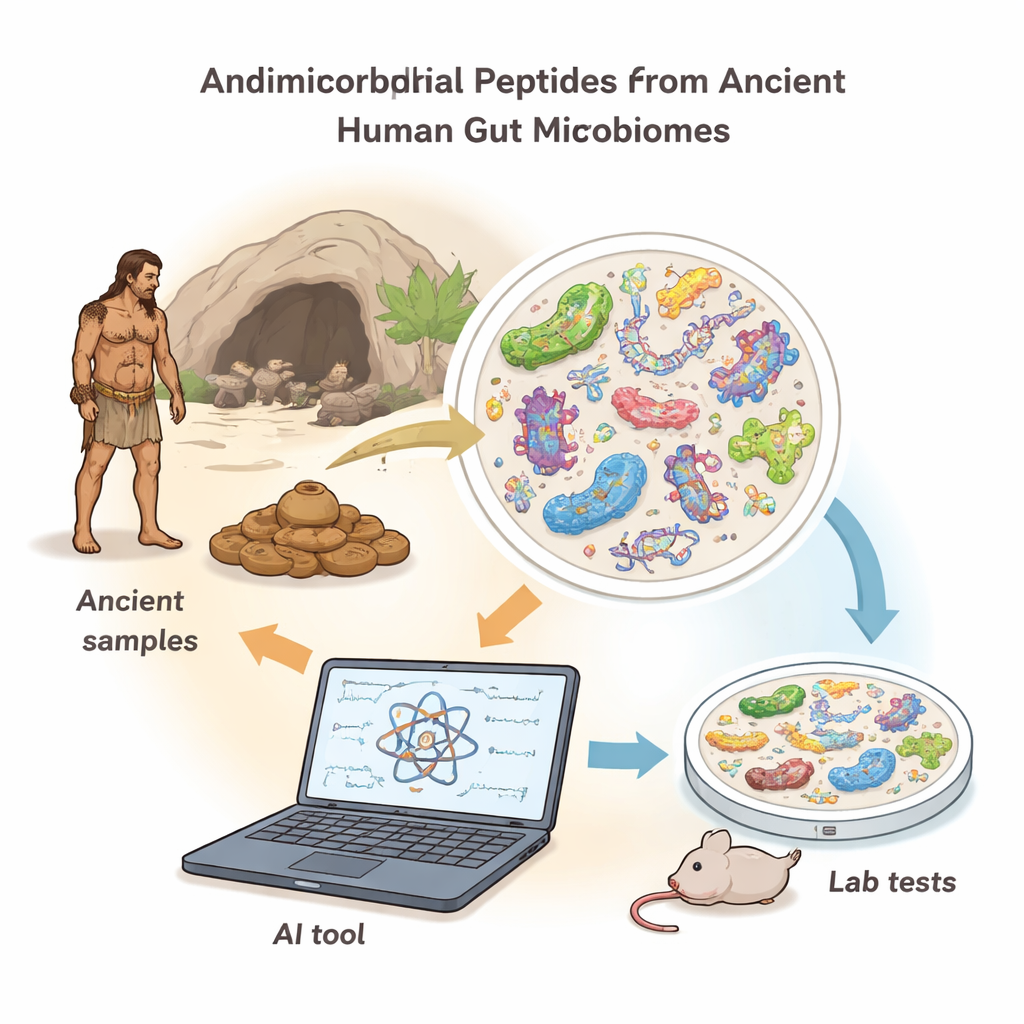
Resucitando asesinos de gérmenes de un habitante intestinal antiguo
Usando AMPLiT, los científicos examinaron el ADN intestinal de siete humanos antiguos que vivieron hace 1.000–2.000 años en Norteamérica. Tras eliminar la contaminación ambiental y centrarse en longitudes de péptido cortas y prácticas, la herramienta predijo cientos de miles de posibles secuencias antimicrobianas. Una serie de filtros más estrictos—presencia en varios individuos, propiedades químicas y baja toxicidad predicha—redujo esto a 41 candidatos de alta confianza, 40 de los cuales pudieron sintetizarse químicamente en el laboratorio. Cuando se probaron frente a bacterias «Gram-positivas» y «Gram-negativas» (dos grandes grupos que incluyen muchos patógenos comunes), 36 de los 40 péptidos ralentizaron o detuvieron el crecimiento bacteriano a dosis relativamente bajas, una tasa de éxito inusualmente alta para este tipo de descubrimiento.
La estrella sorprendente: un aliado intestinal en retroceso
Unos dos tercios de los péptidos más activos procedían de una sola bacteria intestinal: Segatella copri, pariente cercana de un microbio que antes se agrupaba bajo Prevotella copri. Esta especie fue abundante en intestinos antiguos y aún es común en personas con dietas más tradicionales y menos industrializadas, pero hoy es rara en muchas poblaciones urbanas de estilo occidental. Al rastrear dónde se sitúan los genes de los péptidos en el genoma de Segatella, el equipo descubrió que la mayoría son en realidad fragmentos de genes domésticos más grandes y cotidianos que el microbio parece haber reutilizado como armas—un truco evolutivo eficiente. Muchos de estos péptidos antiguos se ven bastante diferentes de los presentes en bases de datos modernas, lo que sugiere que representan diseños químicos genuinamente nuevos, no solo variaciones menores de antibióticos conocidos.
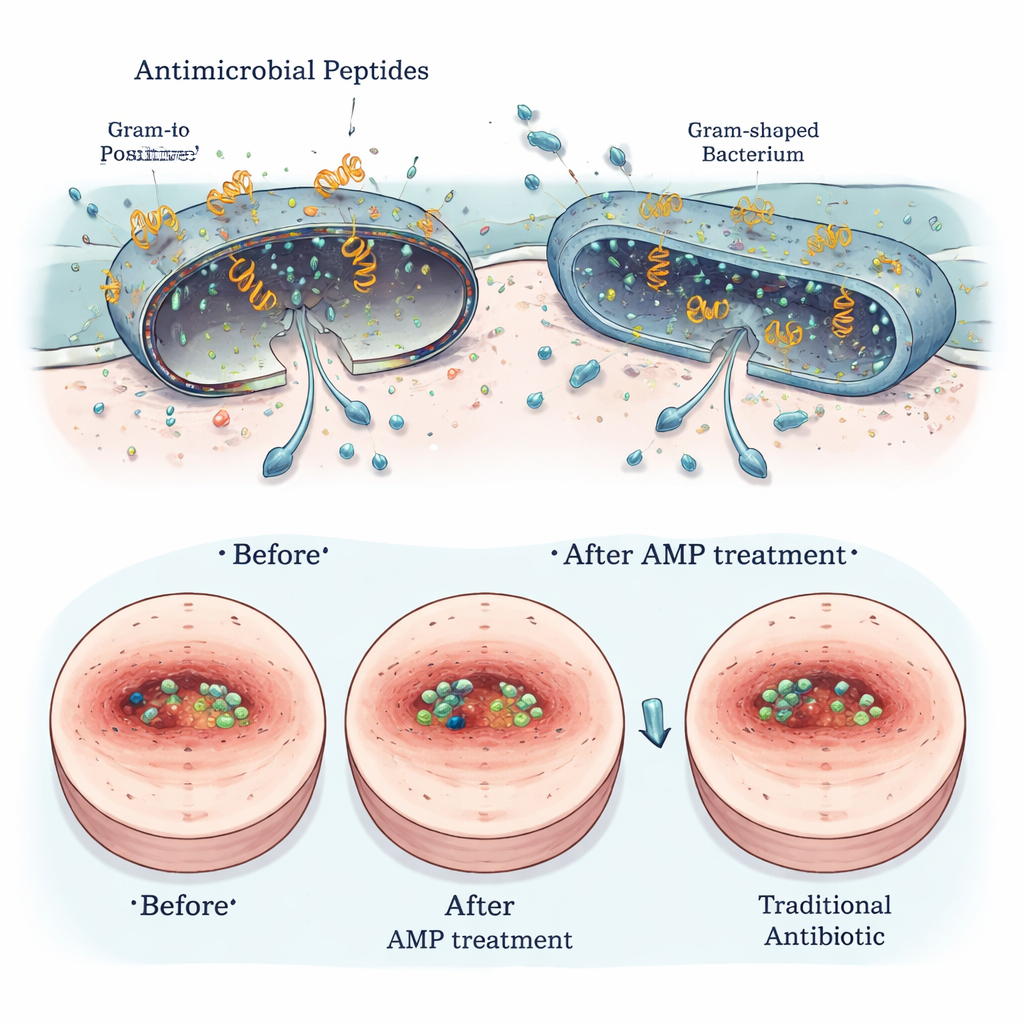
Seguros para los hospedadores, duros con los microbios—y prometedores en heridas
Varios de los péptidos de Segatella más prometedores se probaron para evaluar seguridad y utilidad en condiciones reales. En placas de laboratorio, causaron poco o ningún daño a los glóbulos rojos y solo efectos leves, si acaso, sobre células similares a las del intestino humano. La microscopía de alta resolución mostró que los péptidos alteraban físicamente las membranas externas de bacterias dañinas, mientras respetaban las células de mamíferos. En modelos de heridas infectadas en roedores, la aplicación tópica de péptidos seleccionados redujo la carga bacteriana, aceleró el cierre de la herida y disminuyó los signos de inflamación, con un rendimiento comparable al de antibióticos establecidos como la vancomicina y la polimixina B, especialmente frente a bacterias Gram-positivas como Staphylococcus aureus.
Qué significa esto para los medicamentos futuros
Para un no especialista, el mensaje es claro: los microbios intestinales de nuestros antepasados pueden contener planos para nuevos antibióticos que todavía funcionen contra las infecciones difíciles de tratar hoy. Este estudio muestra que con herramientas de IA inteligentes y eficientes como AMPLiT, los científicos pueden explotar el ADN antiguo para encontrar péptidos antimicrobianos que sean potentes y relativamente benignos para las células humanas. Aunque quedan muchos pasos antes de que cualquiera de estas moléculas se convierta en fármaco, el trabajo sugiere que revivir a socios microbianos «perdidos» como Segatella copri —o al menos tomar prestadas sus armas moleculares— podría ayudar a reponer nuestro menguante arsenal contra bacterias resistentes.
Cita: Chen, S., Yuan, Y., Wang, Y. et al. Identification of antimicrobial peptides from ancient gut microbiomes. Nat Commun 17, 1788 (2026). https://doi.org/10.1038/s41467-026-68495-0
Palabras clave: péptidos antimicrobianos, microbioma antiguo, Segatella copri, resistencia a antibióticos, minería metagenómica