Clear Sky Science · es
El bucle de retroalimentación positiva UFL1-AKT promueve la progresión del cáncer de mama al aumentar la síntesis de lípidos
Por qué a las células cancerosas les importa tanto la grasa
Las células de cáncer de mama, como todas las células de rápido crecimiento, necesitan un suministro constante de bloques de construcción para formar nuevas membranas y moléculas de señalización. Las grasas, o lípidos, son una parte clave de ese suministro. Este estudio revela cómo un sistema proteico poco conocido convierte a las células cancerosas en una «central de producción de grasa» acelerada, ayudando a los tumores a crecer y a evadir los tratamientos. Comprender esta fuente oculta de combustible podría abrir nuevas vías para frenar o «matar de hambre» a los cánceres de mama.
Una etiqueta proteica oculta con grandes consecuencias
Nuestras células ajustan constantemente el comportamiento de sus proteínas mediante pequeñas etiquetas químicas. Una de esas etiquetas, llamada UFM1, la añade una enzima denominada UFL1. La UFM1 (UFMilación) se ha relacionado con la reparación del ADN y las respuestas al estrés, pero su papel en el cáncer no estaba claro. Los autores muestran que UFL1 está mucho más activo en los tumores de mama humanos que en el tejido mamario normal, en todos los subtipos principales. Los pacientes cuyos tumores presentan niveles elevados de UFL1 tienden a tener una supervivencia peor. Cuando los investigadores redujeron UFL1 en células de cáncer de mama o en tumores de ratón, el crecimiento tumoral se ralentizó, la división celular disminuyó y la muerte celular aumentó, lo que sugiere que UFL1 actúa como un factor que favorece el cáncer.
Cómo un centro de señalización se convierte en un modo productor de grasa
Para entender cómo UFL1 ayuda a los tumores, el equipo buscó sus socios moleculares y encontró una proteína clave de control de señales llamada AKT1. AKT1 es un interruptor central que indica a las células que crezcan y que sinteticen nuevos lípidos. El estudio muestra que UFL1 se une físicamente a AKT1 y lo marca con etiquetas UFM1 en varios sitios específicos. Esta etiquetación cambia la conformación de AKT1, aflojando un «freno» interno que normalmente lo mantiene inactivo. También facilita que AKT1 se traslade a un compartimento membranoso dentro de la célula, el retículo endoplásmico, donde otras enzimas pueden activarlo completamente añadiendo grupos fosfato. Sin las etiquetas UFM1 en esos sitios, AKT1 es mucho más difícil de activar.
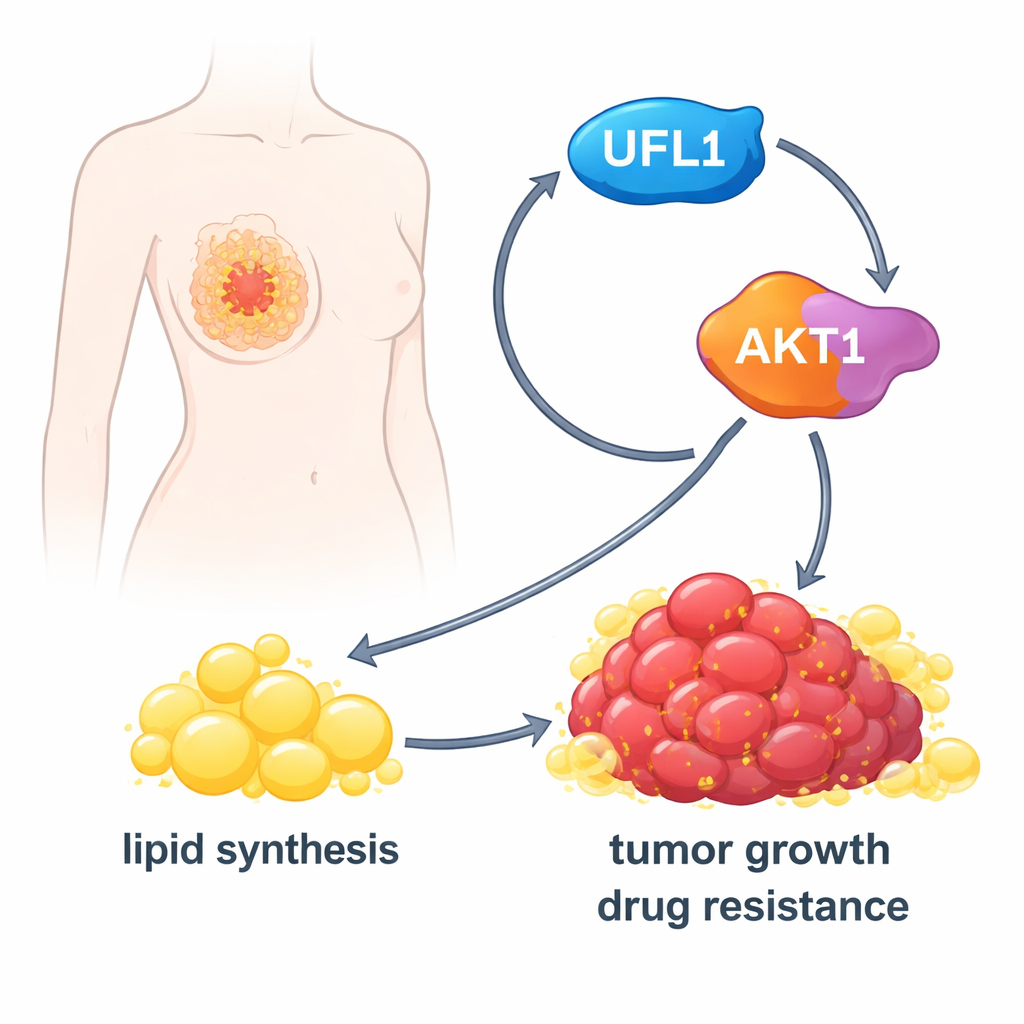
Poner en marcha la fábrica de grasa del cáncer
Una vez activado, AKT1 impulsa a las células a aumentar su producción de lípidos. Potencia la actividad de una enzima metabólica clave, ACLY, y eleva los niveles de reguladores maestros como SREBP1 que activan muchos genes de síntesis de lípidos. En células de cáncer de mama cultivadas en el laboratorio, UFL1 hizo que las células acumulasen más gotas lipídicas, ácidos grasos libres y colesterol. Eliminar UFL1 redujo drásticamente estas reservas lipídicas, tanto en cultivos como en tumores implantados en ratones. Suministrar ácidos grasos adicionales desde el exterior pudo rescatar en gran medida el crecimiento de las células cancerosas deficientes en UFL1, lo que indica que el efecto principal de UFL1 es asegurar suficientes lípidos para sostener la expansión tumoral.
Un circuito autoamplificador que impulsa el crecimiento tumoral
Sorprendentemente, la relación entre UFL1 y AKT1 es bidireccional. Los investigadores descubrieron que, una vez activo AKT1, este añade a su vez un grupo fosfato a UFL1 en un sitio concreto. Esta modificación aumenta aún más la capacidad de UFL1 para marcar AKT1 con UFM1, creando un bucle de retroalimentación positiva: UFL1 activa AKT1 y AKT1 activa UFL1. Mutar cualquiera de los sitios de UFM1 en AKT1 o el sitio de fosforilación en UFL1 rompe este bucle. En ratones, los tumores que portaban estas versiones mutantes crecieron poco, contenían menos lípidos y mostraron más células en proceso de morir. En muestras de pacientes con cáncer de mama triple negativo, niveles más altos de UFL1 activado y AKT1 activado tendían a aparecer juntos, subrayando que este bucle opera en tumores reales.
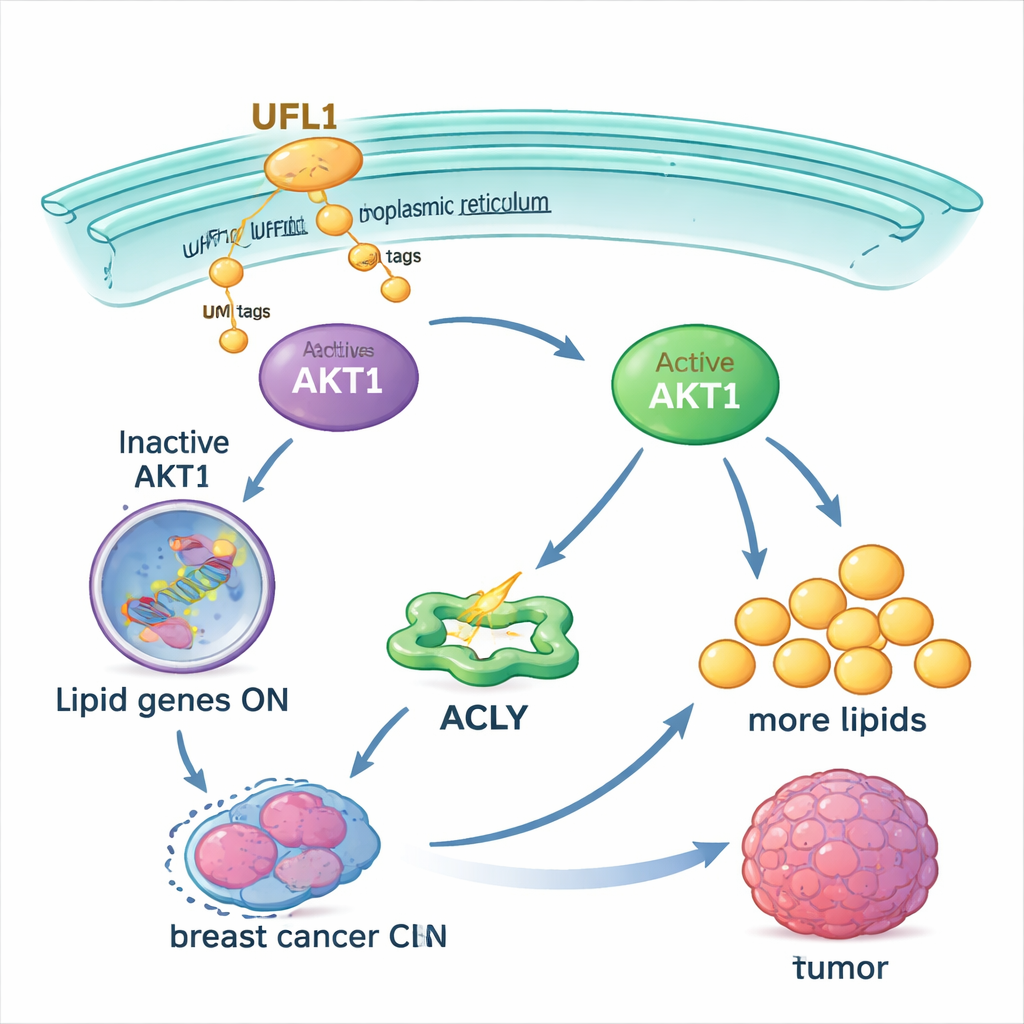
Debilitar el bucle para ayudar a que los tratamientos funcionen
Dado que muchos ensayos farmacológicos ya apuntan a AKT, los autores probaron si bloquear la UFMilación podría hacer estos tratamientos más efectivos. En células de cáncer de mama, un inhibidor de pequeña molécula de la UFMilación y un inhibidor de AKT redujeron cada uno la actividad de AKT1 y la acumulación de lípidos, pero usarlos juntos funcionó mucho mejor que cualquiera por separado. La combinación también ralentizó el crecimiento tumoral y redujo el contenido graso en tumores de ratón sin pérdida de peso apreciable en los animales. Bloquear la UFMilación además hizo que las células cancerosas fuesen más sensibles a quimioterapias estándar como cisplatino y etopósido, que a menudo fracasan cuando AKT está muy activo.
Qué significa esto para los pacientes
Para un lector no especializado, el estudio muestra que ciertos cánceres de mama se conectan mediante un bucle autorreforzante que alimenta tanto su crecimiento como su suministro de grasa. UFL1 y AKT1 actúan juntos como dos pedales apretados a la vez: uno etiqueta, el otro señala, y juntos impulsan la producción de lípidos y la expansión tumoral. Al encontrar fármacos que interfieran con este bucle—bloqueando la UFMilación, AKT1 o su interacción—las terapias futuras podrían ralentizar el crecimiento tumoral y aumentar la eficacia de los tratamientos existentes, especialmente en los tipos de cáncer de mama más agresivos.
Cita: Meng, F., Du, Y., Liang, J. et al. The UFL1-AKT positive feedback loop promotes breast cancer progression by enhancing lipid synthesis. Nat Commun 17, 614 (2026). https://doi.org/10.1038/s41467-026-68492-3
Palabras clave: cáncer de mama, metabolismo de lípidos, señalización AKT, UFMilación, terapia dirigida