Clear Sky Science · es
Hidrogel de reservorio celular autoensamblado in situ para maniobrar la radioinmunoterapia en varias etapas
Convertir la radiación en un arma contra el cáncer más inteligente
La radioterapia es uno de los tratamientos más utilizados contra el cáncer, pero los tumores a menudo sobreviven ocultándose del sistema inmunitario y proliferando en condiciones de bajo oxígeno (hipoxia) que atenúan el efecto de la radiación. Este estudio describe un hidrogel “inteligente” inyectable que se forma directamente dentro del tumor y actúa como una pequeña fábrica de fármacos y generador de oxígeno. Al suministrar tanto radiación como señales inmunoestimuladoras sincronizadas al tumor, el sistema pretende convertir un cáncer difícil de tratar en uno que las propias defensas del organismo puedan reconocer y destruir.
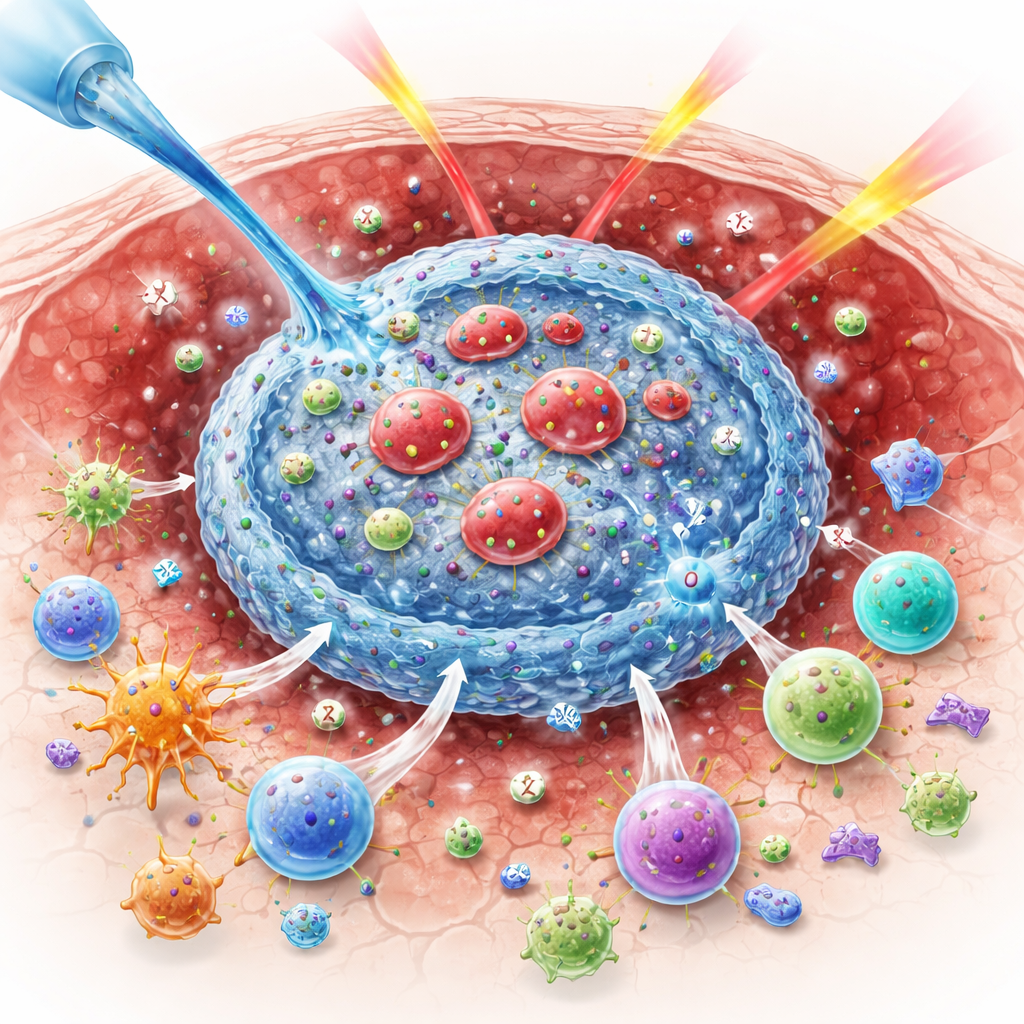
Por qué el oxígeno importa para vencer a los tumores
La radiación mata las células tumorales en parte generando moléculas de oxígeno altamente reactivas que rompen el ADN. Cuando los tumores carecen de oxígeno, esta química es menos eficaz, por lo que sobreviven más células cancerosas. Al mismo tiempo, la radiación envía señales contradictorias al sistema inmunitario. Puede exponer proteínas tumorales que señalan el cáncer como peligroso, pero también puede potenciar “frenos” de las células inmunitarias, como la proteína de control CTLA-4, y favorecer las células T regulatorias que suprimen el ataque. Estos efectos opuestos ayudan a explicar por qué combinar radiación con fármacos inmunitarios no siempre ha funcionado en pacientes tan bien como en ratones.
Un gel vivo construido dentro del tumor
Los investigadores diseñaron un material que se autoensambla solo dentro del ambiente ácido del tumor. Está compuesto por tres partes clave: un polímero natural a base de azúcares llamado alginato, un polvo inorgánico llamado peróxido de bario y glóbulos rojos que han sido suavemente modificados para portar dos fármacos inmunitarios. Cuando la mezcla se inyecta en un tumor, las condiciones ácidas hacen que el peróxido de bario se descomponga, liberando iones de bario y peróxido de hidrógeno. Los iones de bario entrecruzan instantáneamente el alginato formando un hidrogel blando, atrapando los glóbulos rojos modificados en su lugar y evitando que los fármacos se laven. Al mismo tiempo, enzimas presentes de forma natural en los glóbulos rojos convierten el peróxido de hidrógeno en oxígeno, lo que ayuda a aliviar la hipoxia tumoral y prepara el tumor para una radiación más efectiva.
Liberación programada de dos señales inmunitarias
El verdadero poder del sistema reside en cómo escalona la liberación de dos agentes inmunitarios: un anticuerpo que bloquea CTLA-4 y una citocina llamada interleucina-12 (IL-12). El anticuerpo se carga dentro de los glóbulos rojos, mientras que la IL-12 está anclada en su superficie. A medida que se genera oxígeno, se abren poros en la membrana de los glóbulos rojos, permitiendo que el anticuerpo bloqueador de CTLA-4 escape rápidamente. Esta liberación temprana elimina la supresión inmune, fomenta que las células dendríticas lleven antígenos tumorales a los ganglios linfáticos cercanos y ayuda a activar linfocitos T específicos del tumor. La IL-12, en cambio, se filtra lentamente a medida que la estructura del hidrogel se afloja gradualmente. Esta señal tardía impulsa a las células T y a las células asesinas naturales a producir interferón gamma, favorece una mayor incorporación de células inmunes citotóxicas al tumor y refuerza un bucle de retroalimentación positiva entre centinelas y efectoras inmunitarias.
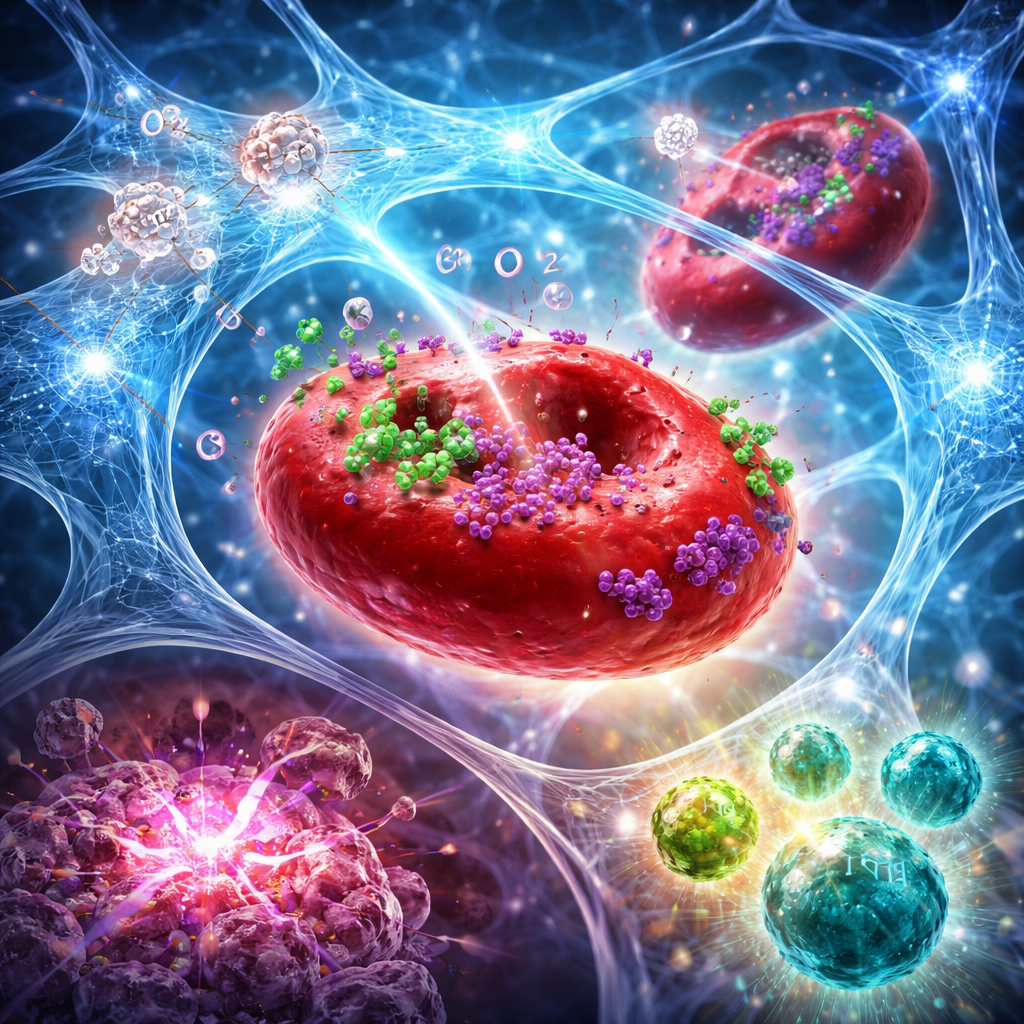
De la inyección local a un ataque inmunitario sistémico
En modelos de ratón de cánceres agresivos de mama y páncreas, combinar este hidrogel con radiación focalizada hizo más que reducir el tumor tratado. El enfoque combinado aumentó los niveles de oxígeno en los tumores durante días, amplificó el daño por radiación en el ADN e indujo una forma de muerte celular que señala de manera natural a los tumores para su reconocimiento inmunitario. Citometría de flujo y tinciones tisulares mostraron un cambio marcado en el microambiente tumoral: más células T CD8 citotóxicas y células asesinas naturales, menos células T regulatorias y una mayor proporción de células “efectoras” frente a “supresoras”. También aumentaron dendríticas especializadas en los ganglios linfáticos, lo que indica una mejor presentación de antígeno. Muchos ratones experimentaron la regresión completa del tumor, y algunos quedaron protegidos contra la reaparición tumoral cuando se reinyectaron células cancerosas semanas después, lo que sugiere la formación de memoria inmune duradera.
Seguridad, practicidad y direcciones futuras
Dado que el gel se forma localmente y retiene su carga, solo pequeñas cantidades de IL-12 y anti-CTLA-4 llegan al torrente sanguíneo, reduciendo el riesgo de efectos adversos graves como tormentas de citocinas o daño a órganos que han limitado estos agentes en el pasado. Los componentes—alginato, glóbulos rojos y peróxido de bario—son relativamente económicos y escalables, lo que genera la esperanza de que esta estrategia pueda adaptarse a distintos tipos de cáncer. Aunque quedan desafíos en manufactura, control de calidad y en la entrega del gel a tumores profundos o ampliamente diseminados, el trabajo demuestra una vía prometedora para sincronizar la radiación con una activación inmune precisamente cronometrada, convirtiendo un tratamiento físico del cáncer en un detonante potente de la inmunidad antitumoral sistémica.
Qué podría significar esto para los pacientes
En términos cotidianos, esta investigación sugiere que, en lugar de administrar radiación y fármacos inmunitarios por separado con la esperanza de que cooperen, podemos empaquetarlos en un material inteligente que se sitúe dentro del tumor, genere su propio oxígeno y libere señales inmunitarias en una secuencia cuidadosamente coreografiada. En animales, este enfoque no solo hizo la radiación más letal para las células cancerosas, sino que también adiestró al sistema inmunitario para reconocer y recordar el tumor, ayudando a prevenir su recurrencia. Si se logran resultados similares en humanos, dichos hidrogeles podrían, algún día, convertir tumores difíciles de tratar en objetivos que las defensas del propio organismo puedan encontrar y destruir con fiabilidad.
Cita: Chen, Y., Chen, Q., Ma, Y. et al. In situ self-assembled cell reservoir hydrogel for maneuvering multistage radioimmunotherapy. Nat Commun 17, 1784 (2026). https://doi.org/10.1038/s41467-026-68490-5
Palabras clave: radioinmunoterapia, hidrogel, inmunoterapia contra el cáncer, microambiente tumoral, radioterapia