Clear Sky Science · es
Multiestabilidad continuamente sintonizable en redes de replicación de ADN
De interruptores simples a muchos estados posibles
Los sistemas biológicos, desde células en división hasta embriones en desarrollo, rara vez funcionan como interruptores de luz simples que solo están encendidos o apagados. En su lugar, a menudo mantienen muchos estados duraderos, como un regulador de intensidad que puede detenerse en innumerables posiciones. Este artículo presenta una red química basada en ADN que se comporta más como ese regulador: puede mantener de forma estable no solo unos pocos estados distintos, sino esencialmente cualquier composición a lo largo de un espectro continuo. Esa capacidad podría convertirse en una base poderosa para materiales inteligentes futuros, memorias moleculares y ordenadores bioquímicos que procesen información analógica, no solo digital.
Por qué importan múltiples estados estables
Muchas decisiones celulares —si una célula madre madura, si una célula se autodestruye o si una red génica recuerda una señal pasada— dependen de la “multiestabilidad”, la capacidad de descansar en más de un patrón estable de actividad bajo las mismas condiciones. Las versiones sintéticas tradicionales de estos sistemas se han construido a partir de circuitos génicos, enzimas o hebras de ADN que se activan o desactivan entre sí. Estos diseños suelen producir un puñado de resultados discretos, como los conmutadores bistables clásicos con dos estados duraderos. Escalar esa idea es difícil: un sistema de N estados puede requerir del orden de N×(N−1) enlaces inhibidores cuidadosamente ajustados, y aun así el sistema solo salta entre un pequeño conjunto de puntos fijos en lugar de ofrecer un continuo suave de posibilidades.
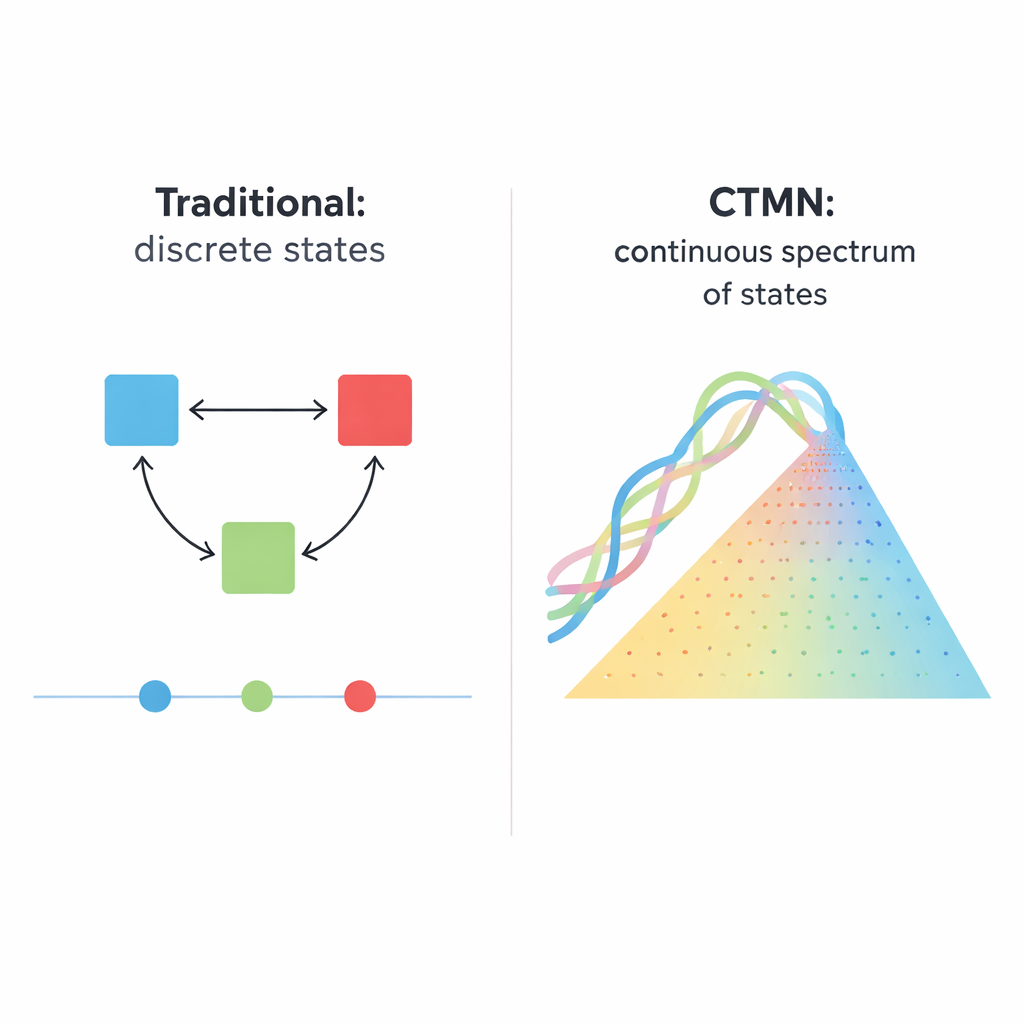
Un nuevo tipo de red de ADN: continuamente sintonizable
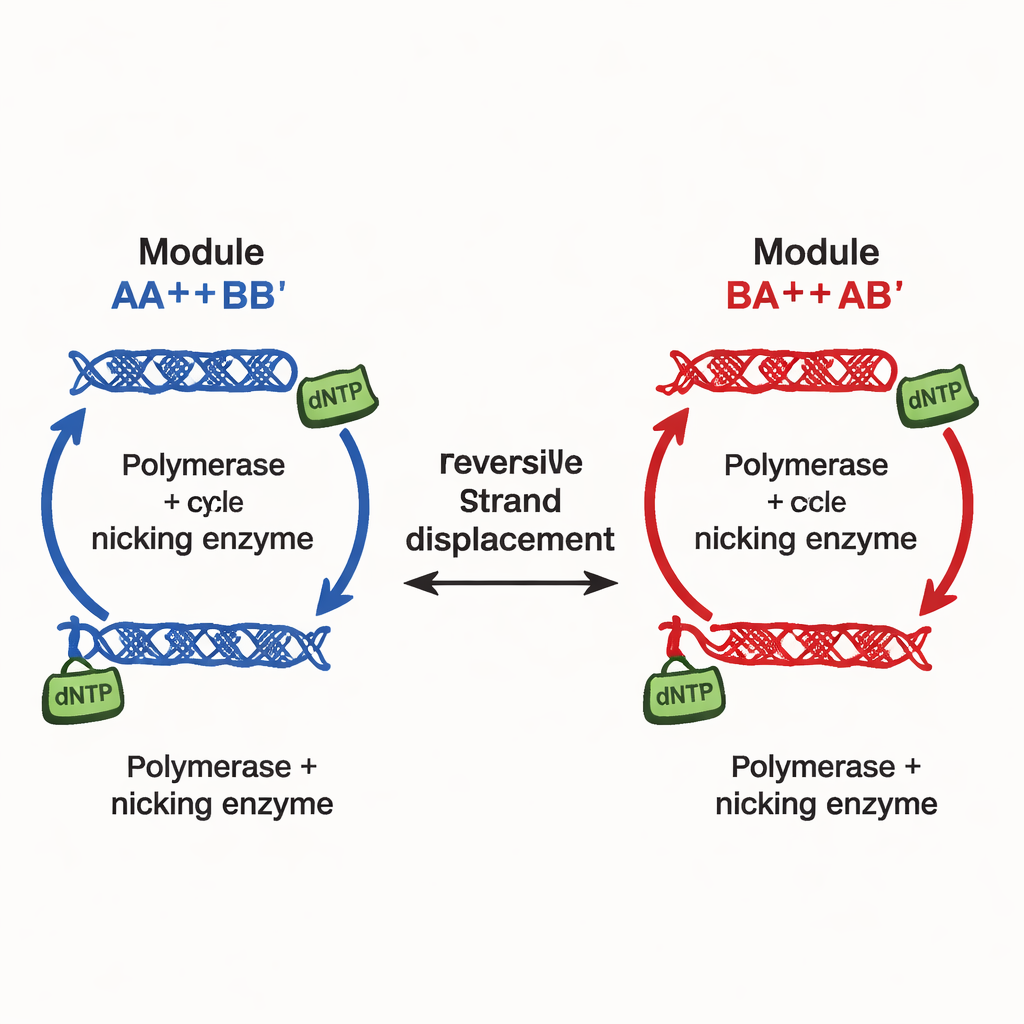
Los autores introducen un principio de diseño diferente, implementado en lo que denominan redes de multiestabilidad continuamente sintonizable (CTMNs, por sus siglas en inglés). En lugar de depender de muchas señales inhibidoras separadas, usan competencia directa entre módulos de replicación de ADN unidos por reacciones reversibles de intercambio de hebras. Cada módulo está formado por dímeros de ADN diseñados que pueden participar tanto en desplazamiento de hebras como servir de plantilla para la ADN polimerasa, asistida por una enzima nickasa que corta y regenera segmentos clave. El combustible químico —los nucleótidos dNTP— impulsa la polimerización y el nicking continuos, manteniendo el sistema lejos del equilibrio. En estas condiciones, los módulos en competencia se “congelan” efectivamente en las proporciones relativas con las que comenzaron, produciendo no solo dos o tres resultados sino toda una línea continua (o, para más módulos, un plano) de estados duraderos.
Cómo la maquinaria molecular fija la memoria
En su red más simple de dos módulos, CTMN‑1, el equipo demuestra experimentalmente y mediante un modelado cinético detallado que el sistema puede asentarse en una familia de mezclas estables que abarcan casi todo el rango desde “principalmente módulo A” hasta “principalmente módulo B”. La polimerización convierte los dímeros activos en formas extendidas que quedan temporalmente fuera de la competencia por intercambio de hebras; el nicking los restaura luego, cerrando un bucle autorregulador. Cuando ambos módulos comparten este bucle, suprimen la interconversión mutua tan fuertemente que el sistema permanece bloqueado cerca de su composición inicial durante muchas horas, siempre que haya combustible disponible. El análisis de estabilidad lineal de las ecuaciones subyacentes revela toda una variedad —efectivamente un continuo— de estados estacionarios, en contraste con el único punto fijo observado cuando se eliminan las enzimas o el combustible.
Respuestas programables y memoria molecular
Puesto que el estado de la red se almacena en composiciones de ADN, puede dirigirse y leerse de formas programables. Los autores diseñan cortos “disparadores” de ARN que se unen temporalmente a hebras de ADN específicas, sesgando la competencia y desplazando la red hacia una nueva composición. Incluso después de que el ARN es degradado por una enzima, el nuevo estado persiste, funcionando como una forma de memoria molecular. Estímulos repetidos o más fuertes empujan el sistema suavemente a lo largo del continuo de estados en lugar de hacerlo alternar entre posiciones simples de encendido/apagado. Además, los propios productos de la replicación de ADN pueden personalizarse para actuar como señales para procesos aguas abajo: en demostraciones, diferentes estados de CTMN‑1 activan selectivamente uno de dos catalizadores basados en ADN o sesgan la transcripción de ARN hacia una u otra hebra mensajera, sin alterar la multiestabilidad subyacente.
Escalando hacia “reguladores” moleculares complejos
Para mostrar que esta estrategia es escalable, los investigadores construyen una red de tres módulos, CTMN‑2, añadiendo más dímeros de ADN diseñados que comparten un dominio de intercambio común pero codifican diferentes plantillas de replicación. Ahora los estados estacionarios posibles llenan una región bidimensional, como puntos sobre un diagrama de fases triangular, en lugar de a lo largo de una línea simple. Nuevamente, los experimentos confirman que muchas composiciones distintas son estables siempre que haya combustible y enzimas presentes, y que todas colapsan a un único punto de equilibrio cuando se elimina el suministro de energía. Dado que añadir nuevos módulos requiere solo nuevos constructos de ADN que se enchufan en el mismo marco de desplazamiento, el cableado global no se dispara en complejidad como ocurre en los diseños tradicionales.
Qué significa esto para futuras tecnologías moleculares
Para un no especialista, el mensaje principal es que los autores han convertido una red de replicación de ADN en un dispositivo de memoria analógica altamente flexible. En lugar de escoger entre unas pocas opciones predefinidas, su sistema puede mantener de forma fiable una de docenas de estados experimentalmente distinguibles, cada uno definido por la cantidad relativa de cada módulo de ADN presente, y puede convertir pulsos químicos transitorios en desplazamientos duraderos a lo largo de este continuo. Dado que las hebras de salida de ADN son programables y están desacopladas del mecanismo estabilizador, el mismo marco podría, en principio, regular una amplia gama de reacciones bioquímicas o propiedades materiales aguas abajo con un control fino y graduado. Este trabajo señala, por tanto, hacia dispositivos moleculares que calculan, recuerdan y se adaptan más como sistemas analógicos neuronales o mecánicos que como simples interruptores digitales.
Cita: Zhong, R., Fu, Y., Jiang, S. et al. Continuously tunable multistability in DNA replication networks. Nat Commun 17, 1782 (2026). https://doi.org/10.1038/s41467-026-68488-z
Palabras clave: Multiestabilidad de ADN, memoria molecular, redes bioquímicas sintéticas, desplazamiento de hebras de ADN, computación molecular analógica