Clear Sky Science · es
Predicción robusta e interpretable de marcadores génicos y tipos celulares a partir de datos de transcriptómica espacial
Convertir portaobjetos rutinarios en mapas moleculares
Cuando se toma una biopsia, los médicos normalmente ven solo lo que revela el microscopio: las formas y los patrones de las células en tinciones rosas y púrpuras. Sin embargo, bajo esos colores existe un mundo oculto de genes que se activan o desactivan y que influyen en cómo crece un cáncer y cómo responde al tratamiento. Este estudio presenta STimage, un nuevo sistema de inteligencia artificial (IA) que pretende leer ese guion molecular directamente a partir de imágenes patológicas estándar, ofreciendo potencialmente información más rápida y barata sin pruebas de laboratorio adicionales.
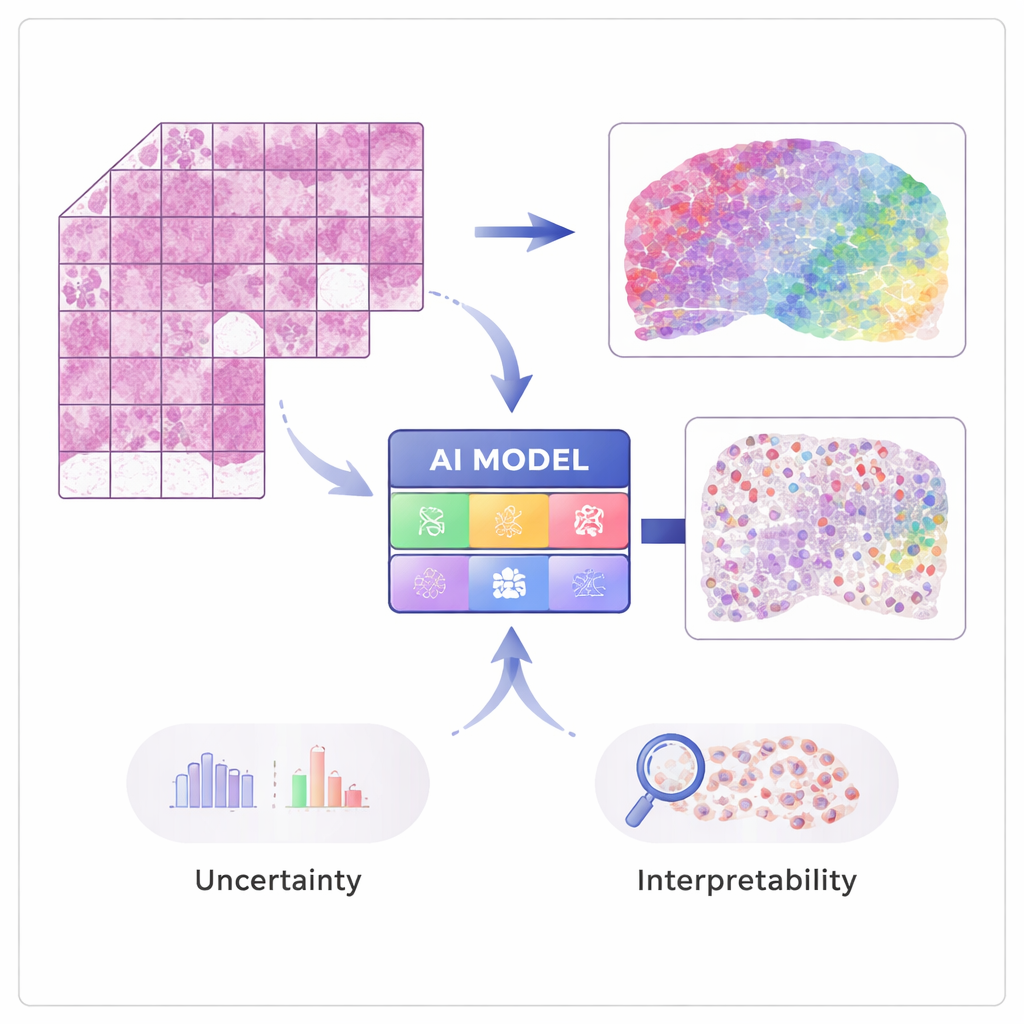
De las imágenes a la actividad génica
Las técnicas modernas de “transcriptómica espacial” pueden medir la actividad de decenas de miles de genes conservando además la localización de cada señal en el tejido. Estos métodos son potentes pero costosos y aún no son de uso rutinario en hospitales. STimage se entrena con un número modesto de esos conjuntos de datos espaciales, en los que cada imagen de tejido se empareja con mediciones génicas detalladas en muchos puntos pequeños. La IA aprende a asociar patrones visuales locales en la tinción de hematoxilina y eosina (H&E)—por ejemplo, la densidad o la irregularidad de los núcleos—con la actividad génica subyacente, de modo que después puede predecir la expresión génica y los tipos celulares a partir de imágenes ordinarias por sí sola.
Construyendo un patólogo IA más confiable
Un objetivo clave del trabajo no es solo la precisión, sino la fiabilidad y la explicabilidad. En lugar de devolver un solo número por cada gen, STimage predice una distribución de probabilidad completa, describiendo un rango probable de actividad génica en cada ubicación. También separa dos tipos de incertidumbre: una debida a datos ruidosos o variables y otra que refleja la propia falta de conocimiento del modelo. Al entrenar muchas versiones ligeramente diferentes del modelo y promediarlas—un enfoque de “conjunto” (ensemble)—los investigadores mejoran tanto el rendimiento como la claridad sobre dónde el sistema está seguro y dónde no lo está, lo cual es crucial para la toma de decisiones clínicas.
Pruebas en distintos cánceres, tecnologías y hospitales
El equipo evaluó STimage en conjuntos de datos diversos de cánceres de mama, piel y riñón, así como en una enfermedad hepática de origen inmunológico. Aprendió a predecir marcadores importantes del cáncer y del sistema inmunitario, con frecuencia reproduciendo los patrones espaciales reales observados en experimentos independientes. El modelo se mantuvo robusto cuando fue desafiado con datos de diferentes laboratorios, métodos de preparación de muestras e incluso tecnologías subyacentes distintas, incluidas plataformas con resolución de célula única y sistemas antiguos de menor resolución. En comparaciones directas con varias herramientas de IA existentes, STimage y sus variantes en conjunto generalmente obtuvieron mejores resultados, especialmente al evaluar qué tan bien las patrones predichos coincidían con la distribución real de la actividad génica en el tejido.
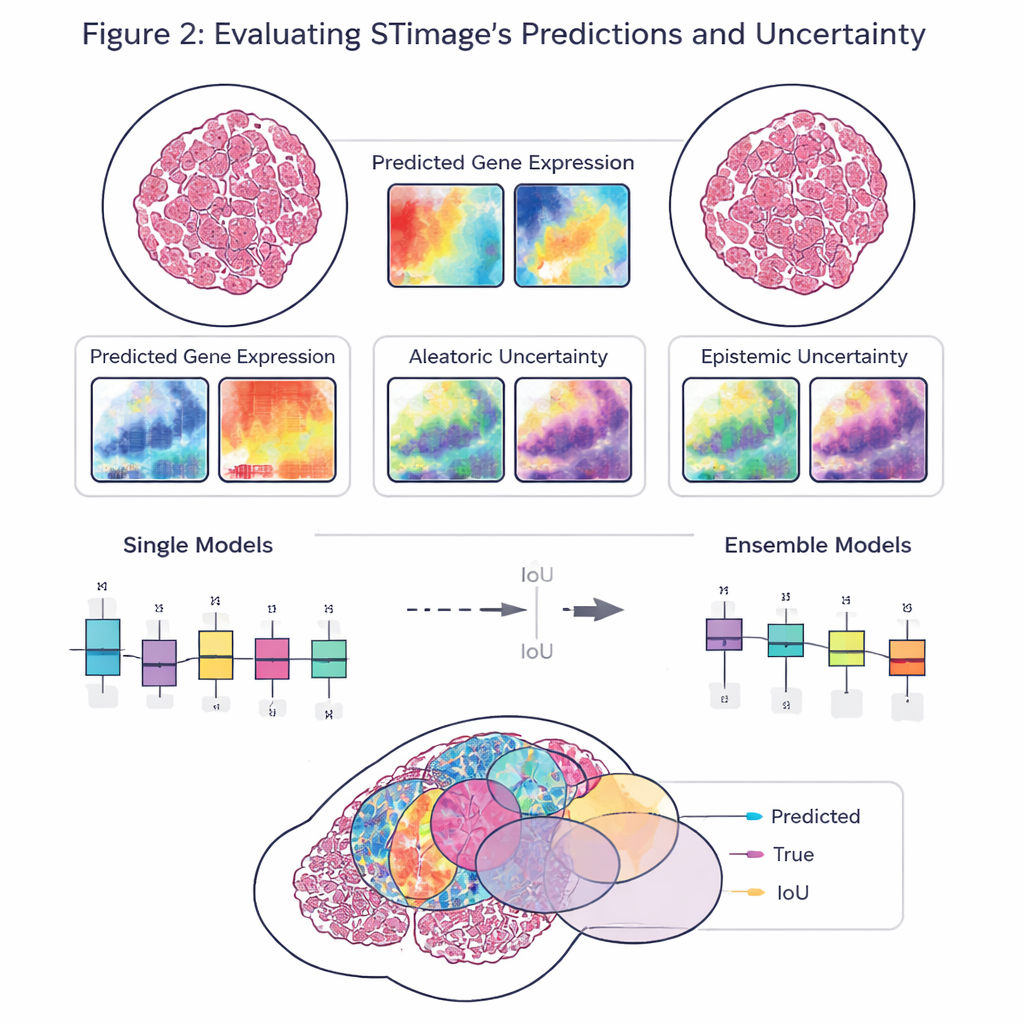
Ver dentro de los tumores: células, supervivencia y respuesta a fármacos
STimage va más allá de la predicción génica para inferir qué tipos celulares ocupan cada región, usando conjuntos de datos de alta resolución donde se conoce la identidad de cada célula. El modelo pudo distinguir células tumorales de células inmunitarias y de soporte y cartografiar su disposición a lo largo del portaobjetos. Los autores aplicaron luego STimage a grandes colecciones de imágenes rutinarias de cáncer del proyecto The Cancer Genome Atlas. Incluso sin mediciones espaciales, los perfiles génicos predichos por la IA se alinearon estrechamente con los datos génicos agregados reales. Estas predicciones fueron lo suficientemente sólidas como para agrupar a los pacientes en categorías de mayor y menor riesgo y para ayudar a distinguir a quienes tenían más probabilidad de responder de forma completa a ciertas terapias para el cáncer de mama.
Por qué esto importa para los pacientes del futuro
Para pacientes y clínicos, la promesa de STimage es una especie de “sobrecapa molecular” sobre el portaobjetos de patología familiar. En lugar de solicitar múltiples pruebas costosas, una única imagen escaneada podría algún día revelar dónde están activos los programas génicos agresivos, cómo se distribuyen las células inmunitarias y qué marcadores señalan mejores o peores resultados o diferentes respuestas a fármacos. Si bien el método aún se está refinando y la correlación con mediciones reales no es perfecta, su capacidad para capturar patrones espaciales, estimar su propia incertidumbre y resaltar qué células impulsan sus predicciones lo convierte en un paso práctico hacia una patología digital más informativa y transparente.
Cita: Tan, X., Mulay, O., Xie, J. et al. Robust and interpretable prediction of gene markers and cell types from spatial transcriptomics data. Nat Commun 17, 1781 (2026). https://doi.org/10.1038/s41467-026-68487-0
Palabras clave: patología digital, transcriptómica espacial, biomarcadores del cáncer, aprendizaje profundo, microambiente tumoral