Clear Sky Science · es
PTRAMP, CSS y Ripr forman un complejo conservado necesario para la invasión de merozoítos de especies de Plasmodium en eritrocitos
Por qué esto importa para combatir la malaria
Los parásitos de la malaria deben introducirse en nuestros glóbulos rojos para causar enfermedad. Este estudio descubre un pequeño conjunto de proteínas que forman un “puente de abordaje” compartido utilizado por varias especies importantes de malaria, incluidas las que infectan a los humanos. Al revelar cómo se construye este puente y cómo los anticuerpos pueden, en ocasiones, bloquearlo, el trabajo apunta a nuevas vías para diseñar vacunas que podrían proteger frente a más de un tipo de malaria a la vez. 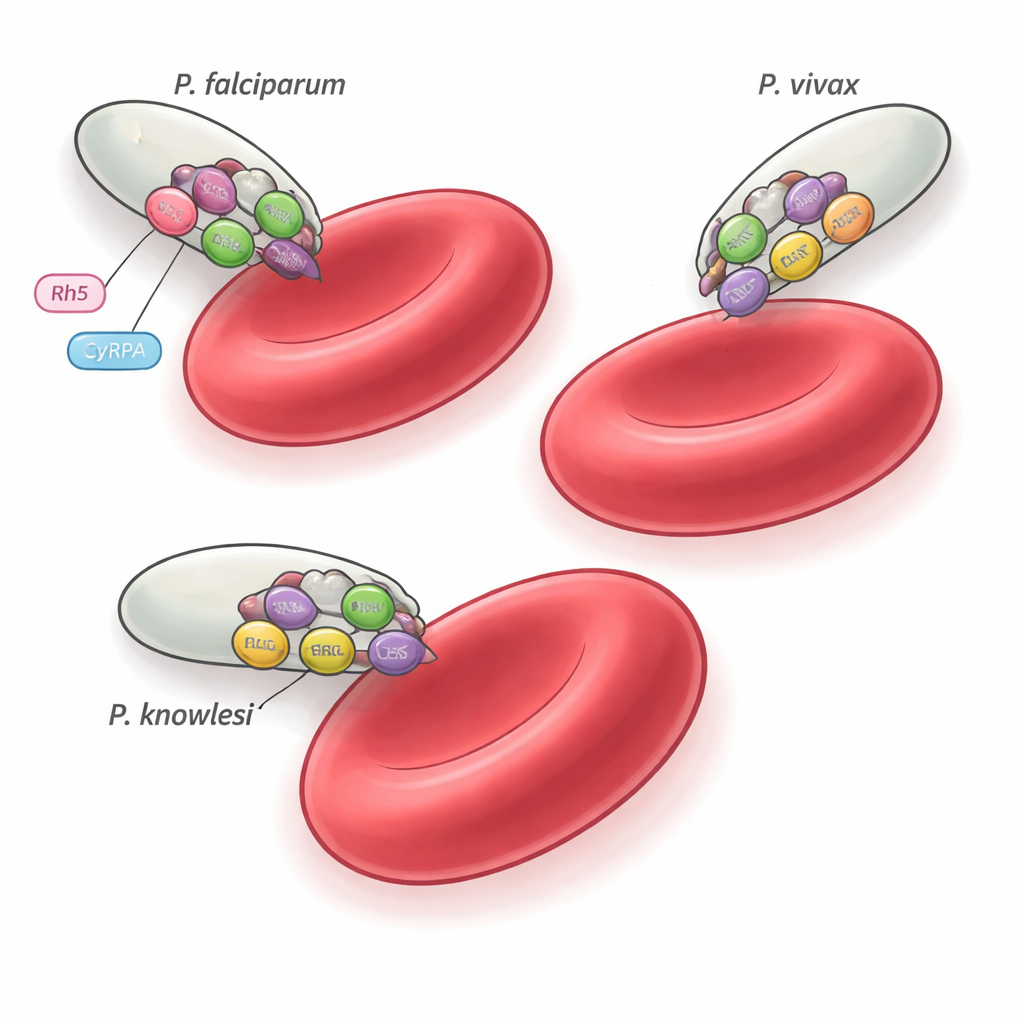
Un conjunto común en muchos parásitos de la malaria
Hay más de 200 especies de Plasmodium, pero solo unas pocas, como P. falciparum, P. vivax y P. knowlesi, infectan a los humanos. Estas especies ocupan ramas distintas del árbol genealógico del parásito y prefieren diferentes tipos de glóbulos rojos, pero todas deben invadir los eritrocitos con una precisión extraordinaria. Trabajos previos en P. falciparum identificaron un ensamblaje de cinco partes, el complejo PCRCR, que es esencial para la invasión y se aferra a un receptor eritrocitario humano llamado basigin. Una pieza de ese complejo, una proteína llamada Rh5, es única de P. falciparum y sus parientes cercanos, lo que plantea un enigma: ¿qué usan las demás especies de malaria en su lugar? El estudio actual se centra en tres proteínas compañeras —PTRAMP, CSS y Ripr— que están conservadas a lo largo del género y prueba si forman una máquina de invasión universal.
Construyendo un puente de invasión de tres partes
Mediante búsquedas de secuencias en numerosos genomas de parásitos, los autores muestran que PTRAMP, CSS y Ripr están presentes en todas las principales líneas de Plasmodium, a diferencia de Rh5, que se restringe a un subgrupo. La predicción estructural con AlphaFold, combinada con mediciones bioquímicas detalladas, revela que PTRAMP y CSS se unen para formar un par estable, mantenido por un puente disulfuro específico entre dos cisteínas conservadas. Esta plataforma de dos proteínas luego sujeta el extremo terminal de Ripr, creando un complejo de tres partes PTRAMP–CSS–Ripr (PCR). Experimentos con proteínas de P. falciparum, P. vivax y P. knowlesi muestran que este complejo se forma en las tres especies con alta afinidad, y que solo una pequeña región en el extremo C-terminal de Ripr es necesaria para la unión fuerte. 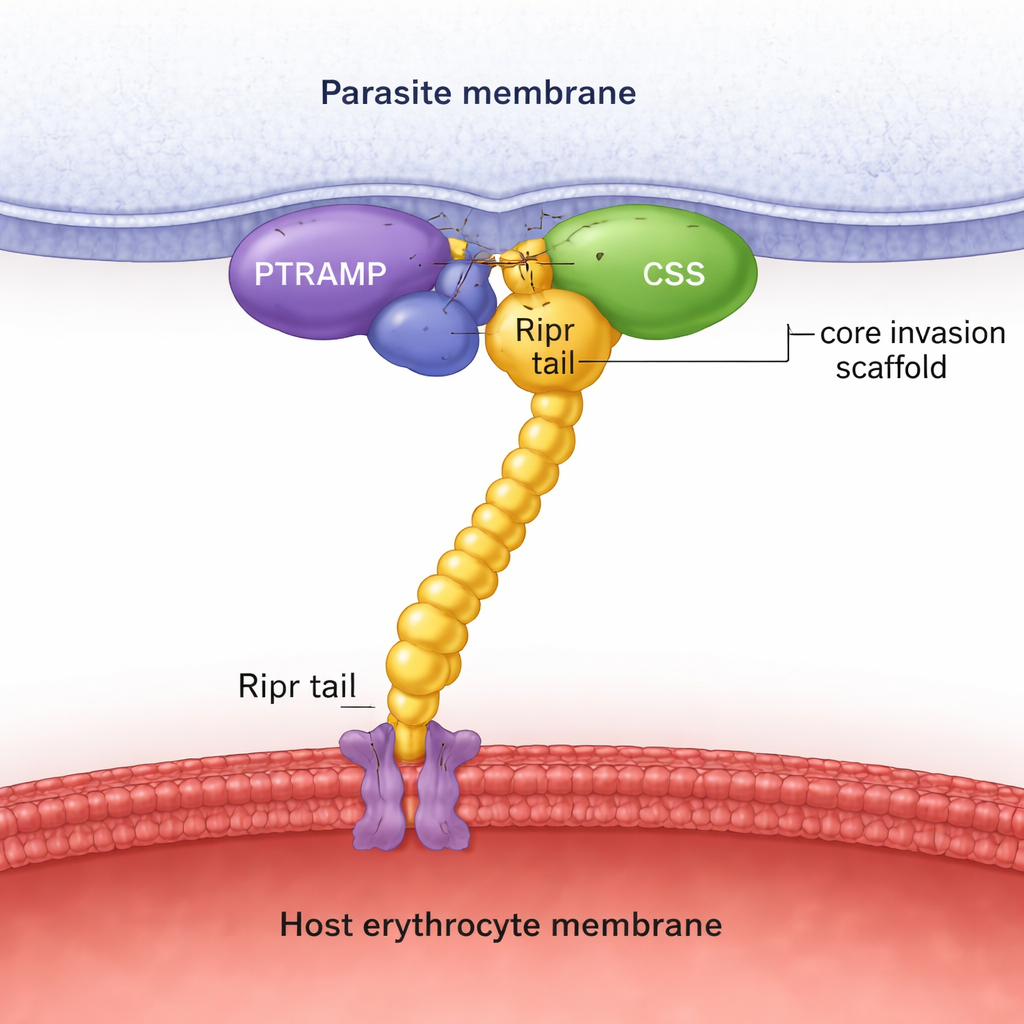
Ver la estructura con detalle atómico
Para ir más allá de las predicciones, el equipo resolvió estructuras cristalinas y recopiló imágenes por criomicroscopía electrónica. La estructura cristalina del par PTRAMP–CSS de P. vivax muestra exactamente cómo un tramo corto de PTRAMP se entrelaza a lo largo de CSS y forma el enlace disulfuro clave. Otra estructura captura un anticuerpo potente unido a dos dominios tipo factor de crecimiento de Ripr, mapeando un epítopo inhibidor en la cola de Ripr. El análisis por cryo‑EM del complejo PCR de P. knowlesi confirma la forma general predicha por AlphaFold: PTRAMP y CSS se sitúan cerca de la membrana del parásito y sujetan a Ripr, cuyo cuerpo alargado se extiende hacia la célula huésped. En conjunto, estas instantáneas estructurales respaldan la idea de que el trío PCR forma un andamiaje rígido que físicamente abarca la distancia entre el parásito y el glóbulo rojo durante la invasión.
Anticuerpos que reconocen más de una especie
Dado que estas proteínas están conservadas, los autores preguntaron si las infecciones humanas generan de forma natural anticuerpos que reaccionan entre especies. El plasma de pacientes infectados con P. falciparum, P. vivax o P. knowlesi mostró respuestas de anticuerpos fuertes frente a CSS y Ripr de múltiples especies, lo que sugiere que las personas desarrollan anticuerpos contra regiones compartidas del complejo PCR. El equipo produjo entonces anticuerpos monoclonales y nanocuerpos dirigidos contra PTRAMP, CSS y Ripr de P. vivax, y probó si estos podían bloquear el crecimiento del parásito en cultivo. Algunos anticuerpos, en especial uno llamado 5B3 que se une a la cola de Ripr, fueron capaces de inhibir la invasión por P. knowlesi y, a concentraciones mayores, por P. falciparum. Sorprendentemente, los mismos anticuerpos no detuvieron a P. vivax ni al parásito de monos estrechamente relacionado P. cynomolgi, aunque sí podían unirse a las proteínas de esas especies.
Un andamiaje compartido con añadidos específicos por especie
Las pruebas funcionales muestran que el complejo PCR en sí no se adhiere directamente a los glóbulos rojos; en cambio, probablemente actúa como un andamiaje estructural conservado al que cada especie acopla sus propios socios de unión a receptores. En P. falciparum, por ejemplo, el trío PCR se asocia con CyRPA y Rh5 para captar basigin en los eritrocitos humanos. En P. vivax y P. knowlesi, las proteínas equivalentes de unión a receptores y los objetivos en el huésped siguen siendo desconocidos, pero el mismo núcleo PTRAMP–CSS–Ripr parece organizar la maquinaria de invasión. El hecho de que algunos anticuerpos puedan reaccionar entre especies pero solo inhibir determinadas especies subraya cómo pequeñas diferencias en el ensamblaje y el momento del complejo pueden cambiar la vulnerabilidad al ataque inmune.
Qué significa esto para futuras vacunas contra la malaria
Para un público no especializado, la conclusión es que los parásitos de la malaria, pese a ser muy diferentes entre sí, comparten un “conector” común que usan para entrar en los glóbulos rojos —formado por las proteínas PTRAMP, CSS y Ripr— aunque lo conecten a distintos receptores en la superficie celular. Este conector conservado está ahora mapeado estructuralmente y, en algunos casos, puede ser atacado por anticuerpos que actúan entre especies. Aunque es necesario más trabajo para identificar el conjunto completo de proteínas asociadas y mejorar los anticuerpos inhibidores, el descubrimiento de un andamiaje de invasión universal abre la puerta a diseños de vacuna que podrían proteger contra varios tipos de malaria en lugar de uno solo.
Cita: Seager, B.A., Lim, P.S., Xiao, X. et al. PTRAMP, CSS and Ripr form a conserved complex required for merozoite invasion of Plasmodium species into erythrocytes. Nat Commun 17, 1780 (2026). https://doi.org/10.1038/s41467-026-68486-1
Palabras clave: invasión de la malaria, proteínas de Plasmodium, entrada de merozoítos, vacuna transespecífica, infección eritrocitaria