Clear Sky Science · es
Tomografía crioelectrónica revela replicación, gemación y maduración acopladas en flavivirus
Cómo los virus que infectan el cerebro secuestran las membranas celulares
Los flavivirus, un gran grupo de virus que incluye a los agentes responsables del dengue y de la encefalitis transmitida por garrapatas, pueden invadir el cerebro y causar enfermedades graves. Sin embargo, cómo estos diminutos patógenos se copian y ensamblan nuevas partículas virales dentro de nuestras células ha permanecido en gran medida oculto. Este estudio emplea imágenes electrónicas 3D de vanguardia a temperaturas criogénicas para observar flavivirus transmitidos por garrapatas en acción dentro de células humanas y tejido cerebral de ratón, revelando un acoplamiento inesperadamente estrecho entre la copia del genoma, el ensamblaje viral y la maduración del virus.
Fábricas virales ocultas en las membranas celulares
Los flavivirus no se limitan a flotar en la célula mientras se replican. En su lugar, remodelan un sistema de membranas celulares llamado retículo endoplásmico (RE) para formar bolsillos especializados conocidos como orgánulos de replicación. Estos se parecen a pequeñas y hacia dentro yemas en la superficie del RE y sirven como cámaras protegidas donde se copia el ARN viral. Mediante tomografía crioelectrónica, una técnica que produce instantáneas 3D de células congeladas rápidamente en un estado casi nativo, los investigadores visualizaron estos brotes en células pulmonares humanas infectadas con un flavivirus transmitido por garrapatas relacionado con el virus de la encefalitis transmitida por garrapatas. Encontraron que el RE alrededor de las regiones infectadas se hincha y se llena de racimos de estos orgánulos de replicación, algunos vacíos y otros llenos de ARN denso y filamentoso.
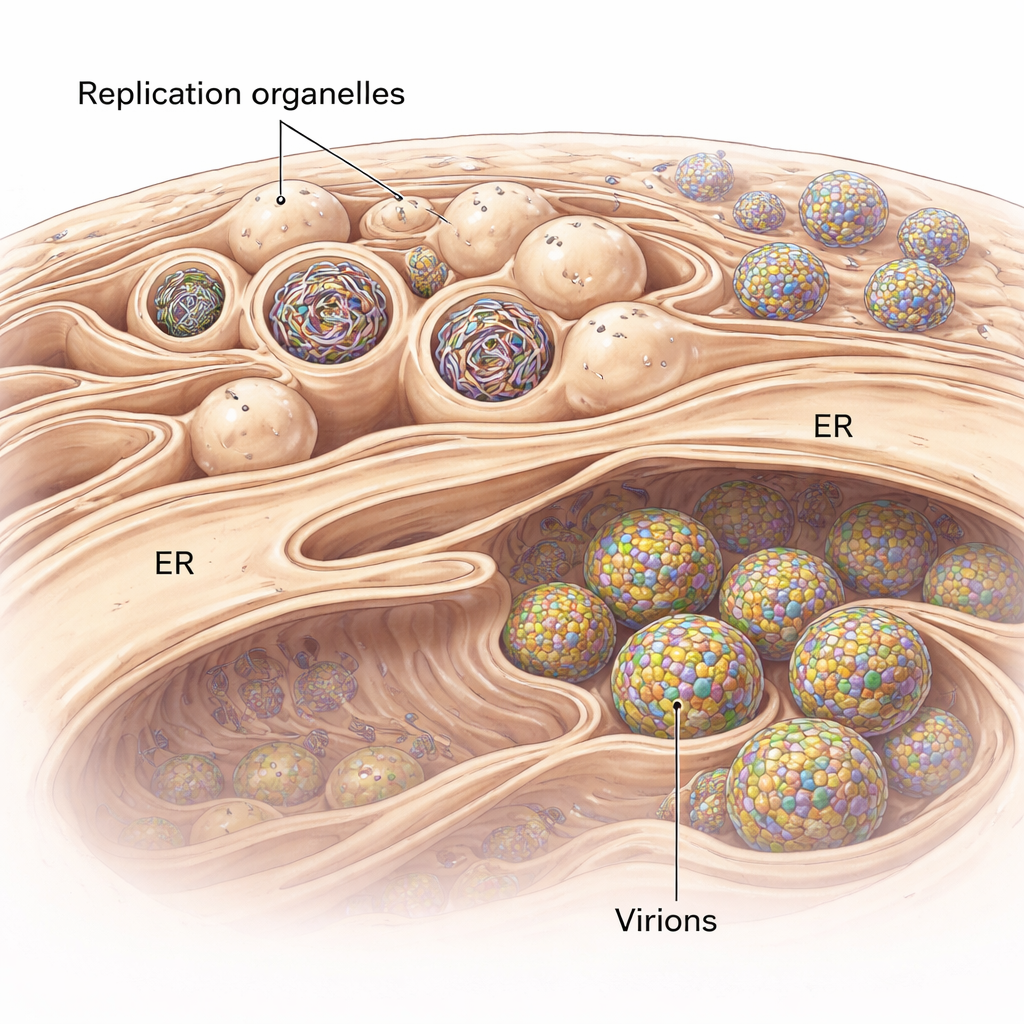
Construyendo la burbuja viral perfecta
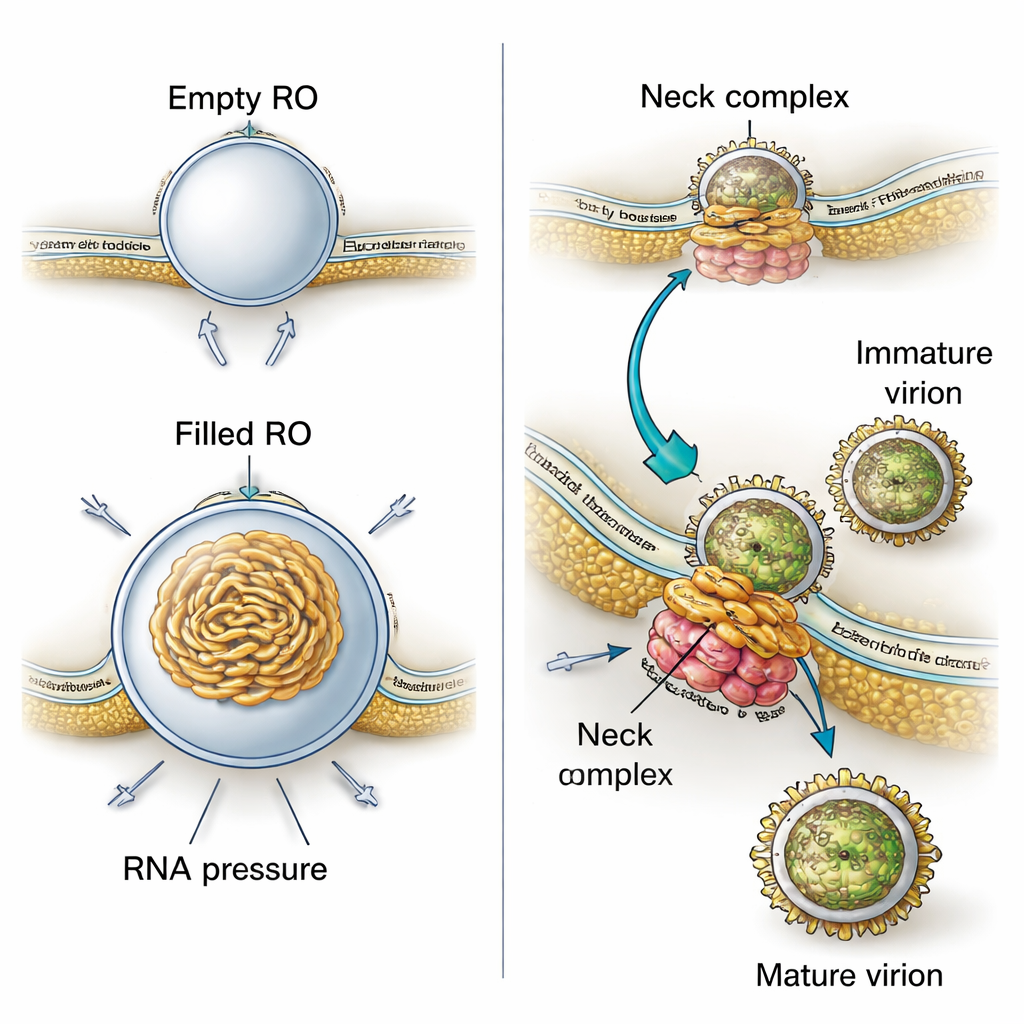
¿Por qué estos bolsillos de membrana tienen una forma tan precisa, parecida a una yema? Al combinar sus imágenes 3D con modelado físico, los autores muestran que actúan dos fuerzas de forma conjunta. Primero, la membrana de los orgánulos de replicación es sistemáticamente más gruesa que el RE normal, lo que sugiere que proteínas virales o lípidos alterados rigidizan y curvan la membrana hacia una yema estable incluso antes de que entre ARN. Segundo, cuando el ARN viral está presente, se enrosca dentro del bolsillo y empuja hacia afuera, aumentando el tamaño de la yema. Cálculos basados en los tamaños medidos indican que cada orgánulo lleno contiene probablemente presión equivalente a aproximadamente una copia del genoma viral en forma de doble cadena. Esto significa que el virus utiliza tanto una membrana preformada como el empuje físico de su propio material genético para construir y estabilizar sus minifábricas.
Línea de ensamblaje: de la copia del genoma a los virus nuevos
El estudio también desvela cuán estrechamente está vinculada la producción viral a estos sitios de replicación. En sus vistas 3D, los investigadores observaron con frecuencia nuevas partículas virales formándose justo al lado de los orgánulos de replicación, gemando hacia espacios cercanos de aspecto similar al RE. Las partículas inmaduras tenían una superficie espinosa, mientras que las más maduras aparecían lisas. Las medidas en los tomogramas mostraron que las partículas inmaduras se sitúan más cerca de los orgánulos de replicación que las maduras, lo que implica que, al desplazarse solo una corta distancia a través de compartimentos membranosos entrelazados, las partículas sufren los cambios estructurales necesarios para volverse infecciosas. Un gran ensamblaje proteico en el estrecho “cuello” donde cada yema de replicación se conecta con el citoplasma parece anclar el orgánulo de replicación a una membrana vecina donde ocurre la gemación. Este complejo probablemente actúa como una cremallera molecular que coordina la producción de ARN con el empaquetamiento de ese ARN en nuevas partículas virales.
Afinando la maduración con un solo aminoácido
Para investigar cómo se controla la maduración viral, el equipo comparó dos versiones de un virus quimérico que difieren en un solo aminoácido en un sitio reconocido por una enzima hospedadora llamada furina. Esta enzima corta una proteína de superficie viral, ayudando a transformar partículas inmaduras y espinosas en maduras y lisas. En ensayos de corte in vitro y en células infectadas, la variante con arginina en esta posición fue cortada más rápidamente que la variante con glutamina. Cuando se visualizaron en células mediante tomografía crioelectrónica, el virus de corte más rápido produjo una proporción mayor de partículas maduras cerca de los orgánulos de replicación. A pesar de estas diferencias microscópicas, ambas variantes mostraron patrones de crecimiento y enfermedad similares en un modelo de ratón, lo que sugiere que el virus puede tolerar un rango de eficiencias de maduración y aun así permanecer infeccioso.
Observando la infección directamente en el cerebro
La mayoría de los estudios estructurales de virus se basan en líneas celulares, pero este trabajo se extiende al tejido vivo. Los investigadores aislaron una estructura cerebral llamada plexo coroideo de ratones infectados y la prepararon para tomografía crioelectrónica mediante congelación a alta presión y fresado con haz de iones enfocado. Incluso en este entorno complejo, observaron las mismas características distintivas: racimos de orgánulos de replicación, membranas engrosadas y vesículas cercanas llenas de partículas virales maduras. Esto demuestra que la remodelación de membranas y la secuencia estrechamente acoplada replicación–ensamblaje–maduración vista en células en cultivo también opera en el cerebro, donde estos virus causan enfermedad.
Por qué importan estos flujos de trabajo ocultos
Para el público general, el mensaje central es que estos virus que infectan el cerebro ejecutan una línea de ensamblaje altamente organizada dentro de nuestras células. Esculpen membranas celulares en pequeñas burbujas presurizadas donde se copian genomas, conectan esas burbujas directamente con sitios donde las nuevas partículas geman e incluso inician los pasos finales de maduración al alcance de la réplica original. Identificar las membranas de replicación engrosadas, el complejo proteico que atraviesa el cuello y los compartimentos de maduración estrechamente entrelazados no solo explica por qué los flavivirus se replican con tanta eficiencia, sino que también señala nuevos objetivos para fármacos antivirales diseñados para interrumpir las fábricas ocultas y las vías de ensamblaje del virus.
Cita: Dahmane, S., Schexnaydre, E., Zhang, J. et al. Cryo-electron tomography reveals coupled flavivirus replication, budding and maturation. Nat Commun 17, 828 (2026). https://doi.org/10.1038/s41467-026-68483-4
Palabras clave: flavivirus, tomografía crioelectrónica, orgánulos de replicación, maduración viral, encefalitis transmitida por garrapatas