Clear Sky Science · es
Perspectiva espectroelectroquímica sobre catalizadores de cobre-cobalto para la codelectrorreducción de CO2 y nitrito a urea
Convertir gases residuales en fertilizante
El fertilizante urea sostiene la agricultura moderna, pero su producción convencional consume mucha energía y genera altas emisiones de carbono. Este estudio explora un enfoque muy distinto: usar electricidad para convertir directamente dióxido de carbono (CO2) y residuos nitrogenados (como nitrito procedente de humos o aguas residuales) en urea. Para el lector no especializado, el atractivo es claro: una vía para obtener un fertilizante esencial que podría reducir emisiones, aprovechar corrientes de residuos como materias primas y, en el futuro, funcionar con electricidad renovable.
¿Por qué replantear la fabricación de urea?
Hoy en día, la urea se fabrica mayormente produciendo primero amoníaco a partir de nitrógeno e hidrógeno de origen fósil (proceso Haber–Bosch), y luego reaccionando ese amoníaco con CO2 a altas temperaturas y presiones. Esta cadena de reacciones está centralizada, requiere gran inversión y emite cerca de una tonelada de CO2 por cada tonelada de urea producida. A medida que crece la demanda global de fertilizantes, también lo hacen los costos ambientales. Una alternativa es eludir los combustibles fósiles por completo haciendo que los pasos químicos clave los impulse la electricidad, preferiblemente renovable, y usando CO2 y óxidos de nitrógeno (NOx) que hoy se tratan como residuos.
Un nuevo papel para el cobre y el cobalto
Los autores diseñan catalizadores en película delgada obtenidos por co-sputtering de cobre (Cu) y cobalto (Co) sobre papel de carbono, ajustando cuidadosamente la relación Cu:Co. Se centran en la reducción electroquímica simultánea de CO2 y nitrito (NO2⁻) en agua a pH neutro, un entorno que puede favorecer la formación tenue de enlaces carbono–nitrógeno (C–N) necesarios para la urea. La composición más destacada es una mezcla 1:1 de Cu y Co, que alcanza una tasa de producción de urea de aproximadamente 61 milimoles por hora y por gramo de catalizador a un voltaje aplicado moderado. Microscopía y medidas con rayos X muestran que los metales están íntimamente mezclados a escala atómica y permanecen en gran medida metálicos durante la operación, proporcionando una plataforma robusta donde tanto el CO2 como el nitrito pueden reaccionar de forma eficiente. 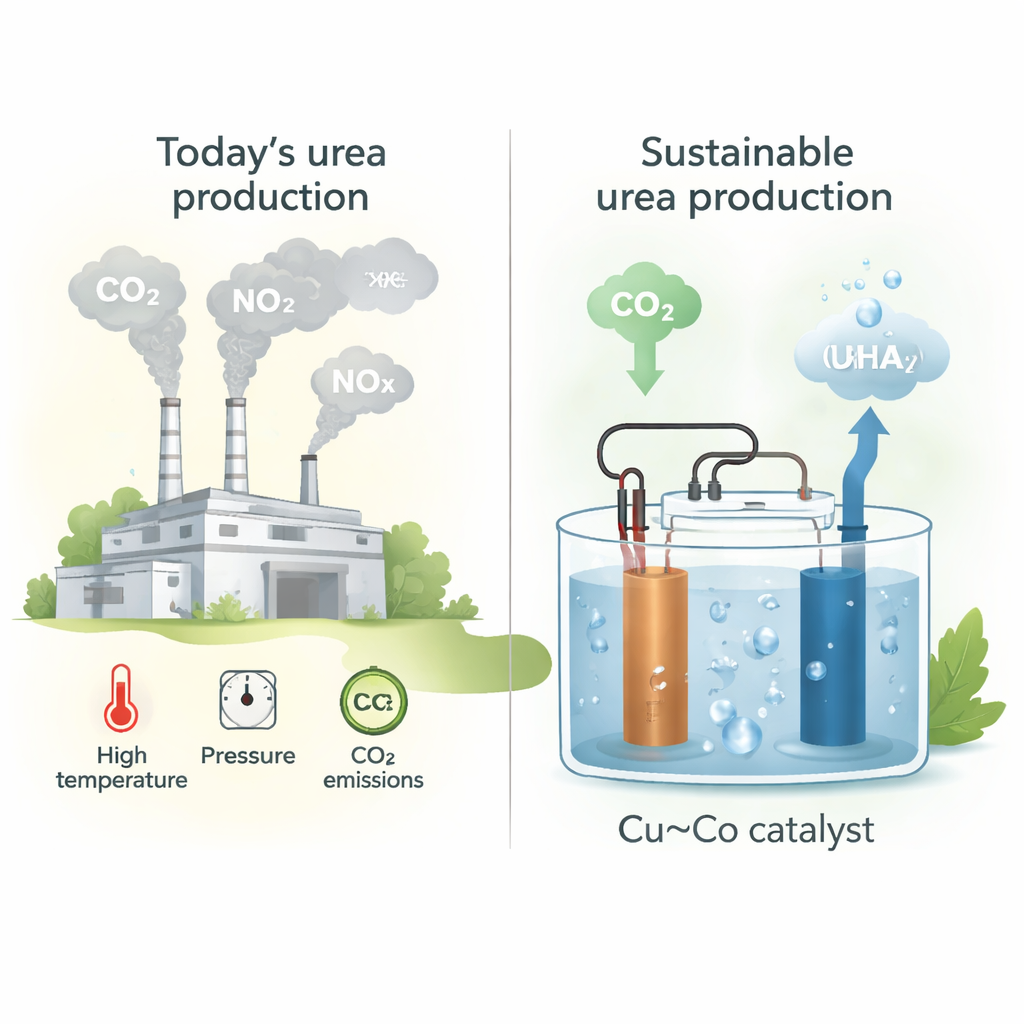
Cómo el catalizador divide y comparte el trabajo
Producir urea de este modo es un reto porque reacciones más simples —como generar hidrógeno o reducir CO2 o nitrito por separado— compiten de forma intensa. La clave, concluyen los investigadores, es una división del trabajo entre sitios de cobre y de cobalto que actúan de manera cooperativa. Las pruebas electroquímicas muestran que el cobre por sí solo convierte principalmente el CO2 en combustibles y productos carbonados, mientras que el cobalto por sí solo convierte mayoritariamente el nitrito en amoníaco, sin producir urea en ninguno de los casos. Solo cuando los átomos de Cu y Co están mezclados de forma próxima se observa una producción significativa de urea. “Instantáneas” espectroscópicas tomadas durante la reacción detectan fragmentos característicos ligados a la superficie: especies de carbono derivadas del CO2 (*CO y *COOH) que prefieren el cobre, y especies nitrogenadas derivadas del nitrito (*NH2 y grupos relacionados) que prefieren el cobalto. En los límites entre Cu y Co, estos fragmentos pueden encontrarse y acoplarse para formar la columna vertebral C–N de la urea.
Encontrar las condiciones adecuadas para formar enlaces
El estudio demuestra que la composición por sí sola no basta; también hay que afinar la solución y la membrana circundantes. La urea aparece únicamente en un electrolito bicarbonato neutro, que mantiene suficiente CO2 disuelto disponible y suministra la cantidad justa de protones (iones hidrógeno) para impulsar pasos de “transferencia de electrones acoplada a protones” sin saturar la superficie con evolución de hidrógeno. En condiciones fuertemente ácidas o fuertemente alcalinas, la urea no se forma o se descompone rápidamente en productos más simples. Experimentos con diferentes fuentes de nitrógeno revelan que el nitrito es especialmente eficaz para la formación de urea, superando a nitrato e hidroxilamina. Ensayos prolongados indican que las películas de Cu–Co son relativamente estables, con pérdida de metal moderada y una producción sostenida de urea.
Mirando bajo el capó con teoría
Para entender por qué este catalizador en tándem funciona tan bien, el equipo recurre a simulaciones por ordenador basadas en teoría del funcional de la densidad. Estos cálculos respaldan la idea de que el cobre favorece la adsorción de especies derivadas del CO2, mientras que el cobalto activa mejor el nitrito y estabiliza fragmentos con nitrógeno. Las simulaciones señalan un paso particular como el cuello de botella energético: el acoplamiento de un fragmento *NH2 (procedente del nitrito) con un fragmento *COOH (procedente del CO2) para formar un intermedio a veces escrito como *NH2CO. Una vez que se forma esta pieza, los pasos restantes hacia la urea son comparativamente sencillos. La interfaz Cu–Co reduce el coste energético de este acoplamiento crucial frente al cobre o al cobalto puros, lo que explica el aumento observado experimentalmente en el rendimiento de urea para el sistema bimetálico. 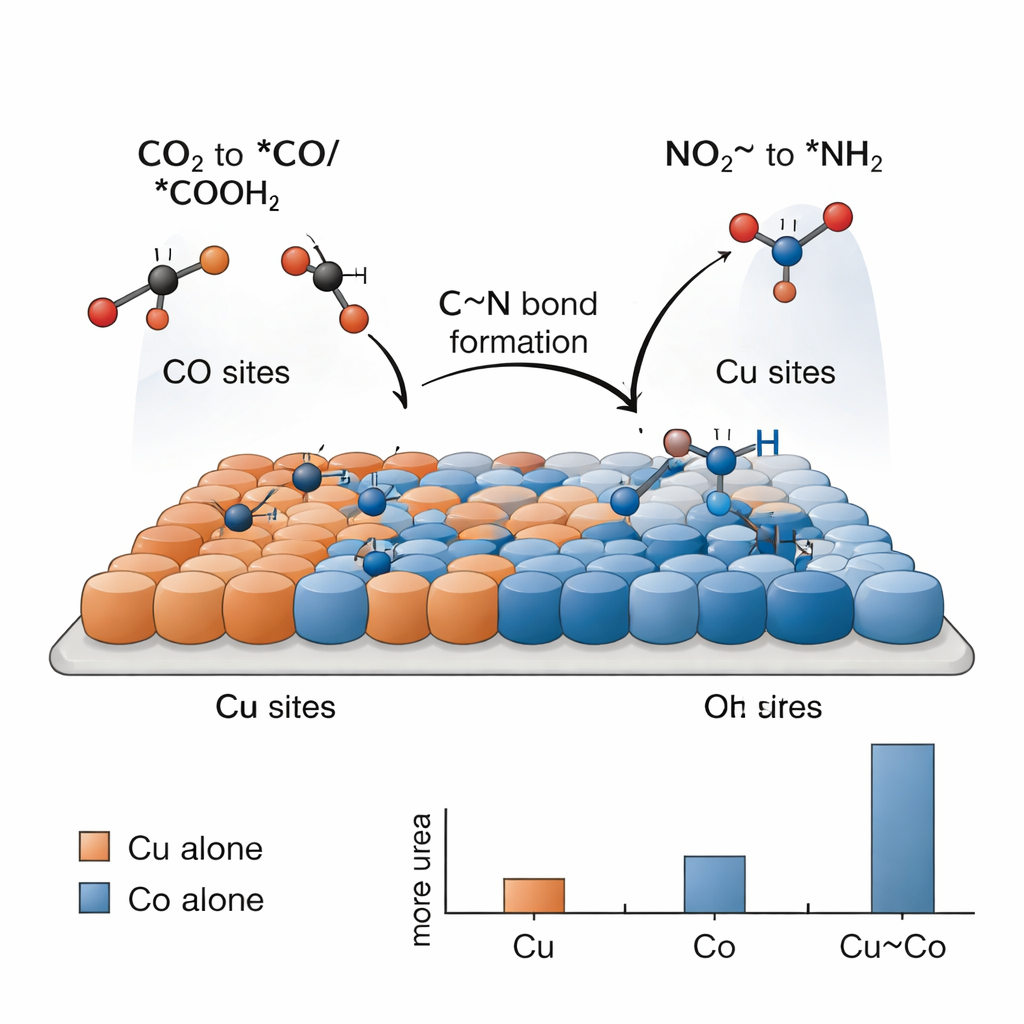
De la visión de laboratorio a un fertilizante más verde
En términos prácticos, este trabajo aún no sustituye a las gigantescas plantas de urea actuales, pero aclara cómo podría diseñarse una vía electroquímica en el futuro. Al mostrar que cobre y cobalto pueden operar en tándem —uno suministrando especies de carbono activadas, el otro especies de nitrógeno activadas, ambos bajo condiciones de protones cuidadosamente controladas— el estudio traza una ruta realista hacia una producción de urea más limpia y potencialmente descentralizada que utilice CO2 y residuos nitrogenados como recursos en lugar de contaminantes.
Cita: Ramadhany, P., Trần-Phú, T., Yuwono, J.A. et al. Spectroelectrochemical insight into copper cobalt catalysts for CO2 and nitrite co-electroreduction to urea. Nat Commun 17, 1776 (2026). https://doi.org/10.1038/s41467-026-68481-6
Palabras clave: síntesis electroquímica de urea, catálisis cobre cobalto, utilización de CO2, reducción de nitrito, acoplamiento C–N