Clear Sky Science · es
Base estructural para la inhibición selectiva del transportador humano de GABA GAT3
Por qué importan las señales que calman el cerebro
Nuestros cerebros dependen de un delicado equilibrio entre señales que excitan y las que calman. Un mensajero clave en la inhibición es el GABA, una molécula que ayuda a evitar la actividad descontrolada asociada con afecciones como la epilepsia, el daño por ictus y la enfermedad de Alzheimer. Este estudio se centra en una proteína llamada GAT3, que elimina el GABA del entorno de las neuronas. Al revelar, con detalle atómico, cómo una nueva molécula se une a GAT3 y lo bloquea, los investigadores ofrecen una hoja de ruta estructural para diseñar fármacos de próxima generación que podrían potenciar de forma sutil el freno natural del cerebro.
El propio pedal de freno del cerebro
El GABA es el principal neurotransmisor inhibitoria, o calmante, del sistema nervioso central. Tras su liberación desde las terminaciones nerviosas, el GABA debe eliminarse rápidamente para que los circuitos cerebrales puedan reiniciarse. Esa limpieza la realizan proteínas transportadoras que bombean GABA de vuelta a las células. Dos de estos transportadores dominan en el cerebro: GAT1, presente principalmente en neuronas, y GAT3, presente en células de soporte llamadas astrocitos. Mientras que un fármaco que bloquea GAT1 (tiagabina) se ha usado durante décadas para tratar la epilepsia, los medicamentos comparables dirigidos a GAT3 han tardado en llegar. Sin embargo, GAT3 es especialmente interesante porque controla los niveles de GABA fuera de las sinapsis y configura una inhibición de fondo duradera que puede afinar la actividad cerebral. 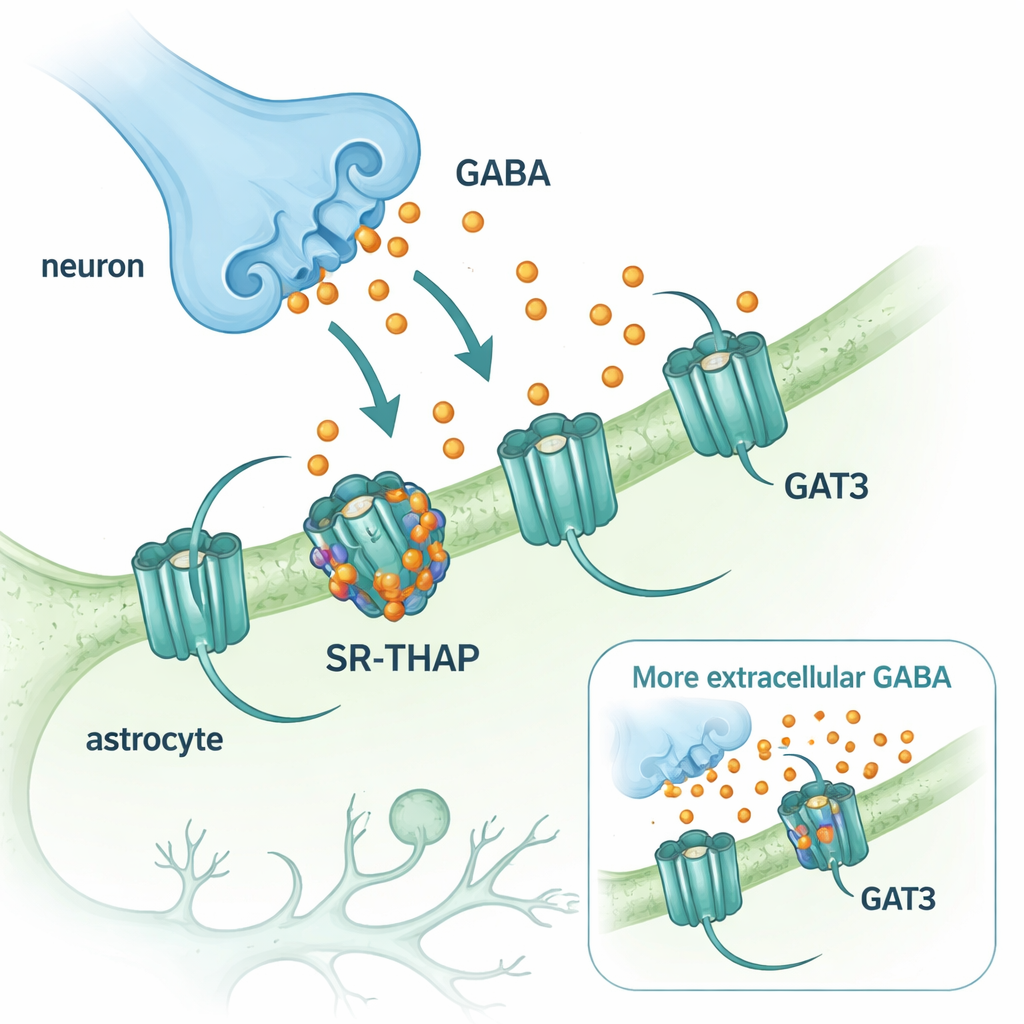
Diseñando un cerrojo molecular más preciso
Los intentos por inhibir GAT3 se han visto limitados por la falta de información estructural detallada. Muchos compuestos anteriores se crearon por ensayo y error, a menudo haciendo variaciones voluminosas de moléculas conocidas similares al GABA. Uno de los más conocidos, (S)-SNAP-5114, resultó ser químicamente inestable y difícil de usar en animales vivos. Partiendo de un pariente más estable de este compuesto, los autores desarrollaron SR-THAP, una nueva pequeña molécula diseñada para encajar mejor en GAT3 y resistir la degradación. Experimentos en cultivos celulares humanos mostraron que SR-THAP bloquea con fuerza GAT3 y lo hace de forma no competitiva: en lugar de competir simplemente con el GABA en el sitio habitual, cambia el modo de funcionamiento del transportador, reduciendo su capacidad máxima de transporte.
Viendo a GAT3 a resolución casi atómica
Para entender exactamente cómo actúa SR-THAP, el equipo recurrió a la criomicroscopía electrónica, una técnica que imagina proteínas congeladas instantáneamente con electrones y reconstruye su forma tridimensional. Resolvieron tres versiones del GAT3 humano: ligado a SR-THAP, ligado a GABA y en un estado libre de sustrato. Las tres revelan la arquitectura típica observada en transportadores relacionados de neurotransmisores: 12 hélices compactas que atraviesan la membrana y forman una vía central para el GABA y sus iones acompañantes, sodio y cloro. En la estructura ligada a GABA, el transportador se encuentra en un estado “ocluido hacia el interior”: GABA y un ión sodio quedan atrapados en el centro, aislados tanto del exterior como del interior. Un aminoácido aromático clave forma una interacción especializada con el grupo amino del GABA, lo que ayuda a explicar cómo GAT3 reconoce su sustrato.
Cómo SR-THAP cala el transportador abierto
En marcado contraste, la estructura ligada a SR-THAP captura a GAT3 en un estado “abierto hacia el interior”, con el lado interno de la proteína abierto hacia el interior celular. SR-THAP se aloja en lo profundo de esta cavidad interna, encajada entre varias hélices que normalmente se desplazan durante el ciclo de transporte. Ocupa tres pequeños huecos con caracteres químicos distintos, estableciendo una red de enlaces de hidrógeno y contactos hidrofóbicos. Esta posición atasca efectivamente el transportador para que el GABA y los iones ya no puedan completar su recorrido. Los autores muestran que algunos aminoácidos específicos que recubren esta cavidad difieren entre GAT3 y sus parientes cercanos; sustituir uno de estos residuos altera tanto la actividad de transporte como la potencia de SR-THAP, lo que ayuda a explicar por qué el inhibidor es mucho más selectivo para GAT3 que para GAT1 u otros transportadores relacionados. 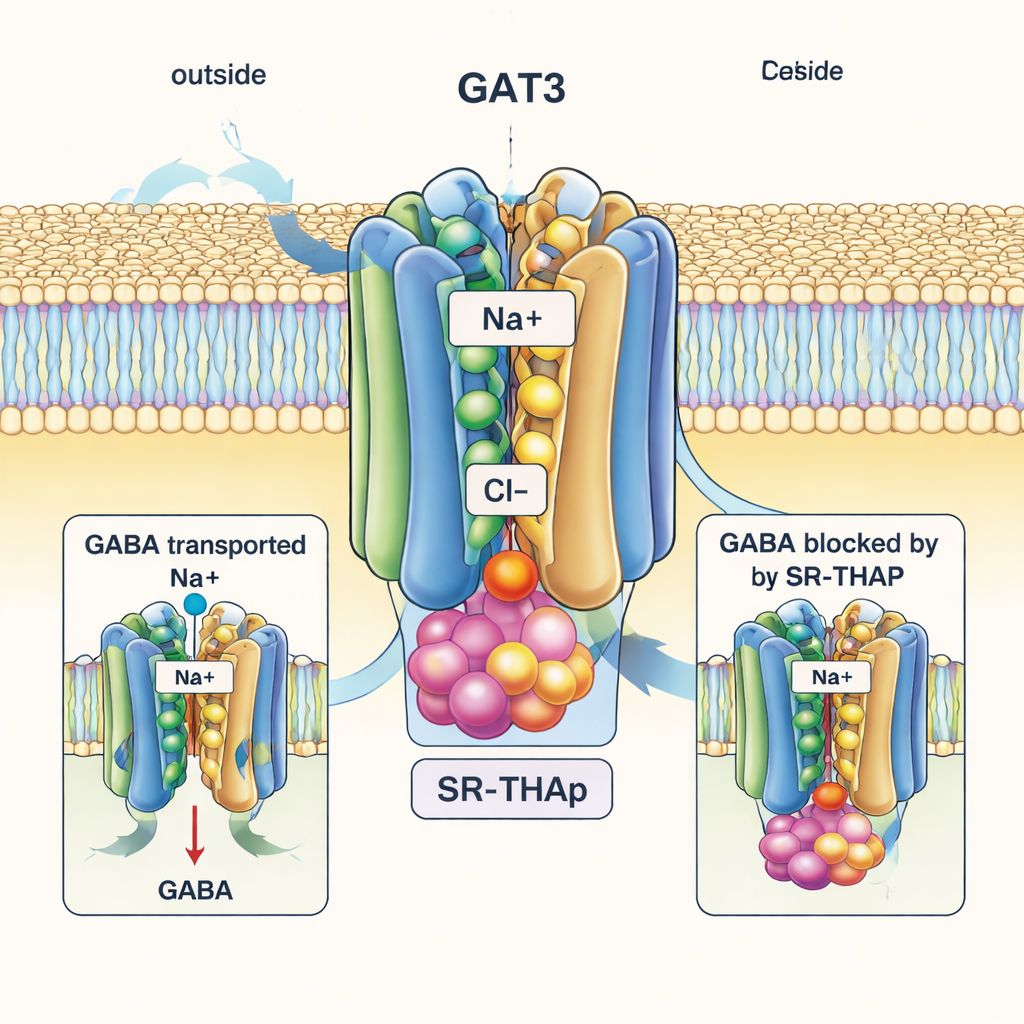
Abriendo puertas a nuevos fármacos para la epilepsia y la salud cerebral
En conjunto, estas estructuras revelan cómo GAT3 cicla entre diferentes conformaciones para mover el GABA, y cómo SR-THAP explota un bolsillo interno menos conservado para congelar ese ciclo. Para el público general, la conclusión clave es que el estudio proporciona un plano molecular detallado para desactivar GAT3 de forma altamente selectiva. Compuestos así podrían elevar los niveles de GABA calmante de manera más afinada que los fármacos existentes, lo que podría conducir a nuevos tratamientos o herramientas de investigación para la epilepsia, la recuperación tras un ictus, la enfermedad de Alzheimer y otras condiciones en las que la señalización inhibitoria está alterada.
Cita: Mortensen, J.S., Bavo, F., Jensen, M.H. et al. Structural basis for selective inhibition of human GABA transporter GAT3. Nat Commun 17, 1774 (2026). https://doi.org/10.1038/s41467-026-68479-0
Palabras clave: Transportador de GABA, GAT3, epilepsia, cryo-EM, inhibición de neurotransmisores