Clear Sky Science · es
Un mecanismo estocástico impulsa la translocación rápida de sustratos en la máquina AAA+ ClpB
Cómo las máquinas celulares mantienen las proteínas en movimiento
Dentro de cada célula, diminutas máquinas moleculares tiran, empujan y remodelan proteínas constantemente para evitar que se agrupen y para reparar daños. Una de estas máquinas, llamada ClpB, ayuda a rescatar proteínas que se han enredado: una función esencial para la supervivencia celular bajo estrés. Este estudio plantea una pregunta sencilla pero profunda: ¿cómo convierte ClpB el combustible químico ATP en trabajo mecánico para tirar de una cadena proteica a través de su poro central, y lo hace en pasos ordenados y regulares o de una manera más aleatoria y difusiva?
Un anillo rescatador de proteínas en acción
ClpB pertenece a una amplia familia de enzimas llamadas máquinas AAA+ que se ensamblan en estructuras en forma de anillo con un túnel central. Muchas de ellas se han representado con gran detalle mediante criomicroscopía electrónica, lo que ha dado lugar a un modelo popular de “mano a mano”: cada molécula de ATP consumida produciría un pequeño y preciso paso, como un equipo de personas tirando de una cuerda en secuencia. Sin embargo, otros experimentos sugerían que ClpB podría mover proteínas mucho más rápido de lo que su lenta tasa de consumo de ATP parecería permitir. Para resolver este enigma, los autores observaron moléculas únicas de ClpB en tiempo real mientras desplazaban una proteína de prueba flexible, κ-caseína, a través de su poro.
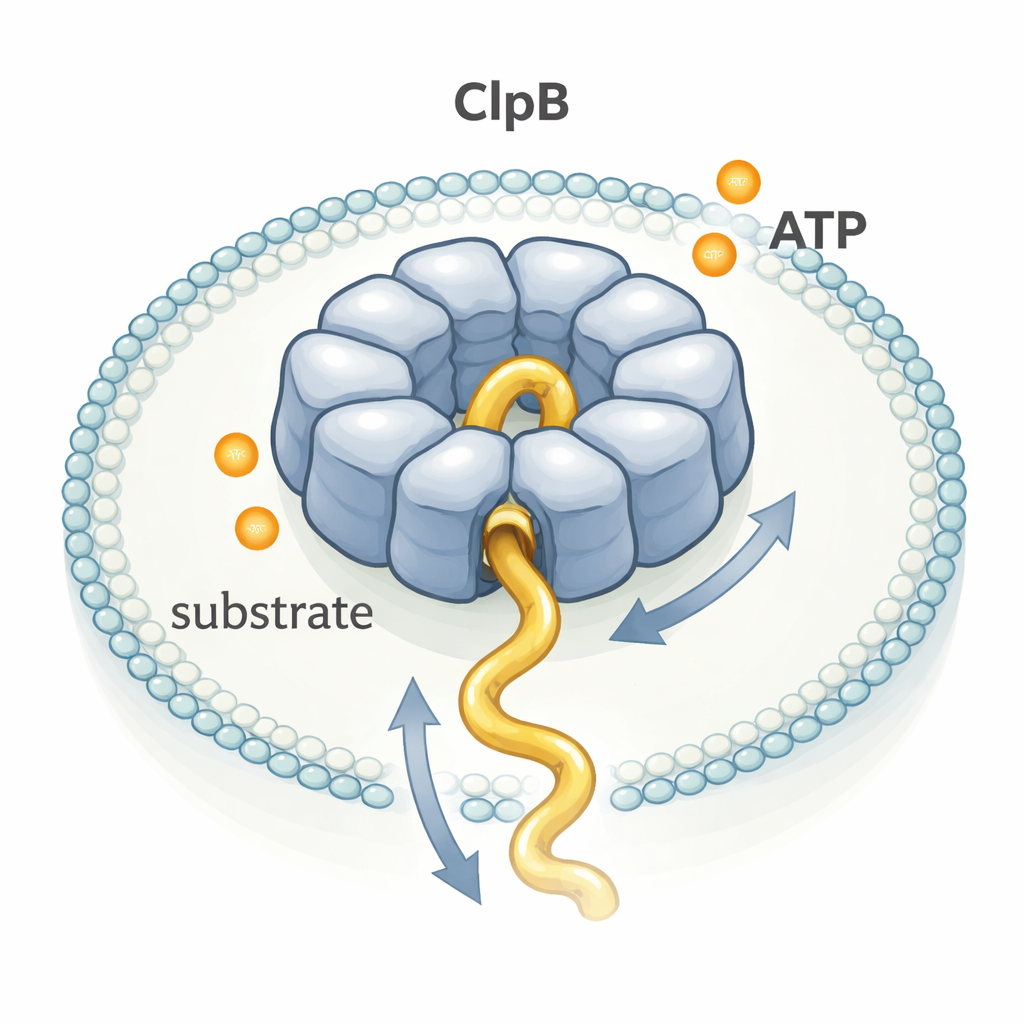
Observando una molécula a la vez
Los investigadores atraparon anillos individuales de ClpB y moléculas únicas de κ-caseína juntas dentro de pequeñas burbujas lipídicas pegadas a una superficie de vidrio. Unieron tintes fluorescentes a puntos específicos de ClpB y de la cadena proteica, y luego usaron FRET de una sola molécula, una técnica que informa sobre cambios de distancia entre tintes a escala nanométrica. Cuando la κ-caseína se deslizaba dentro del poro de ClpB, los tintes se acercaban y la señal FRET se disparaba en un pico breve; cuando la cadena salía, la señal caía de nuevo. Midiendo la duración y la amplitud de miles de picos así, pudieron deducir qué tan rápido y qué distancia recorrían segmentos de la proteína a través del poro.
Rápido, poco alimentado y casi independiente de la temperatura
Sorprendentemente, los eventos de translocación fueron extremadamente rápidos: el segmento marcado de κ-caseína típicamente atravesaba varios nanómetros del poro en aproximadamente 1–2 milisegundos, unas mil veces más rápido que el tiempo medio entre eventos de hidrólisis de ATP en ClpB. La mayoría de los eventos fueron tan cortos y siguieron una distribución amplia de ley de potencias en lugar de un único tiempo característico. Cambiar la temperatura de 10 a 32 °C apenas ralentizó estos movimientos, lo que implica que la barrera energética para el movimiento es diminuta en comparación con la de motores de “golpe de potencia” clásicos como la quinesina. De igual modo, reducir la concentración de ATP disminuyó mucho la frecuencia con la que ocurrían los eventos, pero tuvo casi ningún efecto sobre la duración de cada evento. El ATP, en otras palabras, controlaba más cuándo ClpB se activaba y con qué frecuencia actuaba, que la velocidad de los estallidos individuales de paso.
Movimiento de ida y vuelta con sesgo hacia adelante
Para ver si las cadenas siempre se movían en una dirección, el equipo realizó experimentos de FRET tricromática más complejos, tiñendo ambos extremos del poro y el sustrato. Esto les permitió distinguir si la κ-caseína entraba por la parte superior o inferior del anillo y si lo atravesaba por completo o retrocedía. Descubrieron seis patrones distintos: translocaciones completas hacia adelante y hacia atrás, visitas “parciales” más largas donde la cadena muestreaba ambos extremos del poro antes de salir, y encuentros fugaces cerca de un solo extremo. Aproximadamente tres cuartas partes de los eventos completos fueron en dirección hacia adelante, pero una fracción considerable fue hacia atrás, lo que revela que ClpB permite la difusión bidireccional de su sustrato con solo un sesgo moderado hacia adelante. Cuando el ATP se reemplazó por un análogo de hidrólisis lenta, los eventos se hicieron raros y mucho más lentos, y la preferencia hacia adelante desapareció esencialmente.
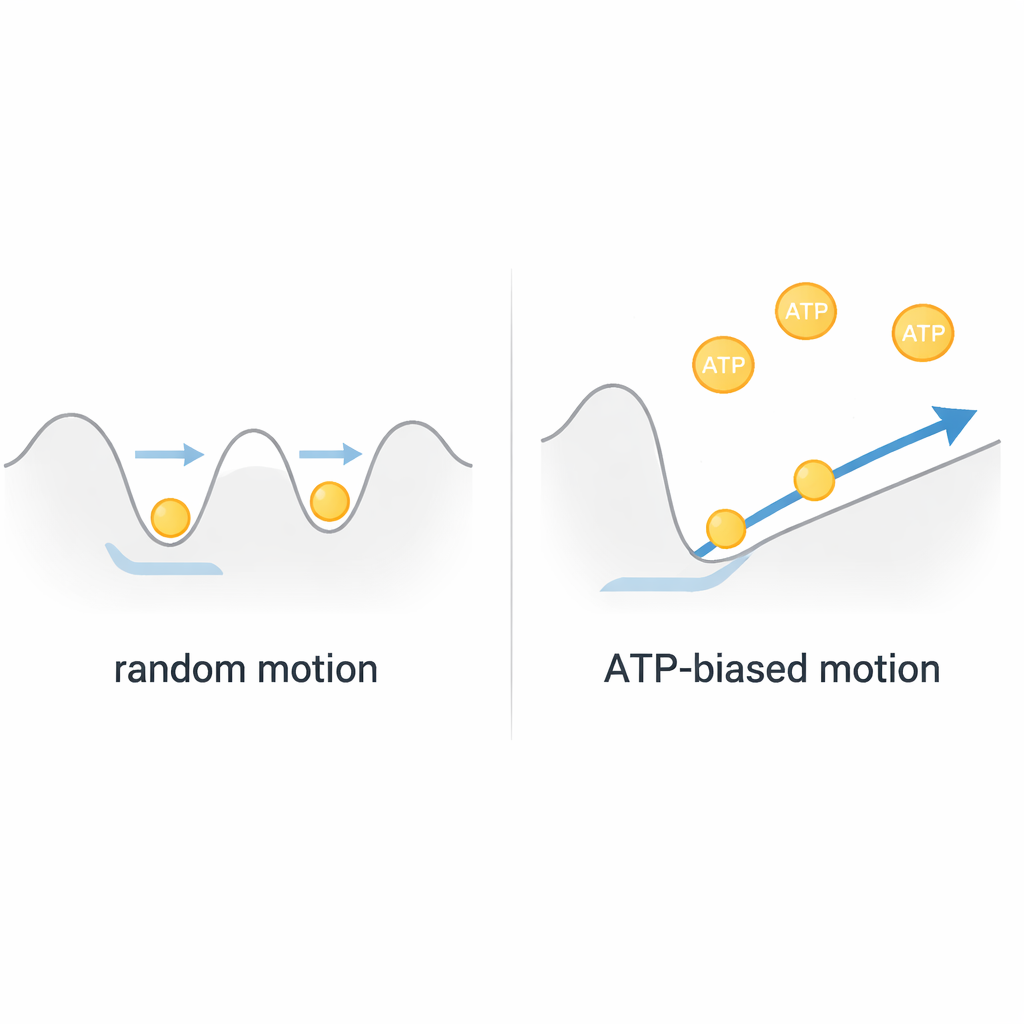
Un motor browniano, no un torno simple
Con estas observaciones en conjunto, los autores concluyen que ClpB funciona más como un motor browniano que como un torno rígido impulsado por combustible. La cadena proteica vibra térmicamente dentro de un paisaje energético poco profundo en el interior del poro, moviéndose de un lado a otro a alta velocidad. El ATP no alimenta directamente grandes tirones discretos; en cambio, modula la forma de este paisaje mediante movimientos rápidos de “lazos de poro” internos, favoreciendo sutilmente el movimiento en una dirección. Dado que cada evento completo de enhebrado se correlaciona con solo una o dos moléculas de ATP consumidas, ClpB logra un transporte notablemente eficiente y rápido al rectificar el movimiento aleatorio en lugar de oponerse a él. Esta visión reconfigura cómo pensamos sobre muchas máquinas AAA+, sugiriendo que los nanomotores biológicos a menudo pueden aprovechar la aleatoriedad en lugar de eliminarla.
Cita: Casier, R., Levy, D., Riven, I. et al. A stochastic mechanism drives fast substrate translocation in the AAA+ machine ClpB. Nat Commun 17, 1773 (2026). https://doi.org/10.1038/s41467-026-68478-1
Palabras clave: translocación de proteínas, máquina AAA+, motor browniano, chaperona molecular, FRET de una sola molécula