Clear Sky Science · es
Estructura de un bacteriófago de Brochothrix thermosphacta revela el mecanismo de adsorción en la pared celular de los sifófagos que infectan Gram-positivos
Virus que mantienen nuestros alimentos frescos
Los virus que matan bacterias, llamados bacteriófagos, influyen de forma silenciosa en nuestra salud y en el suministro de alimentos. Algunos provocan infecciones letales, pero otros pueden aprovecharse para combatir gérmenes alimentarios y el deterioro. Este estudio revela, con detallada resolución atómica, cómo uno de estos virus, denominado NF5, se adhiere y perfora la resistente cubierta externa de una bacteria que estropea la carne. Comprender esta batalla microscópica podría ayudarnos a diseñar formas más seguras de conservar alimentos y combatir bacterias resistentes a los antibióticos.
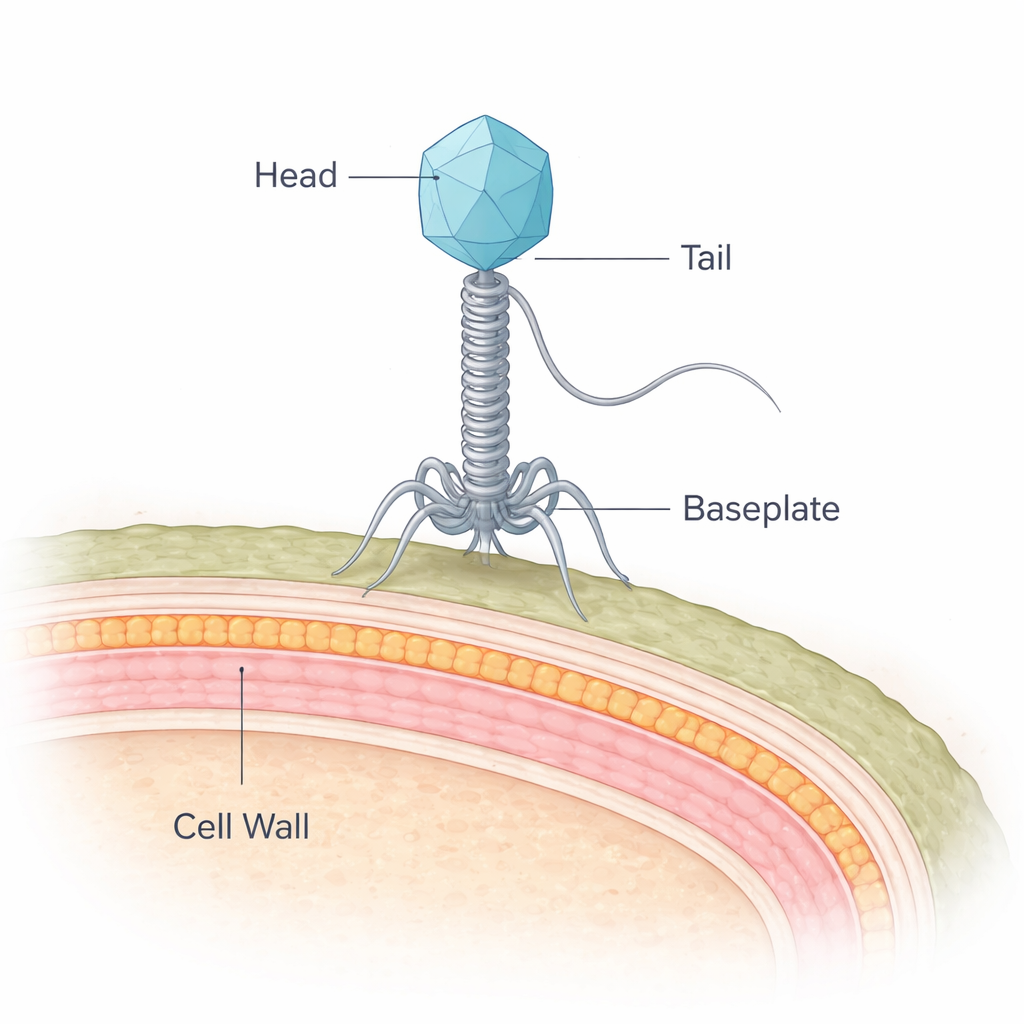
Un estropeador de carne se encuentra con su enemigo natural
La bacteria protagonista de este trabajo, Brochothrix thermosphacta, es una causa habitual de los olores desagradables y la baba que aparecen en la carne refrigerada. NF5 es un virus que infecta esta bacteria y pertenece a un grupo llamado sifófagos, que alojan su ADN en una cápside proteica y lo entregan a través de una cola larga y flexible. Mientras que los científicos han detallado las estructuras de muchos virus que infectan las llamadas bacterias Gram-negativas, los que atacan a Gram-positivas como B. thermosphacta han sido mucho menos comprendidos. Las Gram-positivas plantean un rompecabezas especial porque están protegidas por una pared celular gruesa y multicapa en lugar de una pared delgada y una membrana externa.
Construyendo una jeringa molecular, átomo a átomo
Empleando crio-microscopía electrónica de última generación, los investigadores congelaron millones de partículas de NF5 y reconstruyeron su estructura tridimensional a resolución casi atómica. Identificaron 11 proteínas virales diferentes que, en conjunto, ensamblan la cabeza viral, el cuello, el tubo de la cola y una compleja placa basal en la punta de la cola, con un total de 643 cadenas proteicas. La cabeza forma una resistente cápside icosaédrica alrededor del ADN viral, mientras que una cola de 135 nanómetros se extiende hacia abajo como una jeringa flexible. Anillos de proteínas repetidas forman un tubo de cola hueco, cuya superficie interna tiene una fuerte carga negativa —una disposición que probablemente ayuda al virus a disparar su ADN rápidamente dentro del huésped.
El taladro inteligente en la punta de la cola
La parte más intrincada de NF5 es la placa basal, una estructura en varias capas que actúa a la vez como sensor, taladro y ancla. Cerca del centro se sitúa una proteína “cinta métrica” que llena el tubo de la cola y una lisozina asociada a la cola que tapona el tubo hasta que comienza la infección. Rodeando este núcleo hay proteínas que reconocen y se agarran a la superficie bacteriana. Algunas funcionan como brazos elásticos que pueden doblarse dramáticamente, ayudando a que la placa basal se incline y luego se bloquee en una posición perpendicular a la pared celular. Otras semejan fibras halladas en virus relacionados y se piensa que se unen a moléculas específicas en la gruesa pared Gram-positiva e incluso lamen partes de la red rica en azúcares de la pared celular. De forma intrigante, una proteína de fibra lateral de NF5 parece combinar funciones que en otros virus de Gram-positivos están repartidas en varias proteínas, lo que sugiere un diseño evolutivamente eficiente y simplificado.
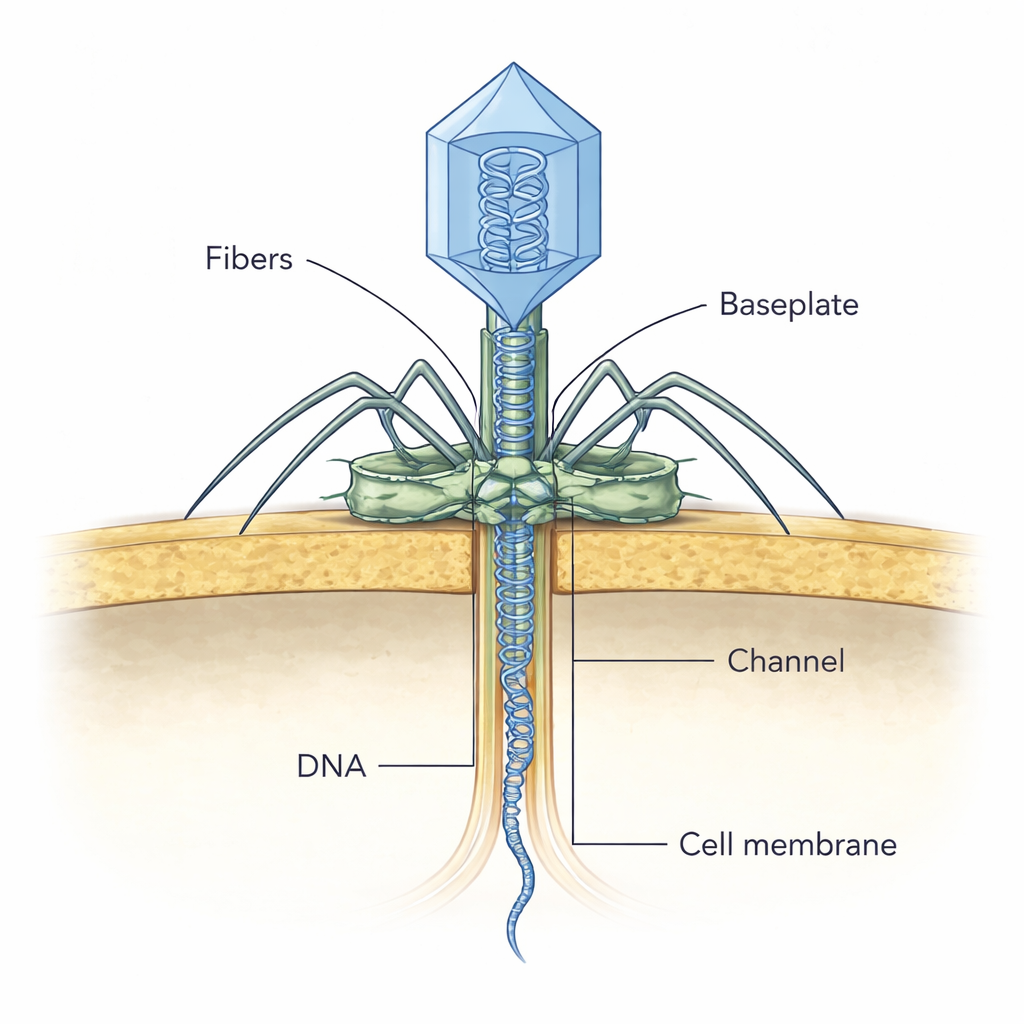
Capturando un virus en acción
Para ver cómo funcionan estas piezas durante la infección, el equipo empleó crio-tomografía electrónica en secciones delgadas de bacterias infectadas. Captaron partículas de NF5 en distintos estadios aparentes del ataque. En instantáneas tempranas, el virus se adhiere a la pared celular en un ángulo, probablemente usando sus fibras exteriores para localizar receptores adecuados. Más tarde, la placa basal se alinea perpendicular a la superficie celular, y la cabeza viral aún aparece llena de ADN. En etapas posteriores, el interior de la cabeza desaparece a medida que se libera el ADN, y aparece una delgada densidad en forma de canal que atraviesa la pared bacteriana hacia la membrana celular. Los autores proponen que, una vez que la enzima de la punta de la cola contacta y digiere la pared celular, se rearregla, abriendo el tapón y permitiendo que la proteína cinta métrica se deslice y forme este túnel temporal por el que el ADN viral viaja protegido hacia el interior de la célula.
Por qué importa más allá de un solo virus
Al comparar NF5 con virus que infectan otras bacterias, los investigadores muestran que las proteínas clave de la cola y la placa basal han evolucionado de forma diferente en fagos de Gram-positivos frente a Gram-negativos para enfrentarse a las arquitecturas superficiales tan distintas de sus huéspedes. Estos ajustes estructurales —dominios adicionales, brazos más largos o funciones combinadas en proteínas individuales— parecen ser adaptaciones finamente ajustadas a paredes celulares más gruesas y complejas. El trabajo ofrece un plano detallado de cómo un virus puede reconocer, adherirse y franquear una barrera bacteriana resistente, proporcionando una base para diseñar fagos o herramientas inspiradas en fagos que ayuden a controlar mejor el deterioro alimentario y, potencialmente, a combatir patógenos Gram-positivos dañinos.
Cita: Peng, Y., Pang, H., Zheng, J. et al. Structure of a Brochothrix thermosphacta bacteriophage reveals cell wall adsorption mechanism in Gram-positive infecting siphophages. Nat Commun 17, 1772 (2026). https://doi.org/10.1038/s41467-026-68477-2
Palabras clave: estructura de bacteriófago, bacterias Gram-positivas, crio-microscopía electrónica, control del deterioro alimentario, mecanismo de infección por fagos