Clear Sky Science · es
Identificación de PAM no canónicos termotolerantes para una detección robusta en un solo recipiente con CRISPR-Cas12a
Subiendo la temperatura de las pruebas de ADN
Las pruebas rápidas y precisas para infecciones y cambios genéticos son esenciales en medicina, pero las pruebas de ADN actuales con frecuencia requieren equipos de laboratorio complejos y pueden pasar por alto dianas raras o sutiles. Este estudio muestra que simplemente ejecutar una prueba basada en CRISPR a una temperatura algo más alta desbloquea muchos más “puntos de agarre” útiles en el ADN, lo que hace que los diagnósticos en un solo tubo sean más rápidos, más sensibles y capaces de distinguir incluso diferencias de una sola letra en el código genético. 
Por qué CRISPR necesita un código postal
Las herramientas CRISPR como Cas12a actúan localizándose en tramos específicos de ADN, guiadas por un pequeño ARN que funciona como cadena de búsqueda. Pero solo pueden engancharse y empezar a actuar si cerca hay una etiqueta de cuatro letras, llamada PAM, con la secuencia adecuada—tradicionalmente un conjunto estrecho que comienza por “TTT”. Es como necesitar un número de casa antes de entregar una carta: si falta el número correcto, el mensaje nunca llega. Este requisito de PAM limita dónde puede actuar CRISPR, un inconveniente serio cuando los médicos deben detectar mutaciones concretas, marcadores de resistencia a fármacos o variantes virales que no están junto a estas etiquetas clásicas.
Descubriendo nuevas “puertas” a temperaturas más altas
Los investigadores probaron sistemáticamente las 256 combinaciones posibles de PAM de cuatro letras para ver cuánto impulsaban la actividad de corte “colateral” de Cas12a—su capacidad de cortar muchas piezas de ADN cercanas una vez que encuentra su diana, que es la base de las señales en los diagnósticos CRISPR. A la temperatura corporal normal (37 °C), solo un puñado de PAM no estándar funcionaba tan bien como los clásicos. Pero al elevar la temperatura de la reacción a unos 45 °C, ocurrió algo llamativo: 82 PAM no canónicos diferentes empezaron a producir una fuerte actividad de corte señaladora, rivalizando con las etiquetas estándar. El equipo piensa que el calor adicional relaja la estructura local del ADN y hace que el complejo Cas12a sea más flexible, reduciendo la barrera para reconocer estos PAM previamente “débiles”.
Señal fuerte, cuidado con la plantilla
Cas12a tiene dos modos de corte. En modo “cis”, corta el ADN específico que se le indicó; en modo “trans”, una vez activado, corta rápidamente cualquier hebra cercana que lleve la señal, lo que ilumina la prueba. Los investigadores encontraron que a temperaturas más altas, los PAM no canónicos produjeron un corte trans muy fuerte—excelente para una lectura brillante y rápida—pero mantuvieron relativamente débil el corte cis del ADN principal. Esa combinación es ideal para pruebas en un solo tubo, donde el ADN debe primero amplificarse sin destruirse. También demostraron que en estos ajustes más cálidos Cas12a se vuelve mucho más exigente respecto a desajustes entre el ARN guía y la diana: incluso una sola letra equivocada puede apagar la señal, especialmente al usar PAM no canónicos. 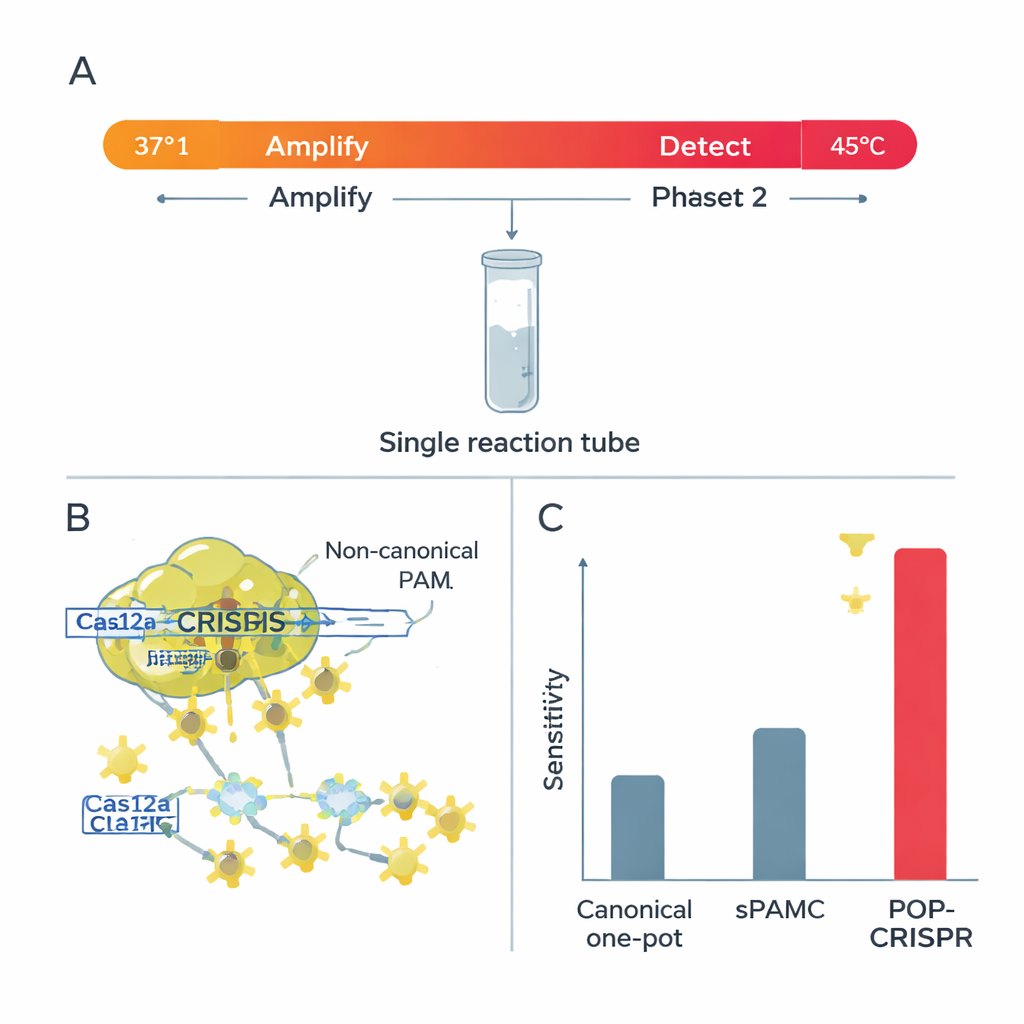
Una prueba de un solo recipiente más inteligente: POP-CRISPR
Basándose en estos hallazgos, el equipo creó POP-CRISPR, un ensayo “poiquilotérmico” (temperatura variable) en un solo recipiente. La reacción comienza alrededor de 37 °C, donde un método de amplificación isotérmica multiplica discretamente cualquier ADN o ARN diana mientras Cas12a está relativamente inactivo. Tras unos 10 minutos, la mezcla se calienta hasta alrededor de 45 °C, un punto óptimo en el que Cas12a—ahora dirigida a sitios PAM no canónicos—activa un potente corte trans y genera una fuerte señal fluorescente. Este simple programa de dos temperaturas aumentó la sensibilidad de detección aproximadamente diez veces en comparación con métodos CRISPR de un solo tubo previos que también usaban PAM débiles, y superó claramente a los formatos convencionales de un solo tubo con PAM canónicos.
Del banco a la cabecera en minutos
El sistema POP-CRISPR se probó con muestras clínicas reales. Detectó con sensibilidad el virus del papiloma humano (VPH-16) en hisopos vaginales y Mycoplasma pneumoniae en hisopos respiratorios, incluidas muestras de muy baja carga “zona gris” que desafían a los métodos estándar. De forma crucial, POP-CRISPR pudo distinguir cepas de Mycoplasma resistentes a fármacos que portaban un cambio de una sola letra en un gen ribosomal, aunque no hubiera un PAM clásico cerca de esa mutación—una tarea que frustra a muchas pruebas Cas12a existentes. Para hacer el enfoque apto para campo, los autores combinaron un paso rápido de lisis con calor y Chelex de dos minutos (evitando una extracción completa de ADN) con un lector de fluorescencia del tamaño de la palma controlado por un teléfono inteligente. Juntos, este flujo de trabajo puede convertir un hisopo crudo en un resultado digital sí/no en alrededor de 20 minutos.
Qué significa esto para las pruebas de uso cotidiano
Al elevar la temperatura de la reacción y explotar un conjunto mucho más amplio de “puertas” PAM, este trabajo convierte a Cas12a en un sensor más flexible y preciso. POP-CRISPR ofrece una detección de ácidos nucleicos más rápida, más sensible y más específica en un único tubo cerrado, al tiempo que amplía el rango de sitios genéticos que se pueden dirigirse—incluidas mutaciones de una sola base vinculadas a resistencia a fármacos o cáncer. Para los pacientes, eso podría traducirse en diagnósticos más rápidos en el lugar y tratamientos mejor ajustados; para investigadores y desarrolladores de pruebas, ofrece una nueva forma potente de diseñar diagnósticos CRISPR que sean a la vez más robustos y más discriminantes.
Cita: Tian, T., Zhang, T., Zhang, W. et al. Identification of thermotolerant non-canonical PAMs for robust one-pot CRISPR-Cas12a detection. Nat Commun 17, 1771 (2026). https://doi.org/10.1038/s41467-026-68476-3
Palabras clave: Diagnósticos CRISPR, Cas12a, Sitios PAM, pruebas punto de atención, detección de ácidos nucleicos