Clear Sky Science · es
Mecanismos estructurales de inhibición y activación del canal de potasio humano de pequeña conductancia activado por Ca2+ SK2
Por qué importan los pequeños canales de potasio
Cada pensamiento que tienes y cada latido que sientes dependen de señales eléctricas en tus células. Esas señales las moldean poros microscópicos, llamados canales iónicos, que permiten el flujo de átomos cargados hacia dentro y hacia fuera. Una familia de estos, los canales de potasio de pequeña conductancia activados por calcio (canales SK), ayuda a controlar cómo disparan las neuronas y cómo el corazón mantiene su ritmo. Este artículo revela, con detalle atómico, cómo distintos fármacos y una toxina de abeja pueden ya sea bloquear o potenciar a un miembro clave de esta familia, el canal humano SK2 —hallazgos que podrían orientar nuevos tratamientos para trastornos que van desde la fibrilación auricular hasta el temblor y problemas de memoria.
Cómo los canales SK2 actúan como frenos celulares
Los canales SK2 se ubican en la membrana celular y actúan como diminutos frenos de la actividad eléctrica. Cuando el interior de una célula se llena brevemente de iones calcio durante una señal eléctrica, una proteína auxiliar llamada calmodulina detecta ese aumento. La calmodulina está unida al lado interior de SK2 y, cuando se une al calcio, tira de una parte del canal como de una cuerda de arranque, abriendo una puerta que permite que iones potasio salgan. Este flujo hacia fuera ayuda a silenciar la célula tras su disparo, modulando con qué frecuencia las neuronas pueden enviar señales y con qué fiabilidad laten las células cardíacas. Dado que los canales SK1–3 están ampliamente distribuidos en cerebro y corazón, y SK2 es un subtipo particularmente importante, entender exactamente cómo se abren, cierran y responden a fármacos es crucial para diseñar medicamentos precisos.
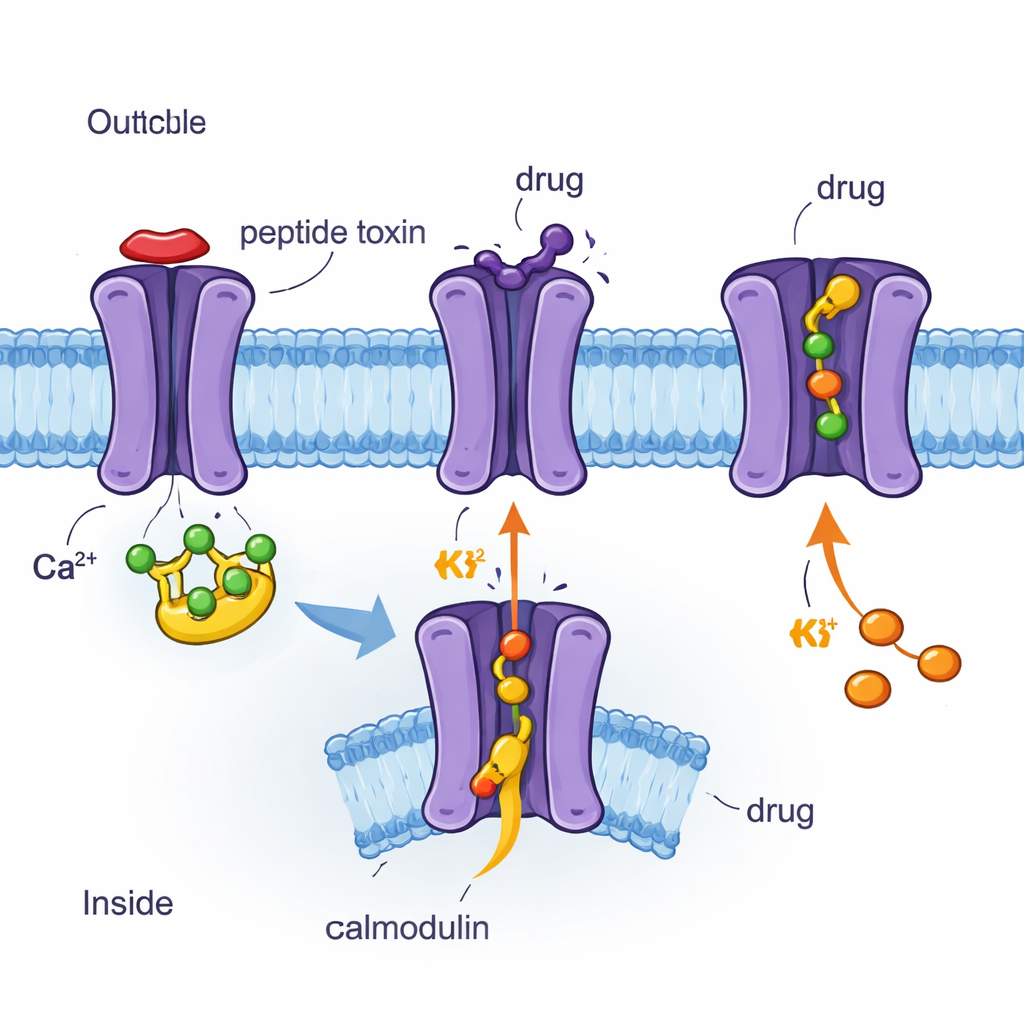
Usar cryo-EM para ver canales y fármacos átomo a átomo
Los autores emplearon microscopía crioelectrónica (cryo-EM), una técnica que imagina proteínas congeladas al instante con resolución cercana a la atómica, para determinar cuatro estructuras tridimensionales del canal humano SK2 unido a la calmodulina y a distintas moléculas. Estas incluyeron el péptido de veneno de abeja apamina, el bloqueador sintético UCL1684, el inhibidor clínico AP30663 y el activador clínico CAD-1883. Las cuatro estructuras muestran a SK2 como un ensamblaje de cuatro partes que atraviesa la membrana, con la calmodulina unida al interior. Comparar estas instantáneas reveló qué regiones del canal son rígidas, cuáles son flexibles y cómo se mueve la calmodulina cuando el canal está en estado cerrado o abierto. Los investigadores combinaron además estas imágenes con mediciones eléctricas en células, probando cómo cambios en aminoácidos específicos alteran la respuesta del canal a cada compuesto.
Una toxina de abeja y un fármaco de laboratorio que taponan la boca exterior
La apamina, un pequeño péptido del veneno de abeja, se conoce desde hace tiempo como un bloqueador extremadamente potente y selectivo de SK2 usado en investigación. Las nuevas estructuras muestran que la apamina se une como un corcho en la boca externa del poro de SK2. Se acopla en un vestíbulo en forma de copa formado por un bucle corto entre dos hélices (el enlazador S3–S4) que está bien ordenado en SK2 pero es flexible en un canal relacionado, SK4, lo que explica por qué SK4 es insensible a la apamina. Residuos clave con carga positiva en la apamina alcanzan entre cuatro cadenas aromáticas del canal, estableciendo fuertes interacciones electrostáticas y de apilamiento que sellan por completo la vía del potasio. UCL1684, un compuesto bis-quinolinios sintético, ocupa esencialmente el mismo bolsillo externo y también bloquea la salida de iones, pero su tamaño menor le permite colocarse más profundo, imitando la posición de las cargas positivas críticas de la apamina. Mutar residuos del canal que conforman este vestíbulo reduce drásticamente la sensibilidad a la apamina y, en menor medida, a UCL1684, confirmando que este lazo externo es un determinante principal de la acción de la toxina y del fármaco.
Un tapón central y una cuña interna que afinan la actividad
En contraste, el candidato clínico AP30663 se une dentro de la cavidad central de SK2, justo por debajo del filtro de selectividad que elige iones potasio. Allí actúa como un tapón físico, encajado entre cadenas laterales específicas que recubren el poro. Cambios en estos residuos de recubrimiento debilitan la capacidad de AP30663 para inhibir SK2, y las comparaciones de secuencia explican por qué sus análogos cercanos distinguen SK1–3 de SK4. CAD-1883, un modulador positivo desarrollado para trastornos del movimiento, emplea otra estrategia distinta. Se desliza en un bolsillo en la interfaz entre el lóbulo N de la calmodulina y un enlace corto (S4–S5) que acopla el movimiento de la calmodulina con la compuerta del canal. Al reforzar los contactos en este bolsillo, CAD-1883 efectivamente pega la calmodulina y SK2 en una configuración que tira de la compuerta interna hacia fuera y ensancha el poro. Las comparaciones estructurales muestran que este estado unido a CAD-1883 se asemeja a un canal completamente abierto, aunque el filtro de selectividad puede adoptar una forma inactivada tras una apertura prolongada.
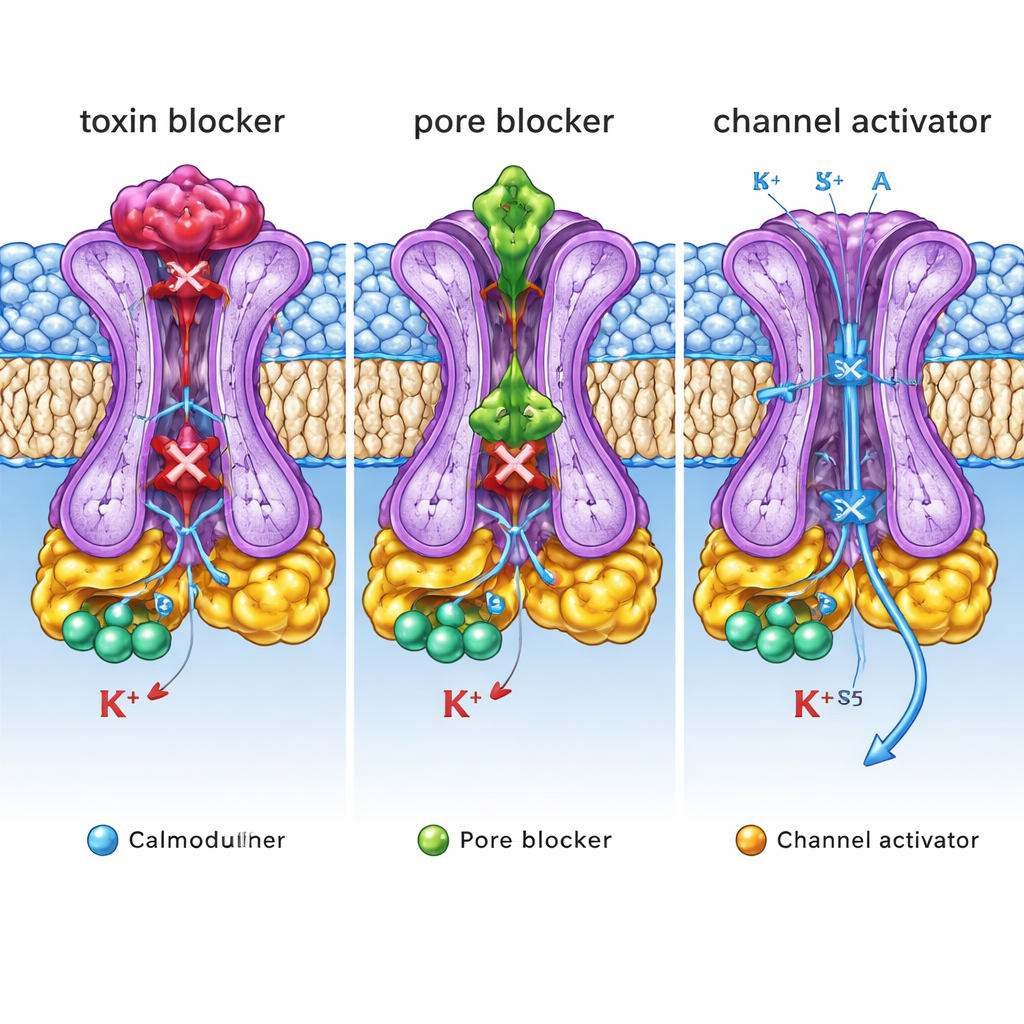
Qué significan estos planos estructurales para la medicina
En conjunto, estas estructuras revelan tres “perillas de control” distintas en un solo canal SK2: una tapa exterior donde se asientan toxinas y algunos bloqueadores, una cavidad interna del poro donde otros inhibidores taponan el flujo, y un bolsillo lateral donde los activadores estabilizan la apertura. Para el no especialista, el mensaje clave es que un mismo canal iónico puede sintonizarse hacia arriba o hacia abajo mediante fármacos que se agarran a asas estructurales muy distintas. Al mapear estas asas con precisión atómica y conectar esas ubicaciones con efectos funcionales, este trabajo proporciona un plano detallado para diseñar moléculas de próxima generación que atenúen o potencien selectivamente la actividad de SK2. Medicamentos a medida así podrían algún día ayudar a normalizar ritmos cerebrales anormales, aliviar temblores o corregir latidos irregulares con menos efectos secundarios.
Cita: Ma, B., Wu, D., Cao, E. et al. Structural mechanisms for inhibition and activation of human small-conductance Ca2+-activated potassium channel SK2. Nat Commun 17, 1770 (2026). https://doi.org/10.1038/s41467-026-68475-4
Palabras clave: canales de potasio SK2, canales activados por calcio, estructuras por cryo-EM, moduladores de canales iónicos, fibrilación auricular y temblor