Clear Sky Science · es
Migración y divisiones de células madre alteradas en la distrofia muscular de Duchenne reveladas por imágenes en vivo
Por qué importa esta historia muscular
La distrofia muscular de Duchenne (DMD) es una enfermedad infantil fatal que destruye gradualmente el músculo. Durante décadas, la mayor parte de la investigación se ha centrado en las grandes fibras musculares que se deterioran en la DMD. Este estudio muestra que un segundo y más silencioso protagonista también está en problemas: las propias células madre del músculo, que normalmente reparan el daño. Al observar estas células en vivo dentro de músculos de ratón y en fibras individuales, los autores revelan cómo las células madre en DMD pierden su rumbo, ofreciendo ideas nuevas para tratamientos que podrían ayudar a que los músculos se regeneren con mayor eficacia.
El equipo de reparación incorporado del músculo
Cada fibra muscular esquelética está flanqueada por un puñado de células madre residentes, conocidas como células satélite musculares. En un músculo sano, estas células permanecen en gran parte inactivas. Cuando se produce una lesión, se despiertan, se dividen y o bien generan nuevas células madre para reponer la reserva o bien producen células especializadas que se fusionan con las fibras dañadas. Este equilibrio entre autorrenovación y diferenciación mantiene el tejido muscular fuerte a lo largo de la vida. En la DMD, sin embargo, las fibras musculares se desgarran repetidamente porque carecen de distrofina, una proteína estructural clave, lo que plantea la cuestión de si el equipo de reparación mismo se agota o se desorienta.
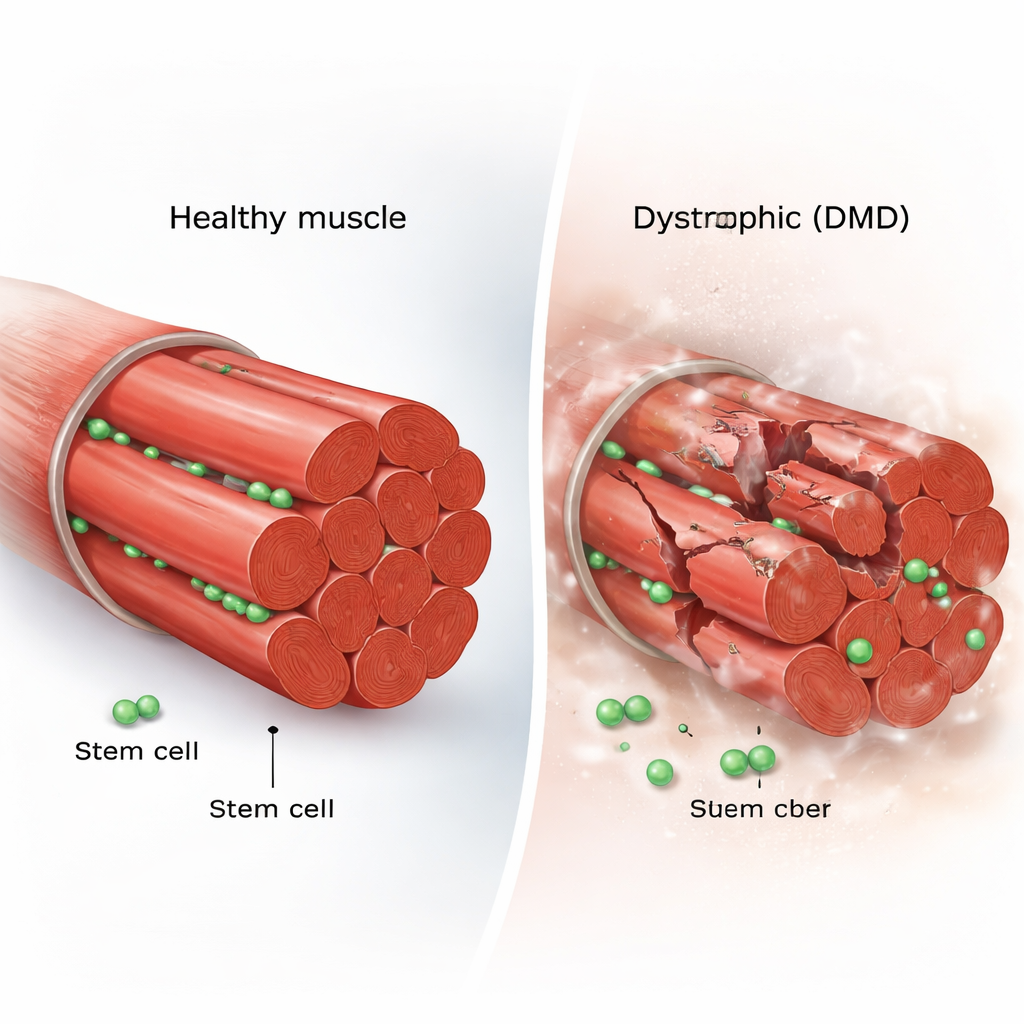
Filmando las células madre en acción
Para responder a esto, los investigadores utilizaron el ratón mdx, un modelo estándar de DMD, e hicieron que sus células madre musculares brillaran bajo el microscopio. A continuación realizaron imágenes intravitales, una técnica que permite filmar células vivas dentro de un animal anestesiado durante muchas horas. También desarrollaron un sistema personalizado de “micropocillos” para mantener fibras musculares individuales en cultivo mientras rastreaban cada división y movimiento de las células madre. Este enfoque dual les permitió seguir células individuales desde el reposo hasta repetidas divisiones, migraciones y, en última instancia, la fusión en nuevo músculo, capturando comportamientos que las instantáneas estáticas podrían pasar por alto.
Cuando las células reparadoras se apresuran y tropiezan
Dentro de músculos lesionados y sanos, las células miogénicas derivadas de células madre se alargaban y se desplazaban a lo largo de las fibras con trayectorias relativamente rectas y dirigidas, dividiéndose y dispersándose de forma eficiente. En cambio, las células distróficas (mdx) a menudo se volvieron redondeadas y lentas. Se movían más despacio y con menos dirección, y una fracción notable permanecía casi inmóvil. El equipo también encontró que las células mdx se fusionaban en nuevas fibras musculares antes de lo normal, y muchas células hijas migraban juntas en lugar de separarse tras la división. En conjunto, los músculos mdx mostraron signos de “diferenciación prematura”: las células madre se apresuraban a convertirse en células musculares y a formar fibras, en lugar de mantener una reserva robusta para la reparación continua.
Divisiones celulares desequilibradas y un vecindario confuso
En fibras aisladas, los investigadores pudieron clasificar cómo se dividía cada célula madre. En músculos sanos, la mayoría de las divisiones eran simétricas pero equilibradas: muchas producían dos hijas proliferativas que podían seguir ampliando la reserva de reparación, y menos producían dos células terminalmente diferenciadas. Las divisiones asimétricas, en las que una hija permanecía como célula madre y la otra se comprometía con la reparación, eran relativamente raras pero estaban presentes. En músculos mdx, el patrón cambió drásticamente: las divisiones simétricas se inclinaron hacia la producción de dos células diferenciadas, con muchas menos divisiones que generaran dos células renovadoras. Experimentos de injerto cruzado, donde células madre sanas se colocaron sobre fibras distróficas y viceversa, mostraron que los defectos de migración estaban dictados en gran medida por el entorno de la fibra dañada, mientras que el comportamiento excesivamente diferenciativo de las células mdx seguía a las propias células, moldeado en parte por su historial inflamatorio.
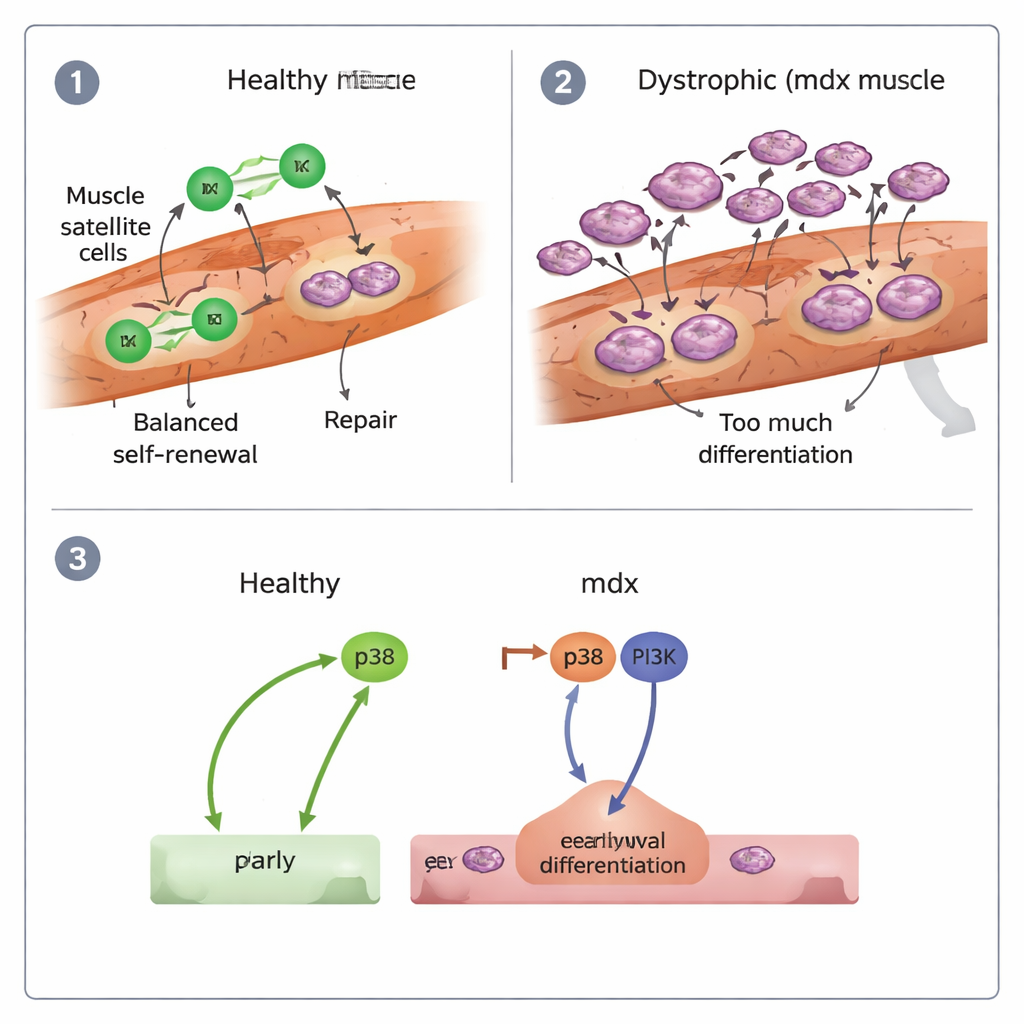
Señales mal conectadas y lo que significa para la terapia
Los autores también examinaron los interruptores moleculares que empujan a las células madre a diferenciarse. Se centraron en dos vías de señalización, conocidas como p38 y PI3K. En células sanas, bloquear p38 reducía fuertemente la diferenciación, mientras que inhibir PI3K tenía poco efecto. En células mdx, sin embargo, fue necesario bloquear ambas vías simultáneamente para frenar la carrera excesiva hacia la especialización, y aun así su capacidad para mantener la proliferación seguía siendo pobre. Esto sugiere que las células madre en la DMD son empujadas a un “agotamiento temprano” por la actividad combinada de p38 y PI3K, lo que contribuye a una regeneración que arranca rápido pero no puede sostenerse.
Una nueva visión de Duchenne: también una enfermedad de las células madre
Para un lector no especializado, el mensaje principal es que la DMD no es solo un problema de fibras musculares frágiles; también es un problema del sistema de reparación destinado a arreglarlas. En el músculo distrófico, las células madre se mueven con menos eficiencia, se dividen de forma que agotan la reserva y responden de manera anormal a señales clave de crecimiento. Al identificar qué aspectos son causados por el entorno muscular dañado y cuáles están integrados en el estado alterado de las propias células madre, este trabajo sugiere nuevas estrategias: terapias que atenúen la señalización p38 y PI3K, restauren divisiones celulares equilibradas o mejoren el nicho local podrían ayudar a reconstruir el músculo con mayor eficacia y ampliar los beneficios de tratamientos génicos o basados en células para personas que viven con la distrofia muscular de Duchenne.
Cita: Sarde, L., Letort, G., Varet, H. et al. Impaired stem cell migration and divisions in Duchenne muscular dystrophy revealed by live imaging. Nat Commun 17, 1769 (2026). https://doi.org/10.1038/s41467-026-68474-5
Palabras clave: Distrofia muscular de Duchenne, células madre musculares, migración celular, división de células madre, medicina regenerativa