Clear Sky Science · es
Sistemas de edición de bases divididos mediada por heterodímeros de coiled-coil permiten sustituciones de nucleótidos flexibles y robustas
Reparar el ADN con menos efectos secundarios
Muchas enfermedades se deben a pequeños errores tipográficos en nuestro ADN: fallos de una sola letra que pueden tener consecuencias potencialmente mortales. Los científicos disponen de herramientas potentes, llamadas editores de bases, que pueden corregir estos errores sin cortar el ADN, pero estas herramientas son voluminosas y difíciles de administrar de forma segura en el organismo. Este artículo presenta una nueva forma de dividir los editores de bases en piezas más pequeñas e inteligentes que siguen funcionando igual de bien —o incluso mejor— que el original, abriendo nuevas vías para tratar enfermedades genéticas en el hígado, los músculos y otros tejidos.
Por qué el tamaño es un problema para las herramientas de corrección génica
Los editores de bases combinan partes del sistema CRISPR con enzimas que pueden intercambiar una letra del ADN por otra, como cambiar una A por una G o una C por una T. Estos intercambios precisos son prometedores para tratar afecciones como el colesterol alto o la distrofia muscular. Sin embargo, un vehículo de entrega líder en terapia génica, el virus adenoasociado (AAV), solo puede transportar unas 4,7 mil bases de ADN, mientras que los editores de bases estándar son más grandes. Trabajos anteriores intentaron dividir estos editores usando “tijeras” proteicas especiales llamadas inteínas, o reduciéndolos con enzimas miniatura, pero estos enfoques a menudo reducían la eficiencia, añadían complejidad de diseño o limitaban dónde en el genoma podían actuar las herramientas.
Usar Velcro molecular para reconstruir el editor
Para resolver esto, los investigadores diseñaron un editor de bases “dividido” que se mantiene unido mediante pequeños cierres proteicos en espiral conocidos como heterodímeros de coiled-coil —como un Velcro molecular. Separaron el editor de bases en dos partes: una que lleva la Cas9 nickasa para dirigir al ADN y otra que porta la enzima editora. Péptidos cortos de coiled-coil en cada mitad se buscan entre sí y se ensamblan cuando ambas mitades llegan al mismo tramo de ADN. Esto crea editores de bases con coiled-coil (CC‑BEs), incluidos tipos que editan C (CC‑CBE), A (CC‑ABE), y variantes más complejas que pueden realizar distintos tipos de cambios de letra. 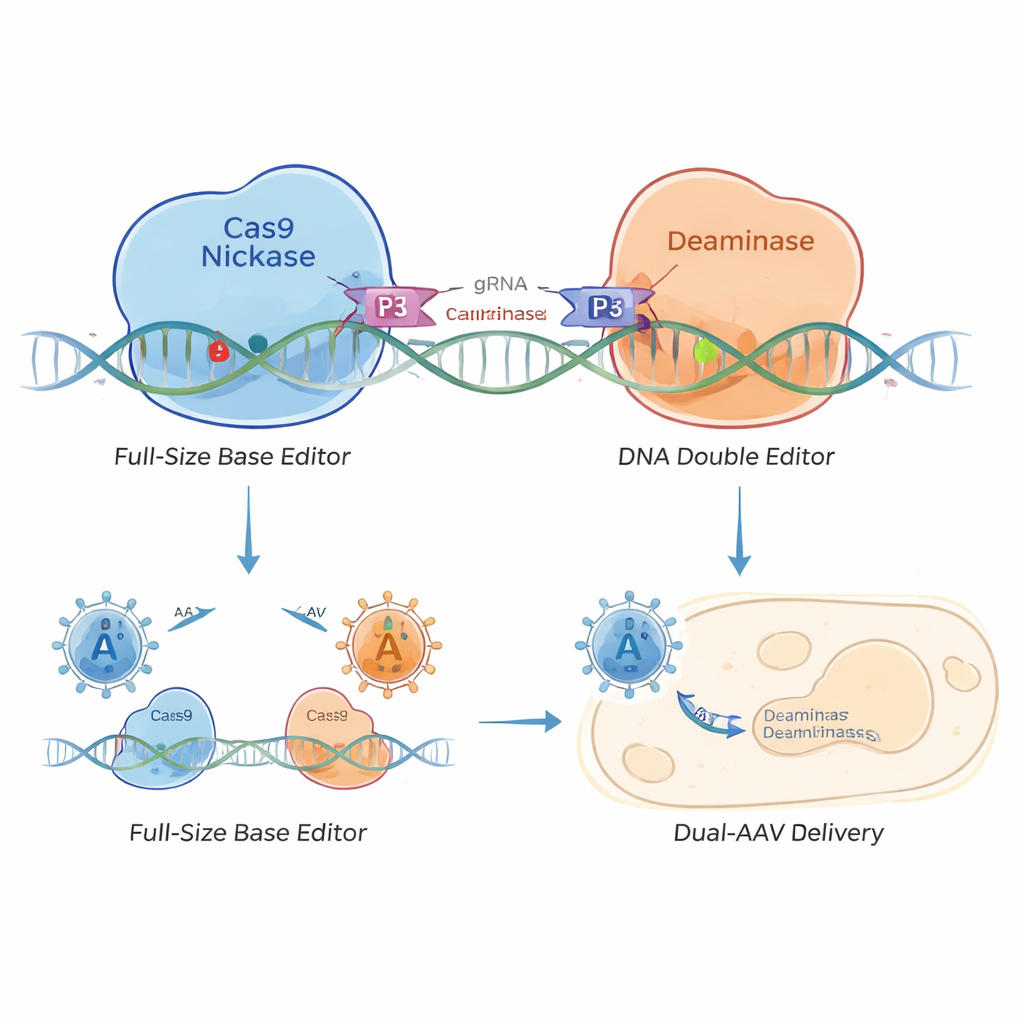
Edición flexible, potente y precisa
El equipo probó los CC‑BEs en varios tipos celulares, incluidas células humanas y células primarias de cerdo, y con diferentes formas de Cas9 que reconocen una gama más amplia de secuencias de ADN. Las versiones CC‑CBE no solo funcionaron de forma fiable en muchos sitios, sino que también mostraron una “ventana de edición” más amplia, lo que significa que podían cambiar letras objetivo a lo largo de un tramo más extenso de ADN, dando a los científicos más flexibilidad al elegir ARN guías. Las versiones CC‑ABE alcanzaron una eficiencia similar a la de los mejores editores de adenina existentes, produciendo a menudo menos subproductos fuera de objetivo. Los investigadores también adaptaron la estrategia de coiled‑coil a diseños de editores más nuevos —como TadCBE compacto y ABE9 preciso— y nuevamente encontraron que dividir las herramientas con pares de coiled‑coil preservaba o mejoraba el rendimiento.
De cultivos celulares a ratones vivos
De forma crucial, los autores demostraron que estos editores divididos funcionan dentro de animales vivos mediante entrega dual por AAV, donde cada partícula viral transporta la mitad del editor. En ratones, un CC‑ABE dirigido al gen Pcsk9 en el hígado logró ediciones de A a G en tasas de hasta aproximadamente el 70%, reduciendo drásticamente la proteína Pcsk9 y el colesterol LDL en sangre sin signos de daño hepático. 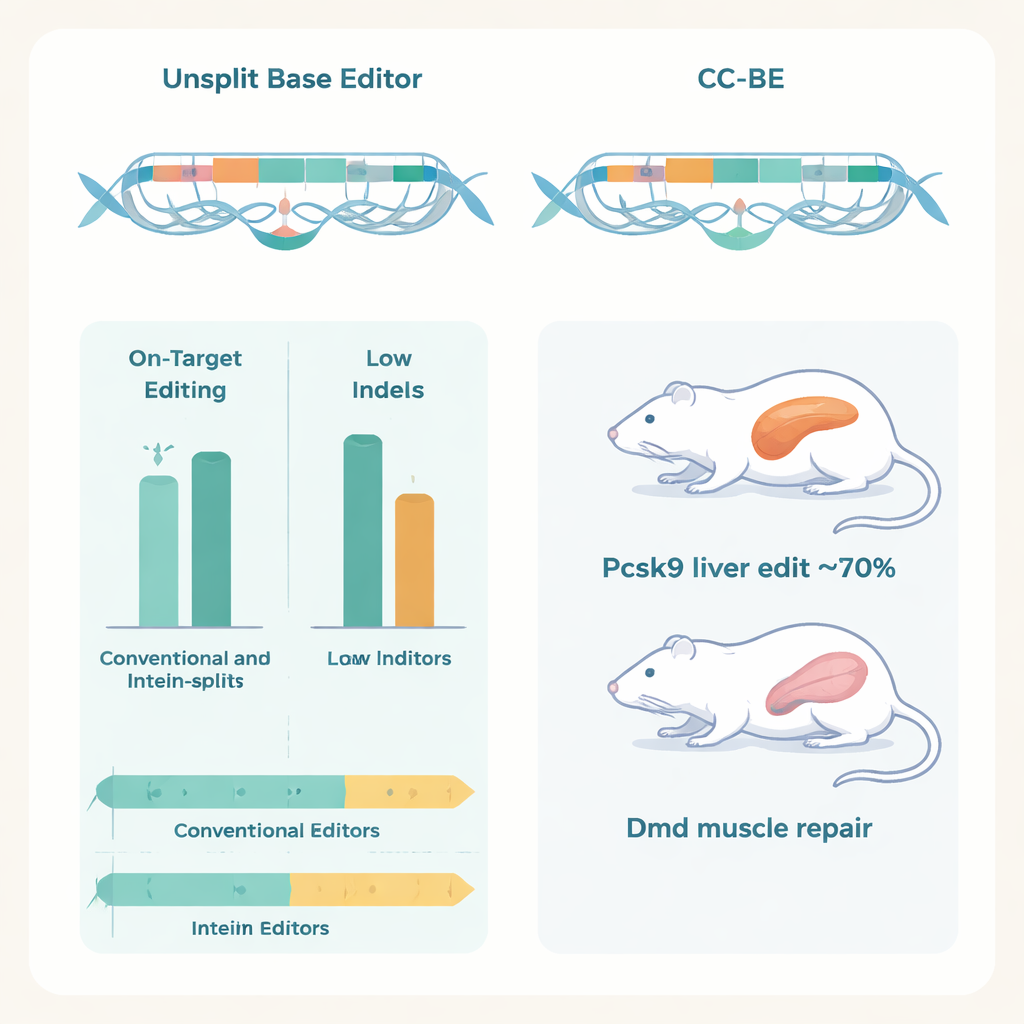
Un nuevo camino hacia la reparación práctica del ADN
En esencia, este estudio presenta un truco de ingeniería sencillo pero potente: usar pequeños “ganchos” de coiled‑coil para dividir grandes editores de bases en módulos del tamaño permitido por AAV que se reúnen solo donde se necesitan. Para el público general, la conclusión es que los científicos pueden ahora empaquetar herramientas de reparación del ADN muy capaces en vectores virales clínicamente probados sin sacrificar precisión ni potencia. Este enfoque de coiled‑coil podría facilitar el diseño de tratamientos para una amplia gama de enfermedades genéticas de una sola letra en órganos como el hígado, el corazón y el músculo, acercando la corrección génica fina un paso más a terapias del mundo real.
Cita: Mu, S., Li, Q., Chen, M. et al. Coiled-coil heterodimer-mediated split base editing systems enable flexible and robust nucleotide substitutions. Nat Commun 17, 1765 (2026). https://doi.org/10.1038/s41467-026-68469-2
Palabras clave: edición de bases, terapia génica, CRISPR, entrega por AAV, enfermedad genética