Clear Sky Science · es
La impronta dependiente de H3K27me3 y la regulación transcripcional en embriones tempranos de ratón requieren la restricción de la actividad de PRC2 mediada por EZHIP
Por qué los embriones diminutos necesitan una sincronía genética cuidadosa
Cualquier mamífero comienza la vida como una sola célula que lleva un juego de cromosomas de la madre y otro del padre. Aunque estos dos paquetes genéticos contienen casi las mismas letras del ADN, llegan envueltos en distintas marcas químicas que ayudan a decidir qué genes se encienden o se apagan. Este estudio explora cómo se mantiene equilibrado uno de esos sistemas de marcado durante los primeros días tras la fertilización en ratones, y por qué alterar ese equilibrio puede descarrilar el desarrollo normal.
Dos progenitores, dos genomas empaquetados de forma distinta
En los mamíferos, ciertos genes se comportan de forma distinta según provengan de la madre o del padre, un fenómeno llamado impronta genómica. La impronta clásica depende de marcas químicas sobre el propio ADN, pero en años recientes los científicos descubrieron un segundo tipo, más efímero, que depende de una modificación de las histonas llamada H3K27me3. Estas histonas actúan como carretes alrededor de los cuales se enrolla el ADN, y H3K27me3 tiende a silenciar genes cercanos. En embriones normales de ratón, el genoma materno lleva más de esta marca que el paterno justo después de la fertilización, ayudando a silenciar copias genéticas maternas específicas mientras permite que las copias paternas funcionen.
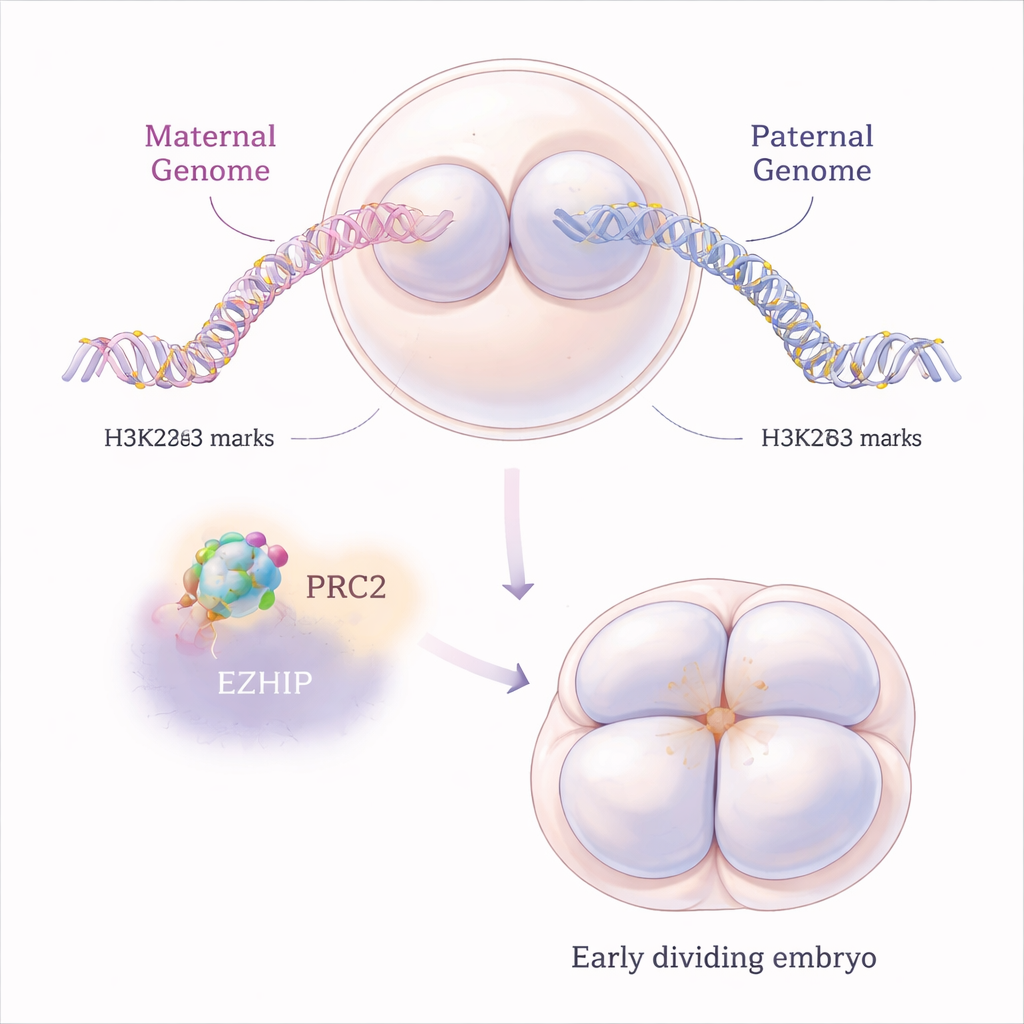
Un freno molecular sobre un represor potente
H3K27me3 se coloca sobre la cromatina mediante una gran máquina proteica llamada PRC2. Los autores se centraron en EZHIP, una proteína menos conocida que se une a PRC2 y lo ralentiza. Los ovocitos de ratón producen mucho ARN de Ezhip, y la proteína EZHIP resultante perdura en los embriones durante las primeras divisiones celulares. Estudiando ratones cuyas madres carecían de Ezhip, los investigadores preguntaron qué ocurre cuando se elimina este freno natural. Encontraron que, sin EZHIP, los óvulos y embriones tempranos acumulaban marcas adicionales de H3K27me3, pero de una forma sorprendentemente “aplanada”: en lugar de dominios nítidos y bien definidos, la marca represora se extendía de manera más amplia y difuminaba los patrones normales, afectando tanto a los cromosomas maternos como a los paternos.
Cuando demasiada represión rompe la impronta
Utilizando métodos sensibles de cartografía del genoma, el equipo mostró que la asimetría habitual entre los paisajes de H3K27me3 materno y paterno se pierde en gran medida en embriones que se desarrollan a partir de óvulos deficientes en Ezhip. Muchas regiones que normalmente mantienen H3K27me3 en una sola copia parental la adquirieron en ambas, o vieron sus patrones difusos. Este cambio tuvo consecuencias importantes para genes imprintados que normalmente están controlados por H3K27me3 en lugar de por metilación del ADN. En embriones control, estos genes tienden a expresarse mayoritariamente desde el alelo paterno. En embriones que carecían de EZHIP materno, sin embargo, los mismos genes con frecuencia se activaron desde ambas copias parentales, y los niveles totales de ARN de muchos de ellos aumentaron en lugar de estar doblemente silenciados.
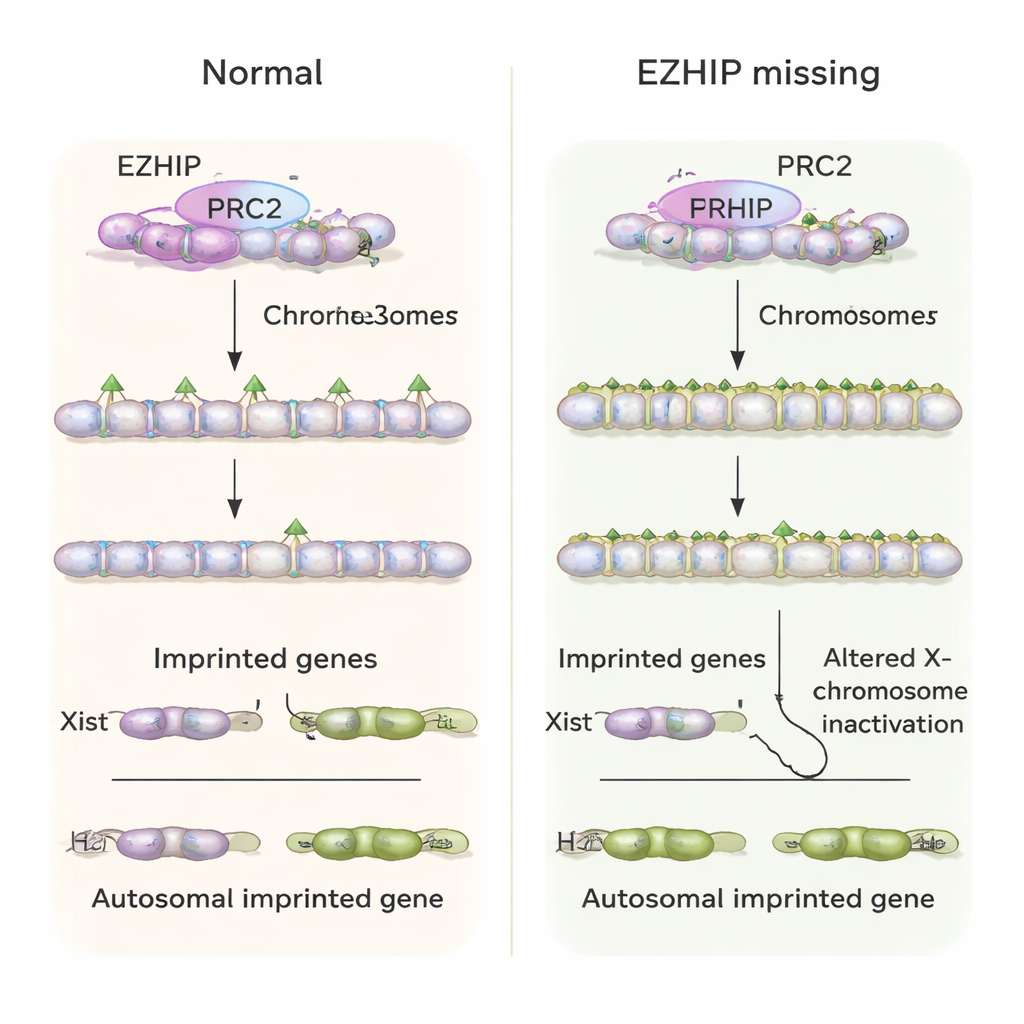
Control del cromosoma X alterado y salud del embrión
Un gen imprintado clave dependiente de H3K27me3 es Xist, un ARN largo que recubre e inactiva un cromosoma X en células femeninas para equilibrar la dosis génica con los machos. Normalmente, los embriones tempranos de ratón expresan Xist solo desde el X paterno en hembras, y nada en machos. En ausencia de EZHIP materno, los autores observaron que las hembras con frecuencia expresaban Xist desde ambos cromosomas X, mientras que los machos “inapropiadamente” activaban Xist desde su único X. Esto condujo a patrones anómalos de inactivación de genes ligados al X. A nivel del organismo, nacieron menos ratones de madres deficientes en Ezhip, y los embriones mostraron crecimiento alterado y problemas en tejidos extraembrionarios que sostienen la placenta, coherente con un estrés del desarrollo de larga duración causado por la falla de la impronta temprana.
Demasiado de algo bueno puede ser dañino
Para un no especialista podría parecer intuitivo que más de una marca silenciosa como H3K27me3 simplemente acallaría más genes. En cambio, este trabajo muestra que sobrecargar el genoma con tales marcas en un patrón incorrecto puede socavar su capacidad para actuar como interruptores precisos. Al eliminar EZHIP, los investigadores desataron a PRC2, provocando que H3K27me3 se difundiera tan ampliamente que las señales de impronta se difuminaron y reguladores críticos como Xist quedaron mal controlados. El estudio subraya que los embriones tempranos dependen no solo de tener las moléculas adecuadas, sino de mantener sus actividades finamente ajustadas para que los genomas materno y paterno se lean en el balance correcto.
Cita: Diop, S., Richart, L., Petitalot, A. et al. H3K27me3-dependent imprinting and transcriptional regulation in early mouse embryos requires EZHIP-mediated restriction of PRC2 activity. Nat Commun 17, 1758 (2026). https://doi.org/10.1038/s41467-026-68467-4
Palabras clave: epigenética, impronta genómica, desarrollo embrionario temprano, inactivación del cromosoma X, Policomb PRC2