Clear Sky Science · es
Aprovechar la inmunidad entrenada inducida por glucanos para el reprogramado epigenético y metabólico de macrófagos para mejorar la respuesta a vacunas contra el cáncer colorrectal
Reavivando a los primeros intervinientes del cuerpo
El cáncer colorrectal es uno de los tipos de cáncer más mortales del mundo, y la mayoría de los pacientes no se benefician de las inmunoterapias disponibles hoy. Este estudio explora una idea intrigante: ¿y si pudiéramos “entrenar” al sistema inmunitario innato —los primeros intervinientes del organismo— para que recuerde el peligro y ayude a que las vacunas funcionen mejor contra los tumores colorrectales? Usando un azúcar natural procedente de la levadura, llamado beta‑glucano, los investigadores muestran cómo las células inmunitarias tempranas pueden ser reprogramadas de modo que las vacunas contra el cáncer desencadenen ataques más fuertes y duraderos contra los tumores.
Por qué el cáncer colorrectal necesita nuevas defensas
El cáncer colorrectal provoca cerca de un millón de muertes al año en todo el mundo, y los casos en adultos jóvenes están aumentando. Los tratamientos estándar como la cirugía, la quimioterapia y la radioterapia pueden ser efectivos, pero muchos pacientes recaen y sufren efectos secundarios graves. Los fármacos inmunológicos más recientes, como los inhibidores de puntos de control, funcionan muy bien solo en un pequeño subconjunto de cánceres colorrectales que presentan defectos específicos en la reparación del ADN. Para la mayoría de los pacientes, estos fármacos e incluso las vacunas experimentales contra el cáncer se quedan cortos porque el microentorno tumoral está dominado por células y señales que suprimen el ataque inmunitario.
Enseñar nuevas habilidades a la inmunidad innata
Las células inmunitarias innatas del cuerpo —especialmente los macrófagos— normalmente reaccionan con rapidez pero de forma breve ante las amenazas y se pensaba que carecían de memoria. Sin embargo, trabajos de la última década han revelado la «inmunidad entrenada», en la que un estímulo inicial intenso deja marcas duraderas en estas células, permitiéndoles responder con mayor vigor más adelante. Los autores usaron beta‑glucano, un componente de las paredes celulares de la levadura, para inducir este estado entrenado. En ratones, un tratamiento breve con partículas enteras de beta‑glucano reprogramó a los macrófagos tanto a nivel de la actividad génica como del metabolismo celular. Cuando estos animales entrenados recibieron después una vacuna contra el cáncer colorrectal basada en un adenovirus diseñado (llamada PeptiCrad), sus sistemas inmunitarios produjeron linfocitos T citotóxicos más potentes, mejores en reconocer y atacar dianas específicas del tumor. 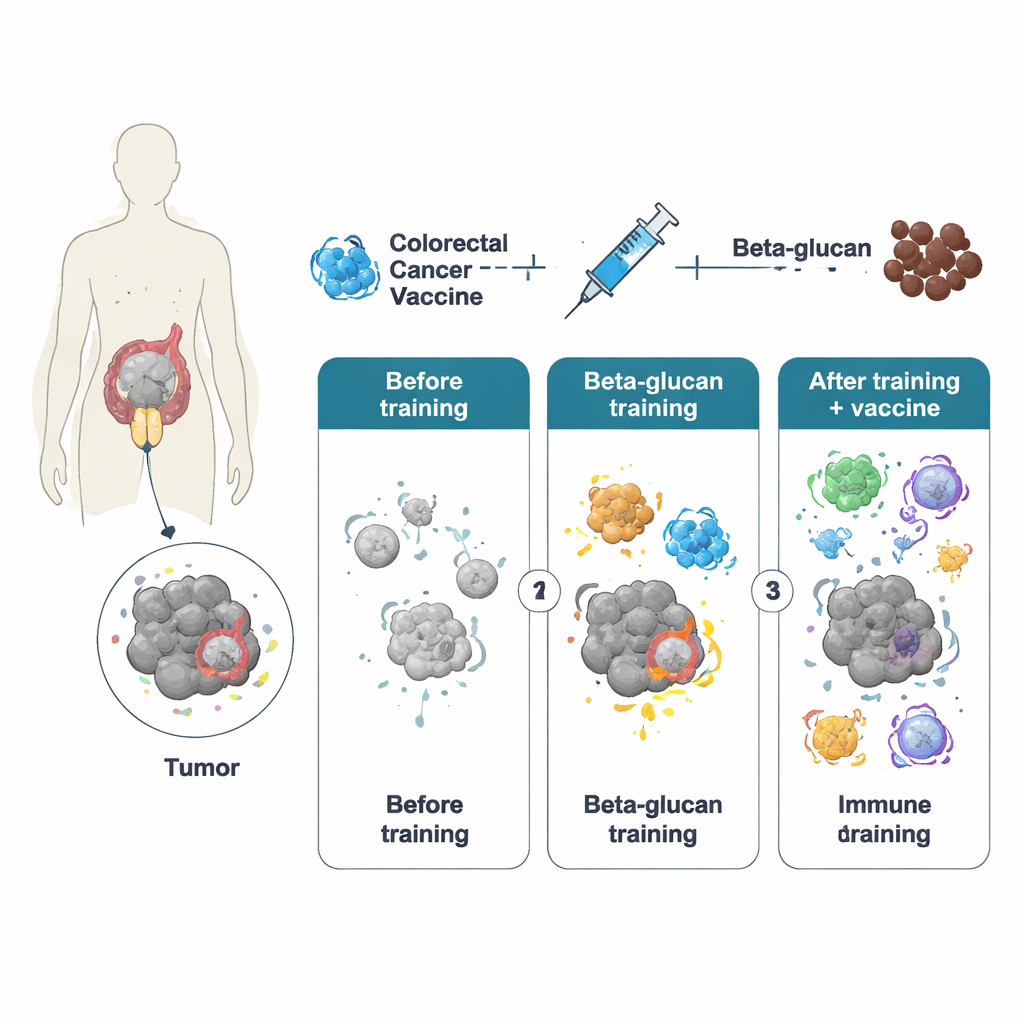
Reconfigurar la energía y la comunicación dentro de los tumores
Indagando más, los investigadores aislaron células inmunitarias de los tumores y analizaron su metabolismo y actividad génica una por una. Encontraron que los macrófagos entrenados cambiaron a un modo metabólico de alta intensidad que recuerda al «efecto Warburg», en el que las células consumen azúcar rápidamente y desvían recursos hacia bloques constructores para crecimiento y función. Estas células también aumentaron el metabolismo de la creatina —más conocido por los suplementos deportivos—, lo que ayudó a suministrar la energía extra necesaria para producir moléculas inflamatorias. Al mismo tiempo, etiquetas químicas específicas en las proteínas asociadas al ADN (notablemente un aumento de H3K4me3) marcaron genes implicados en la producción de quimiocinas, consolidando efectivamente un programa proinflamatorio y antitumoral que persistió en el tiempo.
Construyendo un equipo de relevos inmunitario
La secuenciación a nivel de célula única reveló un relevo escalonado entre diferentes células inmunitarias dentro del tumor. Primero, los macrófagos entrenados liberaron altos niveles de dos señales clave, CXCL9 y CXCL10, que atrajeron a células asesinas naturales (NK) a través de un receptor llamado CXCR3. Una vez reclutadas, estas células NK no solo mataron células cancerosas; también secretaron otro mensajero, CCL5, que atrajo a un subconjunto especializado de células dendríticas conocido como cDC1. Estas células dendríticas son excelentes presentadoras de fragmentos tumorales a los linfocitos T. Como resultado, más células T CD8 se activaron y se convirtieron en células de memoria efectora —células que responden de forma rápida y robusta cuando vuelven a encontrar el tumor. Bloquear el uso de creatina, agotar macrófagos o células NK, o interrumpir estas vías de quimiocinas debilitó el control tumoral, subrayando cuánto dependía el éxito de la vacuna de este circuito macrófago–NK–dendrítica–T. 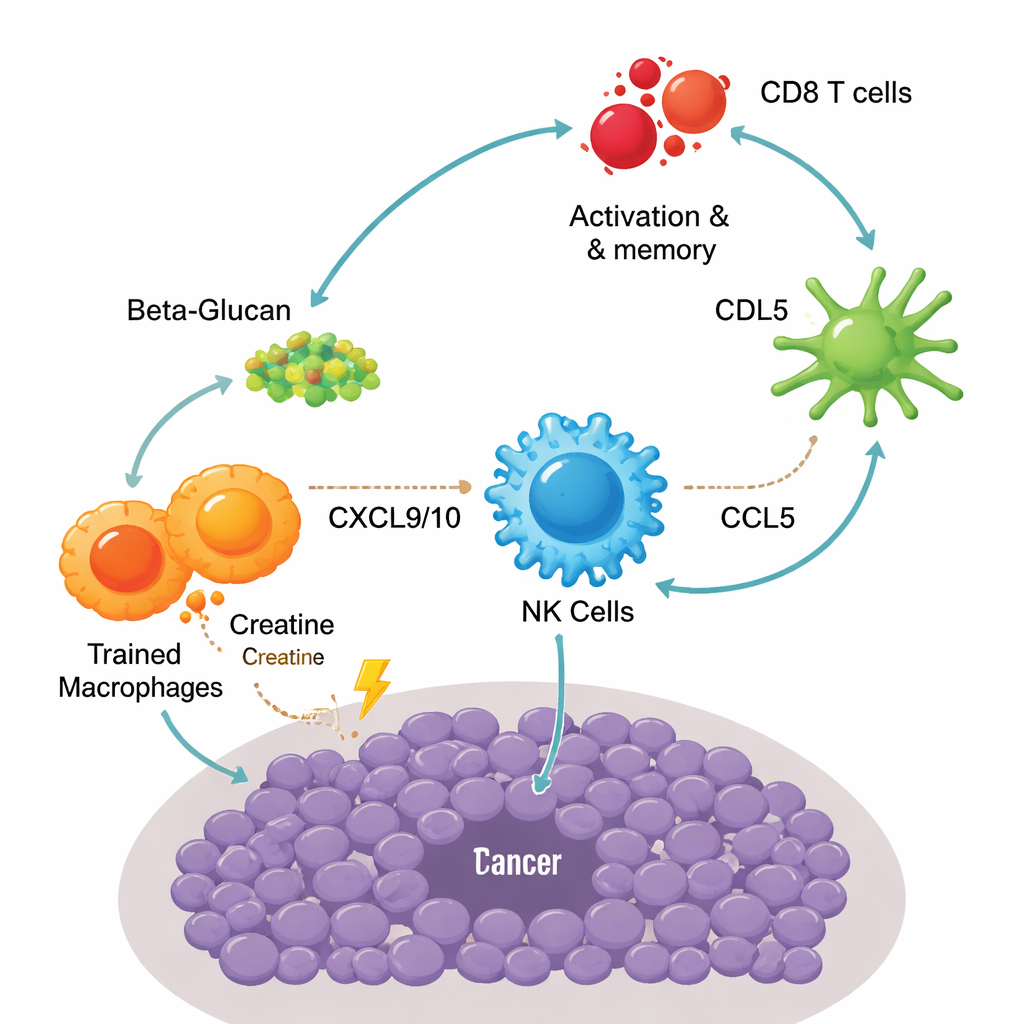
De modelos en ratón a organoides tumorales humanos
El equipo probó su enfoque en varios modelos murinos de cáncer colorrectal, incluido un tipo particularmente resistente a las inmunoterapias comunes. En cada caso, la combinación de entrenamiento con beta‑glucano y la vacuna ralentizó el crecimiento tumoral más eficazmente que cualquiera de los tratamientos por separado. Importante, también fueron más allá de los ratones. Las células sanguíneas humanas expuestas al beta‑glucano mejoraron su respuesta a un péptido de vacuna contra el cáncer colorrectal, produciendo más citocinas estimuladoras del sistema inmunitario. Cuando estas células inmunitarias entrenadas fueron ampliadas y cocultivadas con mini‑tumores colorrectales derivados de pacientes (organoides), eliminaron más células cancerosas que las células no entrenadas. Quitar los monocitos y macrófagos humanos del sistema borró este beneficio, confirmando que estas células entrenadas son organizadoras esenciales más que asesinas tumorales directas.
Lo que esto podría significar para futuras vacunas contra el cáncer
En términos sencillos, este trabajo muestra que un azúcar seguro derivado de la levadura puede «entrenar» a las células inmunitarias innatas para apoyar una vacunación más eficaz contra el cáncer colorrectal. Al reprogramar cómo los macrófagos usan la energía y qué genes mantienen listos para actuar, el entrenamiento con beta‑glucano desencadena un efecto dominó: los macrófagos llaman a las células NK, las NK reclutan a dendríticas expertas y, juntos, construyen un ejército más fuerte de células T CD8 de memoria. Aunque queda mucho por probar en ensayos clínicos —incluyendo seguridad, sincronización y las mejores combinaciones de vacunas— la inmunidad entrenada surge aquí como una estrategia adyuvante prometedora para convertir tumores colorrectales más fríos y supresores en otros que el sistema inmunitario pueda reconocer y controlar.
Cita: Hamdan, F., Gandolfi, S., D’Alessio, F. et al. Leveraging glucan-induced trained immunity for the epigenetic and metabolic rewiring of macrophages to enhance colorectal cancer vaccine response. Nat Commun 17, 1757 (2026). https://doi.org/10.1038/s41467-026-68466-5
Palabras clave: inmunoterapia del cáncer colorrectal, inmunidad entrenada, beta-glucano, macrófagos y células NK, vacunas contra el cáncer