Clear Sky Science · es
Cribado CRISPR in vivo identifica miembros del complejo SAGA como reguladores clave de la hematopoyesis
Por qué es importante mantener el equilibrio en la producción de sangre
Cada día, tu cuerpo fabrica silenciosamente cientos de miles de millones de células sanguíneas nuevas que transportan oxígeno, combaten infecciones y detienen las hemorragias. Esta producción constante depende de unas raras «células madre» en la médula ósea, llamadas células madre formadoras de sangre. Cuando la maquinaria que controla estas células falla, las personas pueden desarrollar anemia, inmunidad debilitada o cánceres como la leucemia. Este estudio plantea una pregunta simple pero potente: entre los miles de genes de nuestro genoma, ¿cuáles son realmente esenciales para mantener la producción de células sanguíneas sana y equilibrada?
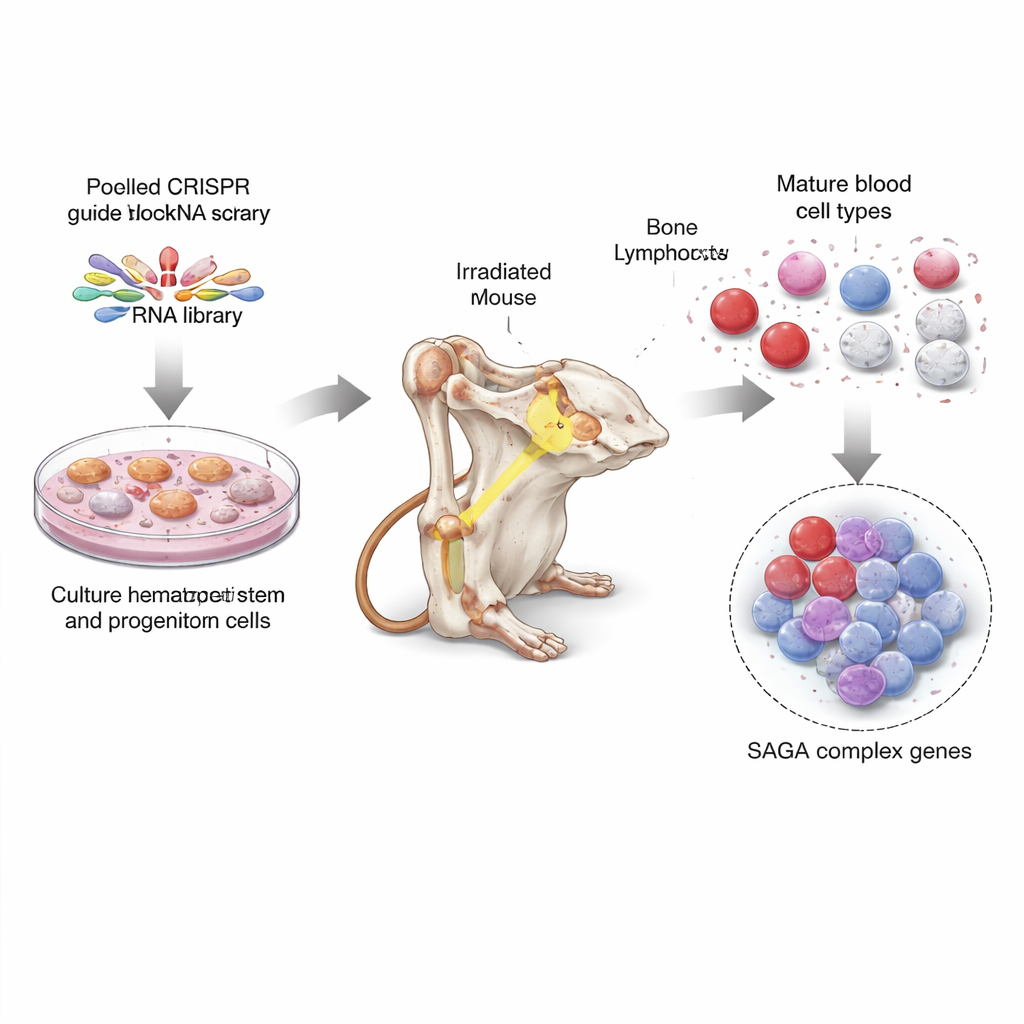
Una búsqueda del tesoro a escala genómica en células madre de ratón
Para abordar esto, los investigadores utilizaron CRISPR, la herramienta de edición genética a menudo comparada con tijeras moleculares, para apagar casi todos los genes del genoma de ratón, con diez guías por gen. Primero cultivaron grandes cantidades de células madre y progenitoras de médula ósea en condiciones de cultivo especiales, y luego infectaron estas células con una mezcla de guías CRISPR para que cada célula llevara la eliminación de un gen distinto. A continuación, trasplantaron estas células mezcladas y editadas a decenas de ratones irradiados, permitiendo que las células editadas reconstruyeran los sistemas sanguíneos de los animales. Meses después, purificaron varios tipos de células sanguíneas maduras y células con apariencia de madre de la médula ósea y analizaron qué guías CRISPR estaban sobrerrepresentadas o infrarrepresentadas. Esto reveló qué pérdidas génicas favorecían a las células inmaduras y cuáles apoyaban la producción de células sanguíneas completamente formadas.
Un centro de control oculto llamado SAGA sale a la luz
Entre muchos reguladores conocidos de la formación sanguínea surgió un conjunto sorprendente de candidatos: varias piezas estructurales de un gran ensamblaje proteico llamado complejo SAGA, incluidos genes denominados Tada2b, Taf5l y Tada1. SAGA no fabrica células sanguíneas directamente; en cambio, ayuda a encender o apagar otros genes marcando químicamente las proteínas que empaquetan el ADN, llamadas histonas. Cuando el equipo desactivó individualmente estos componentes de SAGA y trasplantó las células editadas a ratones, observaron un patrón consistente. Se acumularon células inmaduras de la médula ósea, pero su capacidad para madurar en glóbulos blancos circulantes, glóbulos rojos y ciertos tipos de células inmunitarias se redujo drásticamente. En esencia, las células madre y progenitoras quedaron atrapadas en un cuello de botella, incapaces de completar el trayecto hasta convertirse en células sanguíneas plenamente funcionales.
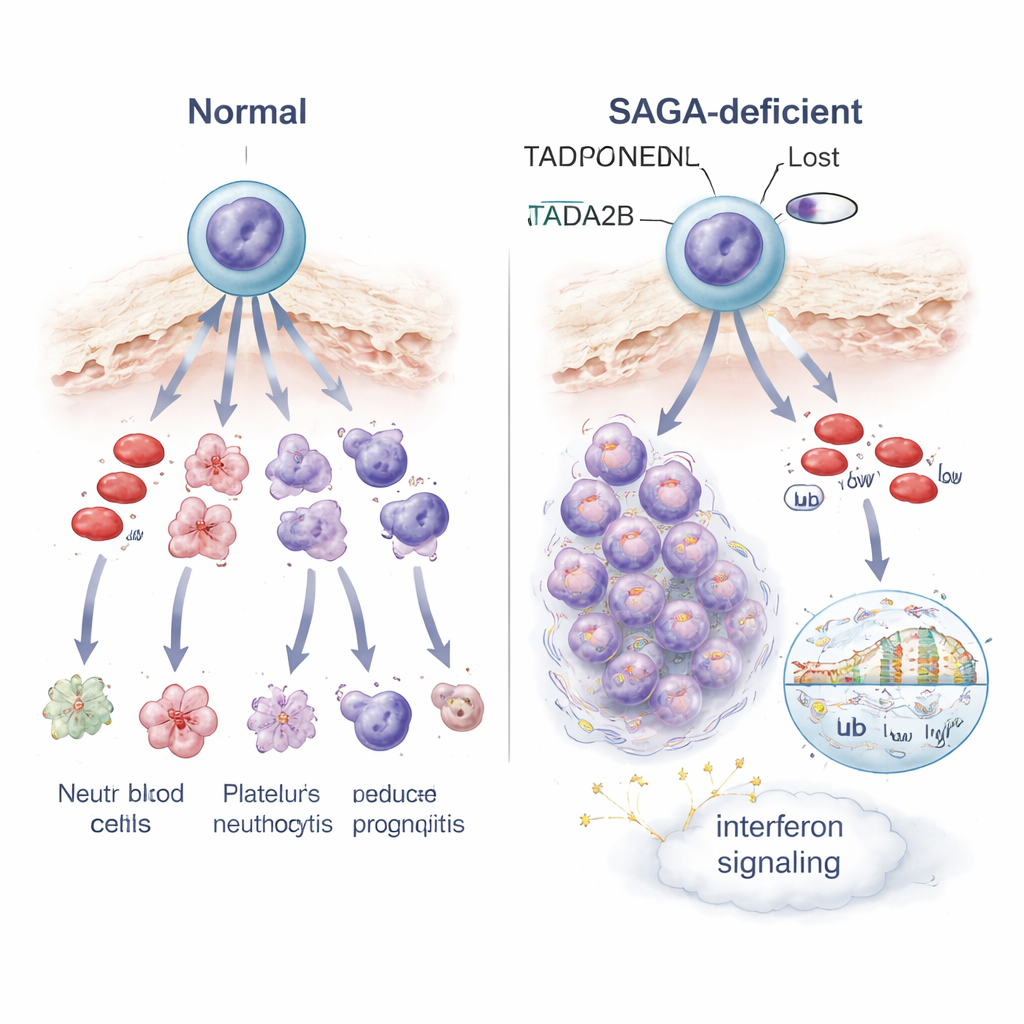
Cómo la alteración del control génico cambia el destino celular y las señales de estrés
Para entender qué falla dentro de estas células bloqueadas, los científicos perfilizaron la actividad génica célula por célula y en conjunto. La pérdida de Tada2b o Taf5l reconfiguró la actividad de muchos genes en las células madre, con dos temas llamativos. Primero, los genes implicados en la señalización por interferón —normalmente parte de la defensa antiviral del organismo— se activaron, indicando una alarma interna o estado de estrés. Segundo, las mitocondrias de las células, las pequeñas centrales energéticas que impulsan el trabajo celular, se volvieron menos activas y las células alteradas mostraron mayor sensibilidad a un fármaco que apunta a la producción de energía mitocondrial. A nivel del empaquetamiento del ADN, las células carentes de Tada2b mostraron niveles reducidos de una marca de histona asociada a cromatina abierta y activa, y cambios en otra marca vinculada a cómo se lee la información genética. Estos cambios en la química de la cromatina probablemente ayudan a explicar por qué muchos genes, incluidos los que guían la maduración adecuada de la sangre, quedan desregulados.
De los mecanismos básicos a modelos de enfermedad
El equipo preguntó luego si modular la actividad de SAGA hacia arriba o hacia abajo podía revertir estos efectos. Forzar a las células a producir Tada2b adicional redujo la actividad de genes relacionados con interferón y disminuyó la proporción de células con rasgos de progenitor, la imagen especular de la eliminación génica. Tratar células madre normales con un fármaco que inhibe las subunidades enzimáticas clave de SAGA reprodujo gran parte de la firma asociada a la pérdida de Tada2b, reforzando la idea de que la actividad modificadora de la cromatina de SAGA es central para su función. Finalmente, los investigadores recurrieron a un modelo celular humano de síndrome mielodisplásico, un trastorno preleucémico en el que la producción de sangre falla y las vías de interferón suelen estar elevadas. Cuando eliminaron componentes de SAGA en estas células humanas y las trasplantaron en ratones inmunodeficientes, las células editadas obtuvieron una ventaja de crecimiento y de nuevo activaron programas génicos de interferón y mieloides, lo que sugiere que este centro regulador también influye en el comportamiento de la enfermedad.
Lo que esto significa para la salud sanguínea y futuras terapias
Para un lector general, el mensaje central es que este estudio revela un potente centro de control —el complejo SAGA— que ayuda a las células madre formadoras de sangre a decidir cuándo permanecer inmaduras, cuándo madurar y cómo evitar respuestas de estrés perjudiciales. Cuando faltan partes clave de SAGA, las células madre se acumulan pero no producen suficientes células sanguíneas funcionales, mientras aumentan las señales de estrés y estilo antiviral y las mitocondrias fallan. Estos hallazgos no solo profundizan nuestra comprensión de cómo se mantiene la producción sanguínea sana a lo largo de la vida, sino que también sugieren que cambios sutiles en la actividad de SAGA podrían contribuir a problemas sanguíneos relacionados con la edad y a trastornos como el síndrome mielodisplásico. A largo plazo, cartografiar este circuito de control podría ayudar a los científicos a diseñar terapias que empujen a las células madre defectuosas de vuelta hacia una producción sanguínea equilibrada y resiliente.
Cita: Shankar, A., Olender, L., Hsu, I. et al. In vivo CRISPR screening identifies SAGA complex members as key regulators of hematopoiesis. Nat Commun 17, 1756 (2026). https://doi.org/10.1038/s41467-026-68465-6
Palabras clave: células madre hematopoyéticas, cribado CRISPR, complejo SAGA, señalización por interferón, síndrome mielodisplásico