Clear Sky Science · es
Inferir la arquitectura de la cromatina en un solo locus mediante localización probabilística in situ del ADN
Cómo la forma 3D del ADN controla cuándo se activan los genes
Nuestro ADN suele representarse como una escalera recta, pero dentro de las células se pliega en bucles y enrollamientos intrincados. Estas formas importan: ayudan a decidir qué genes se activan, cuándo y dónde. Este estudio presenta una nueva forma de observar las pequeñas disposiciones tridimensionales del ADN alrededor de un solo gen en embriones de mosca de la fruta en desarrollo, revelando cómo cambios sutiles en el plegamiento del ADN pueden alterar los patrones de actividad génica que moldean el plan corporal.
Viendo el control génico en un embrión en desarrollo
A medida que un embrión se desarrolla, miles de genes deben encenderse y apagarse en los momentos adecuados. Muchas de estas decisiones las toman tramos cortos de ADN llamados potenciadores, que pueden situarse a decenas de miles de bases del gen que regulan. Para funcionar, los potenciadores deben acercarse físicamente a su gen objetivo en el espacio 3D, formando bucles que permiten que sitios distantes se toquen. Pero estos bucles son diminutos, dinámicos y difíciles de ver. Los autores se centraron en un solo gen, brinker (brk), en la mosca Drosophila. Este gen ayuda a pautar el embrión temprano, activándose en una franja a lo largo del costado del huevo. Tres elementos reguladores cercanos—dos potenciadores (E1 y E2) y un elemento promotor-proximal (PPE) junto al gen—cooperan para producir este patrón preciso.
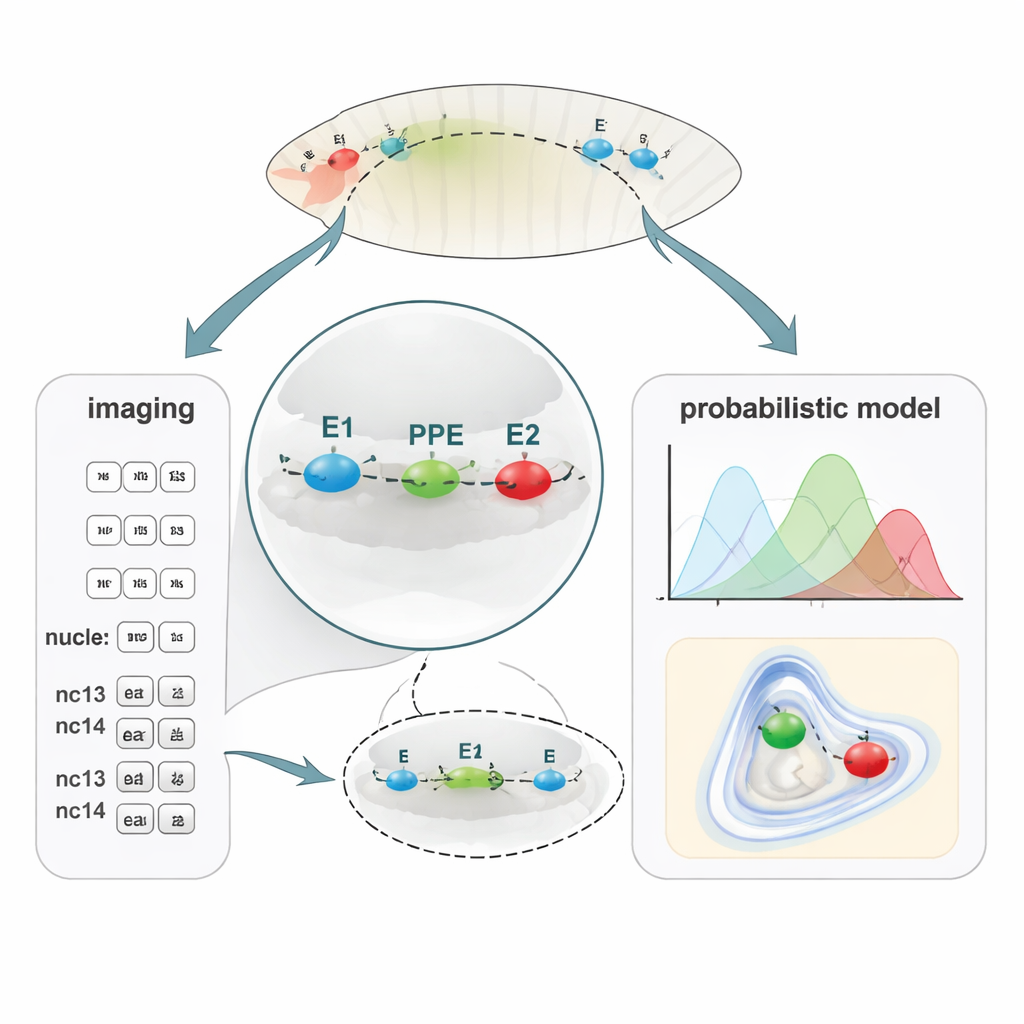
Una nueva forma de cartografiar distancias diminutas del ADN
Para vincular el plegamiento del ADN con la actividad génica, el equipo desarrolló PLOTTED (Localización Probabilística de Distancias entre Elementos Etiquetados con Oligopaint). Primero, usaron un método de marcado del ADN llamado Oligopaint FISH para unir tres tintes fluorescentes distintos a las regiones E1, PPE y E2 en embriones de mosca fijados. Con un microscopio confocal de superresolución, midieron distancias 3D entre estas tres manchas coloreadas en decenas de miles de núcleos a lo largo de embriones en ciclos nucleares sucesivos, desde justo antes de que comience la actividad génica (pre-nc13) hasta etapas posteriores (nc13 y nc14). Luego introdujeron todas estas distancias en una canalización computacional personalizada que filtra mediciones ruidosas y construye mapas de probabilidad que muestran dónde es más probable que se sitúe cada elemento respecto a los demás. En lugar de un único “bucle” estático, PLOTTED produce un paisaje de formas de cromatina probables en cada etapa del desarrollo.
Cuando el ADN se compacta, el gen se activa
En embriones normales, los investigadores encontraron que al llegar al ciclo nuclear 13, ambos potenciadores se acercan al PPE: el vecindario local del ADN alrededor del gen brk se vuelve más compacto. Tras este punto, las distancias entre los tres elementos permanecen relativamente estables. De forma importante, ese momento coincide con el inicio de la expresión de brk, lo que sugiere que el apretamiento de la configuración del ADN ayuda a permitir que el gen se active. PLOTTED también reveló que esta disposición compacta aparece con más frecuencia en las regiones del embrión donde brk está activo, y que configuraciones más sueltas dominan donde el gen está reprimido, reforzando el vínculo entre la arquitectura 3D y la transcripción.
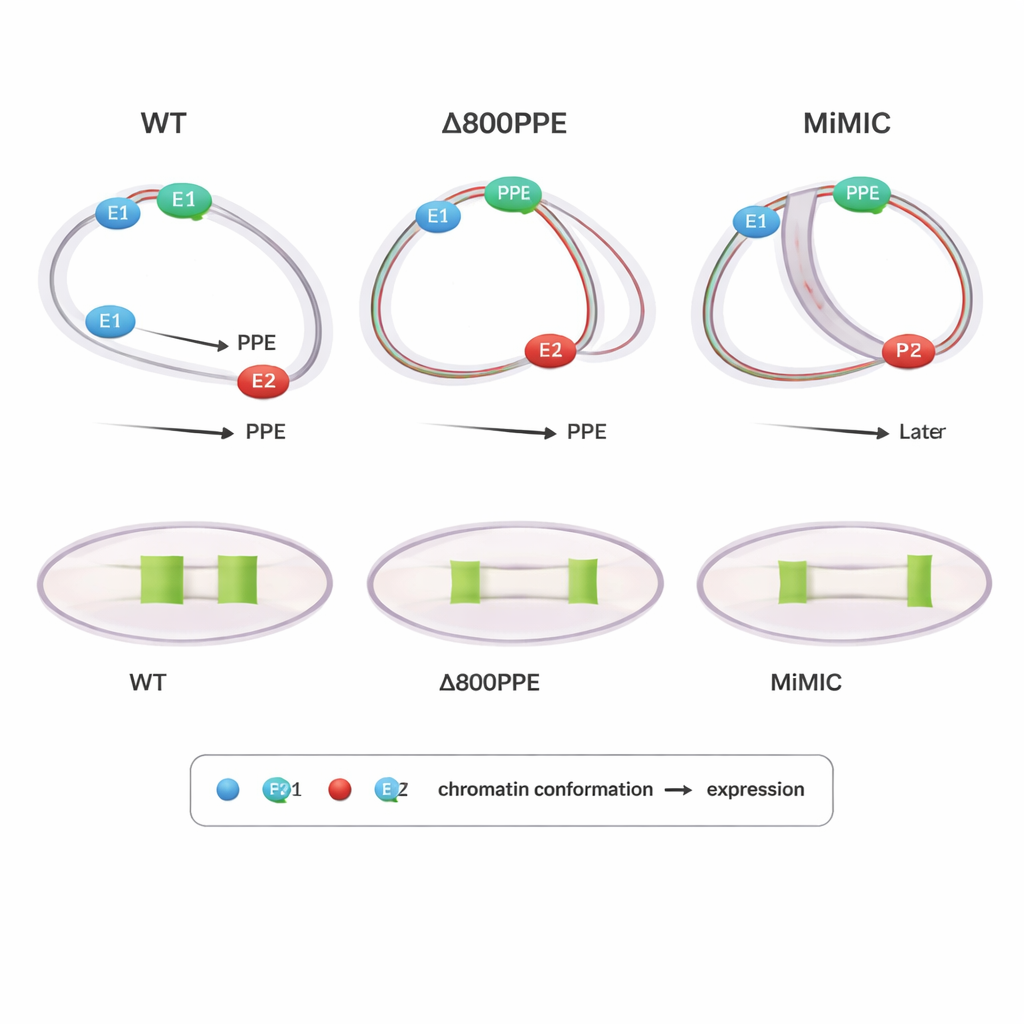
Las mutaciones revelan por qué importan el tiempo y la posición
Para sondear causa y efecto, los autores examinaron moscas con cambios diseñados en el locus de brk. En un mutante se eliminaron 800 pares de bases del PPE, debilitando este elemento central; en otro, se insertó una cassette de 7,3 kilobases (MiMIC) entre E1 y el PPE, empujándolos efectivamente más separados y añadiendo un promotor extra. Ambos mutantes mostraron una expresión de brk retrasada o reducida. PLOTTED mostró por qué: en la línea con deleción del PPE, la compactación de las distancias entre el PPE y ambos potenciadores ocurrió más tarde de lo normal, y en etapas tardías el PPE se mantuvo demasiado cerca de E1, impidiendo que E2 impulsara el patrón de expresión amplio observado en el tipo salvaje. En la línea MiMIC, el PPE se asoció demasiado pronto y con demasiada fuerza con E2 y solo más tarde se acercó a E1, alterando de nuevo la transferencia normal entre potenciadores. Estos resultados sugieren que no solo importa si los elementos se juntan, sino cuándo y con qué socio están más próximos, para obtener una salida génica correcta.
El plegamiento del ADN varía a lo largo del embrión
Puesto que PLOTTED conserva la información espacial dentro de embriones intactos, el equipo también pudo preguntar si la arquitectura del ADN difiere en varias regiones corporales. Comparando zonas laterales donde brk está activo con zonas ventrales donde está reprimido, encontraron que los tres elementos se sitúan más cerca en las regiones activas y se separan más en los dominios reprimidos. A lo largo del eje cabeza-cola, observaron que las distancias E1–PPE cambian de forma distinta en la parte frontal respecto a la trasera del embrión, lo que sugiere que señales regionales ajustan la arquitectura de la cromatina para afinar los patrones de expresión génica. Estos hallazgos apoyan una visión en la que la disposición 3D del ADN regulador depende del contexto, rastreando tanto el tiempo como la posición en el organismo en desarrollo.
Por qué esto importa más allá de las moscas
En términos simples, este estudio muestra que cómo se pliega el ADN alrededor de un solo gen está estrechamente ligado a cuándo y dónde ese gen se activa. El nuevo método PLOTTED proporciona una forma práctica de cartografiar estos pequeños vecindarios del ADN en tejidos intactos usando microscopios de amplia disponibilidad y una química sencilla, combinada con modelado probabilístico potente. Aunque se demostró en embriones de mosca, el enfoque puede aplicarse a muchos organismos y modelos de enfermedad. A medida que los científicos descubren cada vez más que la cromatina mal plegada subyace a trastornos del desarrollo y cánceres, herramientas como PLOTTED ayudarán a revelar cómo pequeños cambios en la disposición 3D de potenciadores y genes pueden propagarse en grandes alteraciones del destino celular y la salud.
Cita: Le, M.T., McGehee, J., Dunipace, L. et al. Inferring chromatin architecture at a single locus through probabilistic in situ DNA localization. Nat Commun 17, 1752 (2026). https://doi.org/10.1038/s41467-026-68460-x
Palabras clave: arquitectura de la cromatina, interacciones potenciador-promotor, embriogénesis de Drosophila, regulación génica, imagen de superresolución