Clear Sky Science · es
DKK1 y NEDD4 derivados de células de la cresta neural modulan la señalización Wnt en el segundo campo cardíaco para coordinar el desarrollo del tracto de salida
Por qué importan los pequeños constructores del corazón
El corazón del embrión temprano comienza como un tubo simple, pero debe remodelarse rápidamente en un órgano complejo que envíe sangre tanto al cuerpo como a los pulmones. Pasos sutiles en este proceso de construcción pueden provocar defectos congénitos graves, incluidas afecciones que requieren cirugía poco después del nacimiento. Este estudio revela cómo dos grupos de células se comunican mientras moldean la vía principal de salida del corazón y muestra un error molecular que puede contribuir a la cardiopatía congénita en ratones y en humanos.
Dos equipos que construyen la rampa de salida del corazón
La porción del corazón que transporta la sangre fuera de los ventrículos —el tracto de salida— se forma a partir de una región llamada segundo campo cardíaco. Las células aquí deben permanecer como «progenitores» flexibles el tiempo suficiente para incorporarse al tracto de salida en crecimiento y luego convertirse en músculo maduro en el momento adecuado. Junto a ellas transitan las células de la cresta neural, una población nómada que ayuda a construir las grandes arterias y las válvulas. Trabajos anteriores sugerían que estas células de la cresta influyen de algún modo en el segundo campo cardíaco, pero se desconocía cómo funcionaba ese diálogo. 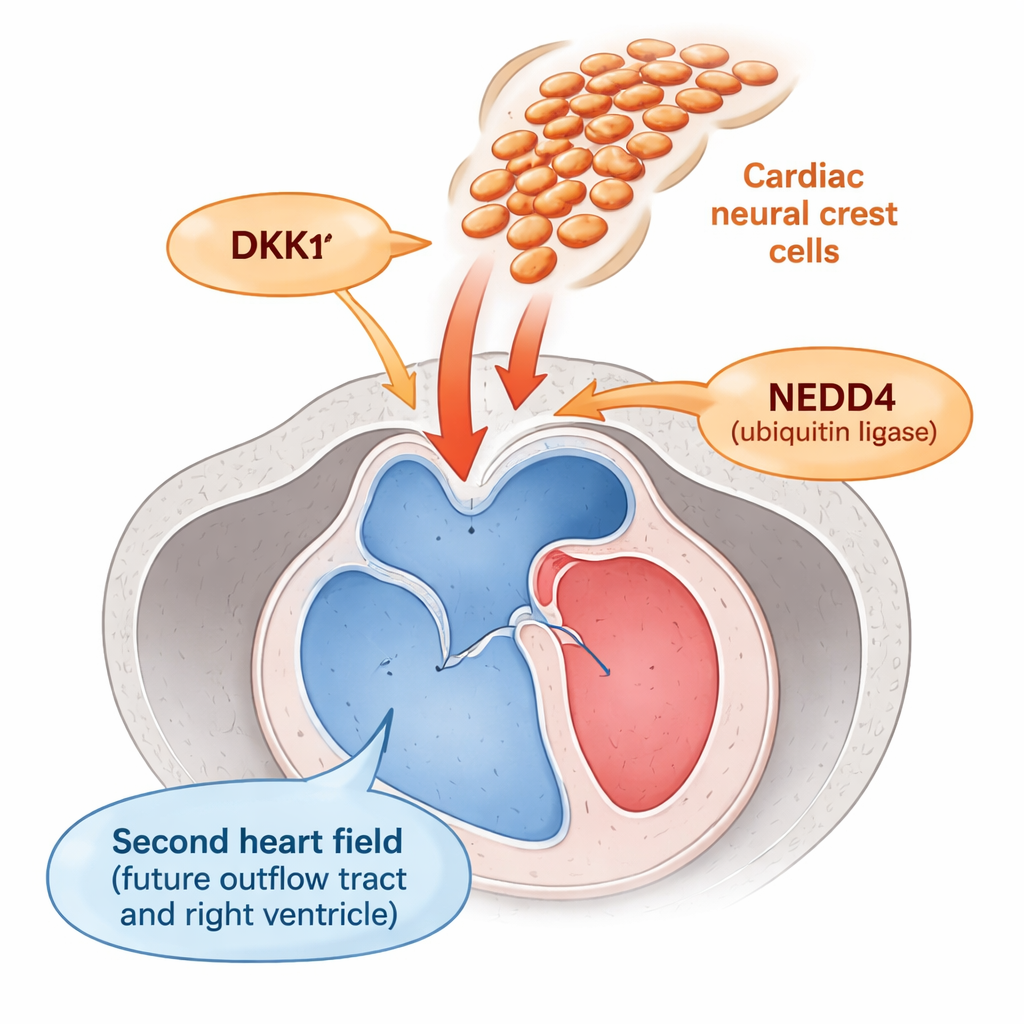
Un regulador molecular tipo atenuador para las señales de crecimiento
Los autores descubrieron que las células de la cresta neural actúan como un atenuador de una señal de crecimiento clave llamada Wnt, que mantiene a los progenitores proliferando y retrasa su maduración. Encontraron que las células de la cresta son una fuente importante de DKK1, una pequeña proteína secretada que apaga la señalización Wnt en las células vecinas. DKK1 en sí está normalmente controlada por NEDD4, una proteína que marca a DKK1 para su eliminación. En embriones de ratón que carecían de Nedd4 específicamente en las células de la cresta neural, DKK1 se acumuló a niveles anormalmente altos. Este exceso de DKK1 redujo la actividad de Wnt en el segundo campo cardíaco vecino, como se mostró por la disminución de beta‑catenina nuclear —una medida estándar de la señalización Wnt— y por niveles más bajos de múltiples genes sensibles a Wnt.
Cuando el momento falla, la geometría del corazón se altera
Demasiado DKK1 y muy poca señal Wnt tuvieron una consecuencia clara: las células del segundo campo cardíaco comenzaron a convertirse en músculo cardíaco demasiado pronto. Marcadores de músculo maduro aparecieron temprano en esta zona de progenitores, y quedaron menos células indiferenciadas para alargar el tracto de salida. Al seguir las células en división a lo largo del tiempo, el equipo mostró que se incorporaron menos células del segundo campo cardíaco al tracto de salida en los mutantes. Como resultado, el tracto de salida era más corto y rotaba de forma incorrecta, lo que provocó desalineación entre las grandes arterias y los ventrículos. Estos errores estructurales se parecían a defectos conotruncales humanos como el ventrículo derecho de doble salida y malformaciones relacionadas observadas en ratones con eliminación completa de Nedd4.
Demostrando el papel de la señal y un vínculo con la enfermedad humana
Para confirmar que la alteración de la señalización Wnt causaba realmente estos problemas, los investigadores manipularon la vía con fármacos en ratonas gestantes. Bloquear Wnt en embriones sanos los empujó hacia la misma diferenciación prematura y los defectos de rotación observados cuando se perdió Nedd4, mientras que reducir la dosis del gen Dkk1 en el contexto deficiente en Nedd4 rescató parcialmente el tamaño y la rotación del tracto de salida. Finalmente, el equipo identificó a un niño con tetralogía de Fallot que portaba un cambio hereditario raro en NEDD4 que debilitaba su capacidad para marcar DKK1 para su degradación. Ratones diseñados para portar la misma variante de Nedd4 desarrollaron defectos en las paredes y en el septo del corazón derechos, lo que respalda la idea de que un control defectuoso de NEDD4–DKK1 puede contribuir a la cardiopatía congénita humana. 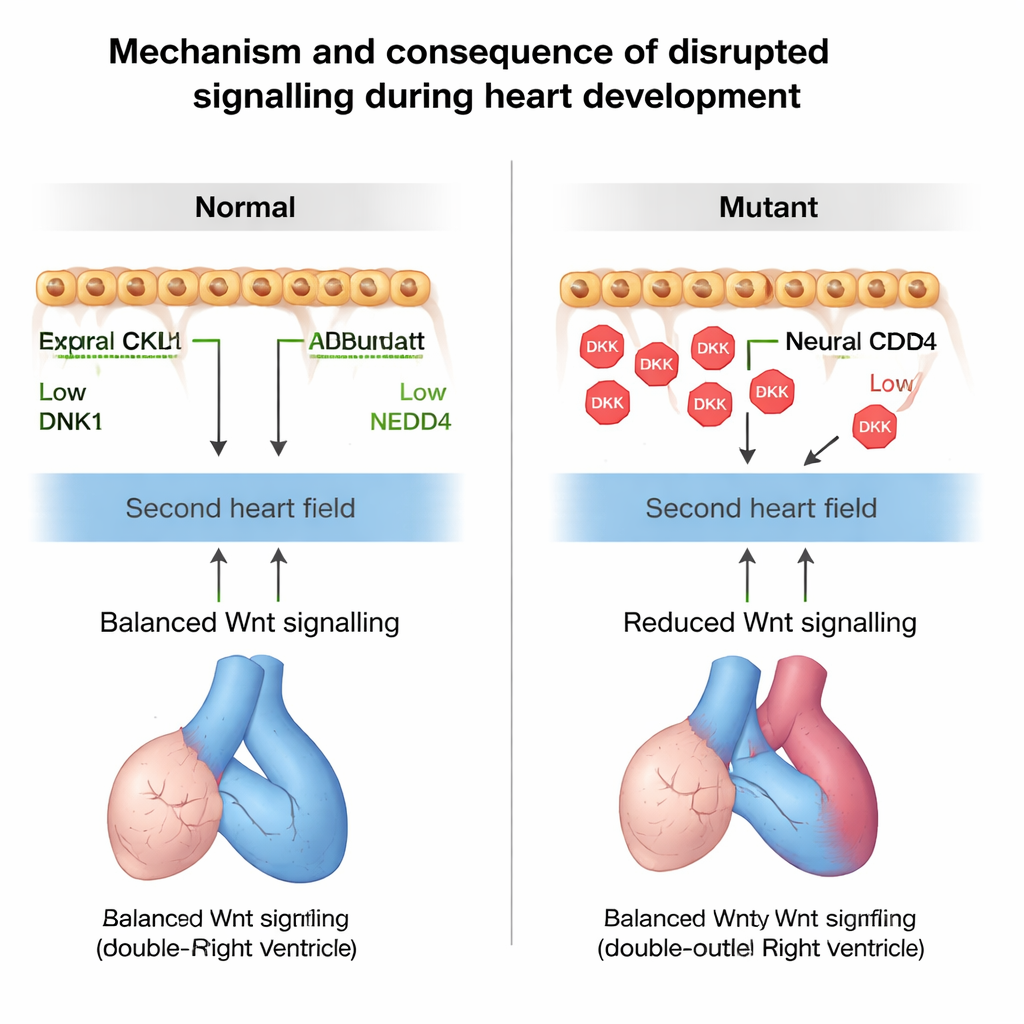
Qué significa esto para entender los defectos cardíacos
Para el público general, el mensaje clave es que la «rampa de salida» del corazón depende del momento preciso en que sus componentes dejan de multiplicarse y empiezan a convertirse en músculo. Este cronometraje no está controlado solo desde el propio tejido cardíaco, sino también por las células de la cresta neural vecinas que ajustan finamente una señal de crecimiento mediante el par NEDD4–DKK1. Cuando este regulador molecular queda demasiado bajo, el tracto de salida queda infraestructurado y desalineado, lo que conduce a defectos congénitos graves. Al trazar esta vía y vincularla a una variante genética humana, el estudio ofrece nuevas pistas sobre cómo surgen algunos defectos cardíacos congénitos y señala posibles dianas moleculares para futuros diagnósticos o intervenciones.
Cita: Wiszniak, S., Alankarage, D., Lohraseb, I. et al. Neural crest cell-derived DKK1 and NEDD4 modulate Wnt signalling in the second heart field to orchestrate outflow tract development. Nat Commun 17, 1751 (2026). https://doi.org/10.1038/s41467-026-68459-4
Palabras clave: cardiopatía congénita, desarrollo cardíaco, células de la cresta neural, señalización Wnt, tracto de salida cardíaco