Clear Sky Science · es
Una deleción común en el ADN que altera la región 3’UTR de mdr1 se asocia con una menor susceptibilidad a mefloquina en parásitos de P. vivax de pacientes camboyanos
Por qué importa este estudio sobre la malaria
Para las personas que viven o viajan a regiones endémicas de malaria, los fármacos eficaces son un salvavidas. Pero los parásitos de la malaria evolucionan constantemente para sobrevivir al tratamiento. Este estudio se centra en Plasmodium vivax, la principal causa de malaria fuera de África, y revela un cambio genético sutil que podría ya estar ayudando al parásito a tolerar un fármaco importante, la mefloquina. Entender este cambio ahora podría ayudar a las autoridades sanitarias a adelantarse a la aparición de resistencia a los medicamentos.
Un parásito tenaz y sus opciones de tratamiento que se reducen
La malaria en humanos la causan varios parásitos relacionados, pero P. vivax es especialmente difícil de eliminar. Puede esconderse en el hígado durante meses antes de reaparecer en la sangre y a menudo circula a niveles demasiado bajos para ser detectados por las pruebas estándar. Durante décadas, el fármaco de primera línea cloroquina funcionó bien contra P. vivax, pero han aparecido señales de resistencia. Como resultado, la Organización Mundial de la Salud recomienda ahora el uso de terapias combinadas basadas en artemisinina (ACT), que emparejan un fármaco de acción rápida con un compañero de acción más prolongada, como la mefloquina. Debido a que el cultivo en laboratorio de P. vivax es complicado, los científicos dependen en gran medida de muestras de pacientes y de pistas genéticas para rastrear cómo responde el parásito a estos medicamentos.
Una diminuta pieza de ADN ausente en un gen clave de resistencia
Los investigadores secuenciaron los genomas de 206 muestras de P. vivax tomadas de pacientes con malaria en Camboya entre 2021 y 2023. Buscaron tramos de ADN que estuvieran eliminados o duplicados. Entre muchas reordenaciones, destacó una: más del 80% de los parásitos portaban una pequeña deleción de ADN situada justo después del final de la región codificante de un gen llamado mdr1 (multidrug resistance 1). Este gen codifica una proteína transportadora que puede bombear diversos compuestos, incluidos fármacos, a través de una membrana dentro del parásito. A diferencia de mutaciones descritas anteriormente, esta deleción de 837 pares de bases no cambió la secuencia proteica en sí. En lugar de eso, se localizaba en la llamada región no traducida 3' (3'UTR), un segmento del gen que no se traduce en proteína pero que puede influir fuertemente en la cantidad de proteína que finalmente se produce.
Deleciones independientes y mensajes alterados del mismo gen
Para ver si aparecían cambios similares en otras zonas, el equipo reanalizó casi 830 genomas de P. vivax de 25 países. Descubrieron otra deleción más corta que solapaba la misma región aguas abajo de mdr1 en parásitos de Sudamérica. Comparaciones detalladas y pruebas PCR confirmatorias mostraron que las deleciones del Sudeste Asiático y de Sudamérica eran distintas, lo que sugiere que surgieron de forma independiente —una indicación de que la selección natural puede favorecer alteraciones en esta región reguladora. Mediante secuenciación de ARN en 95 infecciones camboyanas, los investigadores demostraron que los parásitos con la deleción producían una versión alternativa del ARN mensajero de mdr1, con una 3'UTR diferente. Tras ajustar por la longitud del transcrito, los parásitos que portaban la deleción presentaban casi el doble de ARN mensajero de mdr1 que los que no la tenían, lo que implica que el ADN ausente o la nueva secuencia de la 3'UTR ayuda a estabilizar o aumentar la expresión del gen.
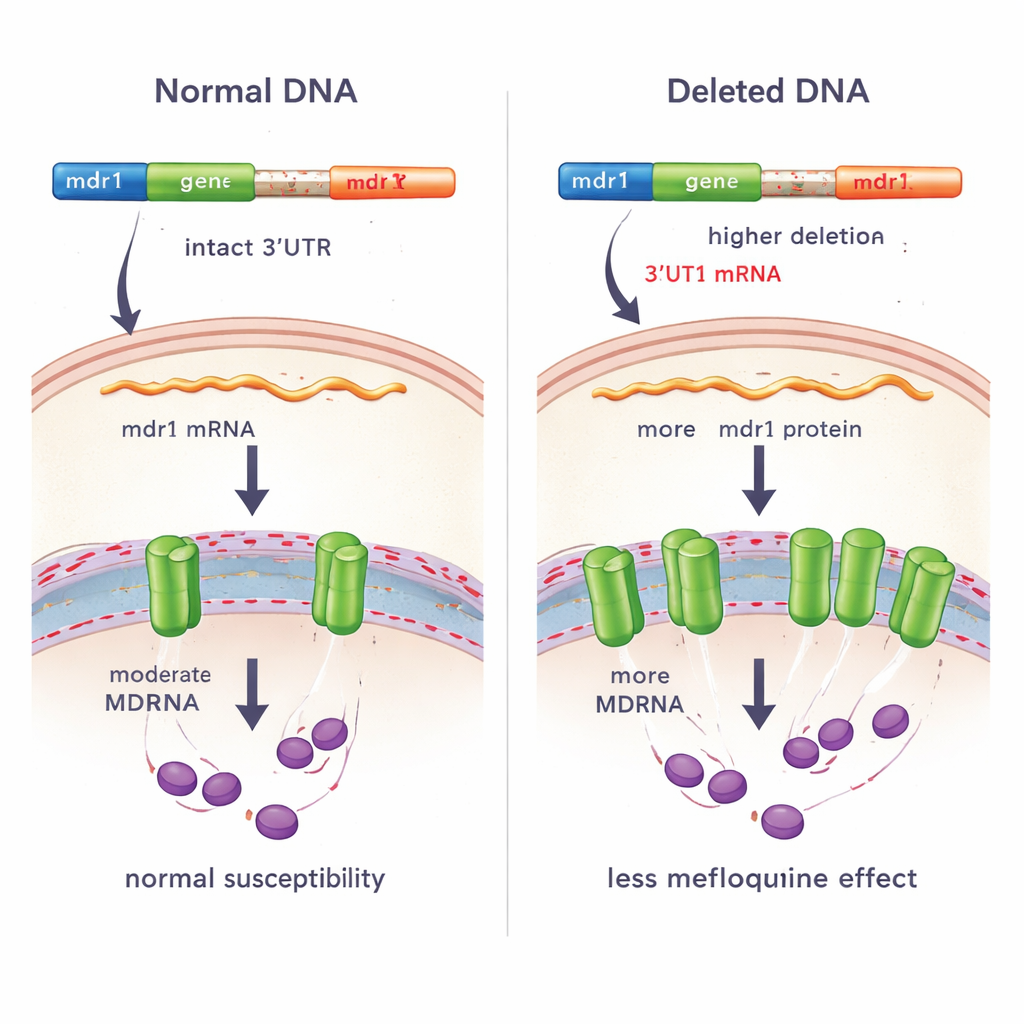
Vinculando la deleción con la respuesta a fármacos en pacientes y pruebas de laboratorio
Dado que mdr1 se ha implicado en la resistencia a varios antimaláricos, el equipo investigó si la deleción estaba ligada a la respuesta de los parásitos al tratamiento. Primero compararon la rapidez con que los parásitos eran eliminados de la sangre de los pacientes tras el tratamiento con artesunato. Entre 167 infecciones, no hubo una diferencia significativa en las tasas de aclaramiento entre parásitos con y sin la deleción, lo que sugiere que este cambio genético no afecta directamente la sensibilidad al artesunato en sí. Sin embargo, en un conjunto más pequeño de 14 infecciones en las que los investigadores midieron el crecimiento del parásito en presencia de mefloquina fuera del organismo, los parásitos con la deleción tendieron a mostrar valores de CI50 más altos —lo que significa que requerían más fármaco para inhibir el crecimiento— que los parásitos sin la deleción. Este patrón es coherente con una menor susceptibilidad a la mefloquina, aunque el tamaño de la muestra fue limitado.
Un aumento preocupante a lo largo del tiempo y lo que podría significar
Para entender qué tan extendida se ha vuelto la deleción, los autores analizaron 592 muestras archivadas de P. vivax recogidas en Camboya entre 2014 y 2024. Antes de que la mefloquina se introdujera como parte de las ACT para la malaria por vivax alrededor de 2016–2017, aproximadamente el 30% de los parásitos portaban la deleción. Tras el cambio, la frecuencia subió por encima del 60% y luego se estabilizó, una tendencia estadísticamente sólida que se mantuvo incluso al centrarse solo en el este de Camboya. La deleción ya estaba presente en niveles bajos antes de que la mefloquina se usara ampliamente contra P. vivax, posiblemente debido a la exposición indirecta cuando el fármaco se empleó para tratar P. falciparum o porque el cambio también afecta la respuesta a otros medicamentos. Junto con informes recientes de un aclaramiento ligeramente más lento de los parásitos después del tratamiento con artemisinina, los resultados plantean la preocupación de que P. vivax en Camboya pueda estar avanzando hacia una disminución de la efectividad de la combinación actual artesunato–mefloquina.
Qué significa esto para el control de la malaria
Para no especialistas, el mensaje central es que incluso cuando el gen principal de resistencia a fármacos de un parásito parece intacto, pequeños cambios en el “cableado de control” cercano de su ADN pueden alterar la intensidad con la que se activa el gen. En este caso, una deleción común en una región no codificante de mdr1 parece aumentar la actividad del gen y se asocia con efectos ligeramente menores de la mefloquina sobre P. vivax. Aunque aún no hay evidencia clara de fallos de tratamiento en Camboya, la creciente frecuencia de esta deleción sugiere que la presión farmacológica podría estar favoreciendo silenciosamente a los parásitos con este rasgo. Reconocer y vigilar pronto estos sutiles signos genéticos de advertencia puede ayudar a las autoridades sanitarias a ajustar las políticas de fármacos, diseñar mejores herramientas de vigilancia y proteger el reducido arsenal de tratamientos antimaláricos eficaces.
Cita: Ko, K., Tebben, K., Andrianinarivomanana, T. et al. A common DNA deletion altering the 3’UTR of mdr1 is associated with reduced mefloquine susceptibility in P. vivax parasites from Cambodian patients. Nat Commun 17, 1748 (2026). https://doi.org/10.1038/s41467-026-68456-7
Palabras clave: Plasmodium vivax, resistencia a fármacos antipalúdicos, mefloquina, gen mdr1, Camboya