Clear Sky Science · es
Af-CUT&Tag: un método sensible y sin anticuerpos para el perfilado de la cromatina que utiliza etiquetas codificadas genéticamente y dianas de alta afinidad fusionadas a Tn5
Un vistazo al centro de control de nuestro ADN
Cada célula de tu cuerpo decide de forma continua qué genes activar o silenciar, determinando desde la reparación hepática hasta el riesgo de cáncer. Los científicos estudian estas decisiones mapeando dónde se sitúan proteínas clave sobre el ADN, pero las mejores herramientas para hacerlo han dependido durante mucho tiempo de anticuerpos frágiles y caros que no siempre funcionan bien. Este artículo presenta una nueva forma, sin anticuerpos, de trazar estas interacciones ADN–proteína, llamada Af-CUT&Tag, que es más sensible, más fiable y lo bastante potente como para funcionar incluso con muestras diminutas y células individuales.
Por qué los anticuerpos nos limitan
Los métodos clásicos de mapeo de la cromatina requieren anticuerpos —grandes proteínas en forma de Y que reconocen una proteína objetivo concreta— para guiar una enzima hacia los lugares correctos del ADN. Cuando los anticuerpos funcionan a la perfección permiten a los investigadores ver dónde se unen los factores de transcripción y otros reguladores en todo el genoma. Pero en la práctica, los anticuerpos pueden ser difíciles de conseguir, inconsistentes en calidad y verse bloqueados por modificaciones químicas habituales en las proteínas, como fosforilación o acetilación. Estos problemas pueden difuminar los mapas resultantes, limitar las proteínas que pueden estudiarse y dificultar la comparación de resultados entre laboratorios o experimentos.
Etiquetas diminutas y dianas inteligentes reemplazan a los anticuerpos
Af-CUT&Tag evita por completo los anticuerpos al dar a la proteína de interés una pequeña etiqueta genética. Mediante edición genómica CRISPR, los investigadores fusionan breves péptidos etiquetadores, como HiBiT o ALFA, a la proteína natural dentro de células o tejidos. Luego usan proteínas asociadas diseñadas —dianas de alta afinidad que reconocen esas etiquetas— directamente fusionadas a la enzima Tn5, que corta el ADN y añade adaptadores para secuenciación. Cuando la fusión diana–Tn5 se une a la etiqueta en la proteína de interés, corta el ADN cercano y marca esos sitios para secuenciarlos. Dado que las etiquetas son muy pequeñas y la fusión diana–Tn5 es mucho menor que un anticuerpo, este sistema entra fácilmente en células y núcleos, se une con precisión excepcional y no se ve afectado por modificaciones químicas en la proteína objetivo. 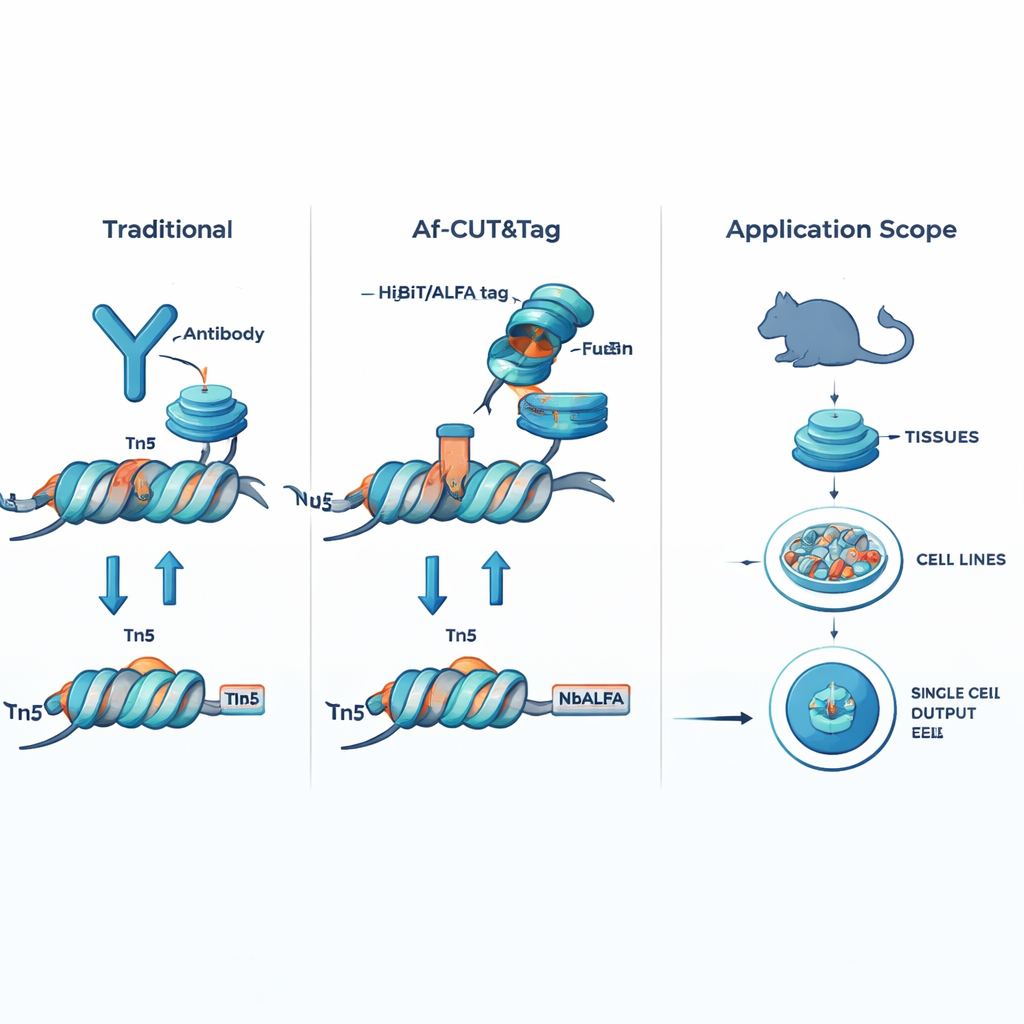
Mapas más nítidos a partir de menos células
El equipo mostró primero que sus fusiones diana–Tn5 siguen captando las etiquetas con gran fuerza y cortando el ADN de forma eficiente. Después compararon Af-CUT&Tag con métodos basados en anticuerpos de última generación para mapear la ARN polimerasa II, la enzima que transcribe los genes codificadores de proteínas, y la proteína CTCF, un organizador principal de la estructura del genoma. En líneas celulares humanas, Af-CUT&Tag produjo señal más limpia en los puntos de inicio de los genes, menos cortes fuera de objetivo en regiones de ADN abiertas pero irrelevantes, y bibliotecas de secuenciación de mayor calidad. De forma notable, generó mapas robustos a partir de tan solo unas 500 células aproximadamente, y la misma estrategia puede adaptarse a muchos dianas distintas que apunten a características diferentes del ADN. El método también se extendió a células individuales mediante el barcoding de los fragmentos de cada célula, permitiendo construir mapas detallados de la cromatina célula por célula.
Siguiendo la reparación hepática en tiempo real
Para demostrar lo que esta tecnología puede revelar en animales vivos, los autores aplicaron Af-CUT&Tag a la regeneración hepática en ratón. Usaron virus y CRISPR para añadir etiquetas HiBiT a dos reguladores clave de la «vía Hippo», YAP1 y TAZ, que ayudan a controlar el tamaño del órgano y la reparación. Tras extirpar quirúrgicamente parte del hígado, aislaron núcleos de células hepáticas antes de la operación y 24 horas después, y luego usaron Af-CUT&Tag para ver dónde se unían YAP1 y TAZ en el genoma. Los mapas mostraron que, poco después de la lesión, estas proteínas reducen su presencia en genes que impulsan el procesamiento y la síntesis de grasas, mientras que las células hepáticas acumulan temporalmente gotas de grasa. Al mismo tiempo, YAP1/TAZ aumentan su unión en genes implicados en la eliminación del hemo, un componente potencialmente tóxico de la sangre, y en Mir122, un gen que produce un microARN muy abundante en el hígado.
miR-122 como guardián de la regeneración
miR-122 es una molécula de ARN diminuta que ayuda a afinar la actividad de muchos otros genes. Usando Af-CUT&Tag, los investigadores observaron una mayor unión de YAP1/TAZ cerca de la región de Mir122, junto con una cromatina más abierta y marcas químicas reforzadas asociadas a la activación génica. Experimentos confirmaron que los niveles de miR-122 aumentan durante la ventana temprana de regeneración. Cuando el equipo eliminó específicamente miR-122 en células hepáticas de ratón, los animales mostraron más acumulación de grasa, respuestas inflamatorias más intensas y menos células hepáticas entrando en el ciclo celular tras la cirugía. En conjunto, estos resultados sugieren que YAP1/TAZ ayudan al hígado a mantener un equilibrio cuidadoso durante la reparación: acumular temporalmente grasa para obtener energía, limitar el daño por hemo y la inflamación, y usar miR-122 para frenar el estrés excesivo mientras promueven el crecimiento del tejido. 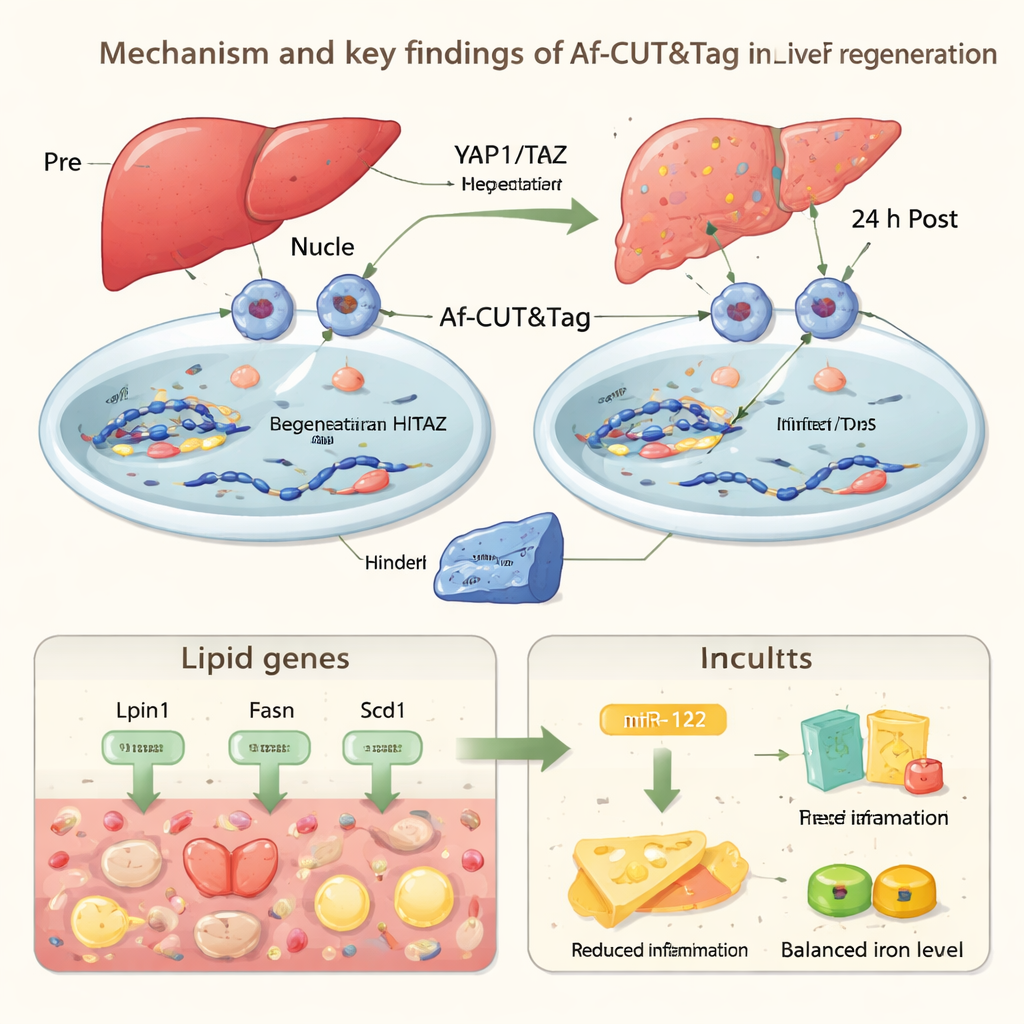
Una nueva lente versátil sobre el control génico
Af-CUT&Tag ofrece una forma modular y sin anticuerpos de ver dónde se sitúan proteínas clave sobre el ADN en líneas celulares, tejidos e incluso células individuales. Al reemplazar anticuerpos impredecibles con pequeñas etiquetas genéticas y dianas diseñadas, proporciona mapas más nítidos y reproducibles a partir de muchas menos células. Aplicado a la regeneración hepática, reveló cómo YAP1 y TAZ coordinan el metabolismo, el manejo del hierro y el microARN miR-122 para apoyar la reparación temprana. A medida que la edición genómica y las dianas diseñadas continúen mejorando, esta estrategia podría convertirse en una herramienta estándar para diseccionar cómo la regulación génica funciona correctamente en el desarrollo y la regeneración —y cómo falla en enfermedades como el cáncer y la insuficiencia hepática.
Cita: Wang, X., Deng, X., Qiu, L. et al. Af-CUT&Tag: a sensitive and antibody-free chromatin profiling method using genetically encoded tags and high-affinity binders fused to Tn5. Nat Commun 17, 1746 (2026). https://doi.org/10.1038/s41467-026-68454-9
Palabras clave: perfilado de cromatina, epigenética, regeneración hepática, YAP1 TAZ, microARN-122