Clear Sky Science · es
Variantes funcionales en 1p36.23 confieren riesgo de esquizofrenia modulando RERE
Por qué importan los pequeños cambios en el ADN para la salud mental
La esquizofrenia es una enfermedad mental grave que afecta cómo las personas piensan, sienten y se relacionan con los demás. Tiene una fuerte carga familiar, pero la mayoría de los cambios genéticos implicados son pequeñas variaciones dispersas en nuestro ADN. Este estudio se centra en una de esas regiones del genoma y muestra, paso a paso, cómo dos sutiles variantes de ADN pueden alterar el desarrollo y la comunicación de las células cerebrales de maneras que podrían aumentar el riesgo de esquizofrenia. 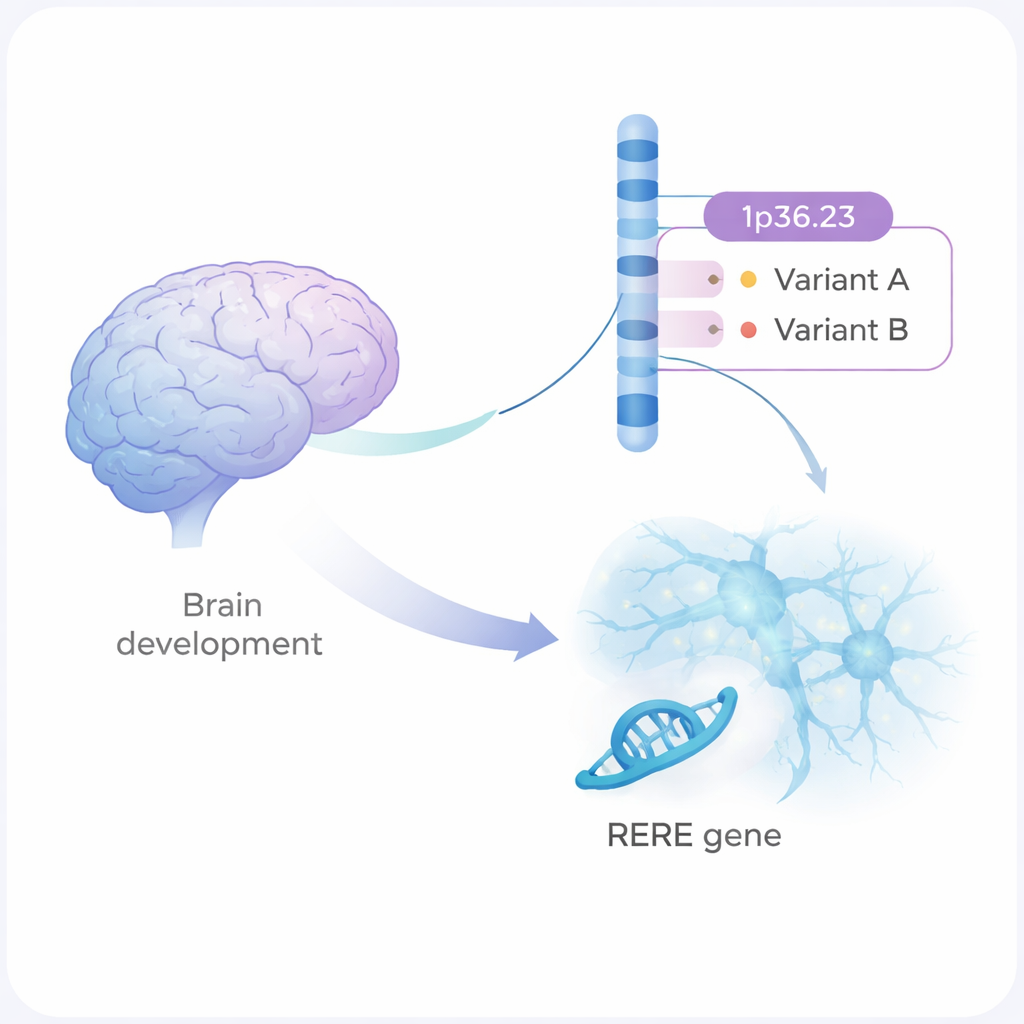
Un punto caliente genético en el cromosoma 1
Grandes estudios genéticos han señalado más de 300 regiones del genoma humano vinculadas a la esquizofrenia. Una de ellas es un tramo de ADN en el cromosoma 1, denominado 1p36.23. Hasta ahora, los científicos no sabían qué cambios concretos en esta región, ni qué gen, estaban causando el efecto. Los autores combinaron genética estadística con experimentos de laboratorio y señalaron dos variantes de ADN, llamadas rs159961 y rs301792, ubicadas dentro de un gen denominado RERE. Estas variantes no cambian la proteína RERE en sí; en cambio, se sitúan en zonas reguladoras —«interruptores»— dentro del gen que controlan cuán activo está RERE.
Cómo las variantes de riesgo suben el volumen de RERE
El equipo preguntó primero si estas dos variantes actúan realmente como interruptores funcionales. Usando ensayos reporteros —pruebas en las que un fragmento de ADN impulsa un gen que produce luz— mostraron que las versiones asociadas a la esquizofrenia de rs159961 y rs301792 se comportan como potenciadores (boosters) más fuertes en células de tipo nervioso, pero no en tipos celulares no relacionados. Ensayos bioquímicos de unión revelaron por qué: la forma de riesgo de una variante debilita la unión de REST, una proteína que normalmente reprime la actividad génica, mientras que la forma de riesgo de la otra fortalece la unión de POLR2A, una parte central de la maquinaria lectora del gen. En conjunto, estos cambios en la unión proteica aumentan la actividad de los segmentos potenciadores y elevan la expresión de RERE.
De RERE aumentado al crecimiento alterado de las células cerebrales
A continuación, los investigadores preguntaron qué hace el exceso de RERE dentro del cerebro. Encontraron que las personas fallecidas con esquizofrenia mostraban niveles más altos de RERE en su tejido cerebral en comparación con individuos no afectados. Para modelarlo, aumentaron artificialmente los niveles de RERE en células madre neuronales de ratón —las células inmaduras que originan neuronas y glía. Cuando RERE se sobreexpresó, estas células madre proliferaron menos, se quedaron atrapadas en una fase tardía del ciclo celular y produjeron menos neuronas maduras, dejando otros tipos celulares mayormente sin cambio. En neuronas en cultivo, el exceso de RERE también reconfiguró sus patrones de ramificación y redujo el número y el tipo de pequeñas protuberancias llamadas espinas dendríticas, donde se forman las sinapsis. Estos cambios concuerdan con la evidencia de larga data de que la esquizofrenia implica un desarrollo cerebral alterado y pérdida de espinas.
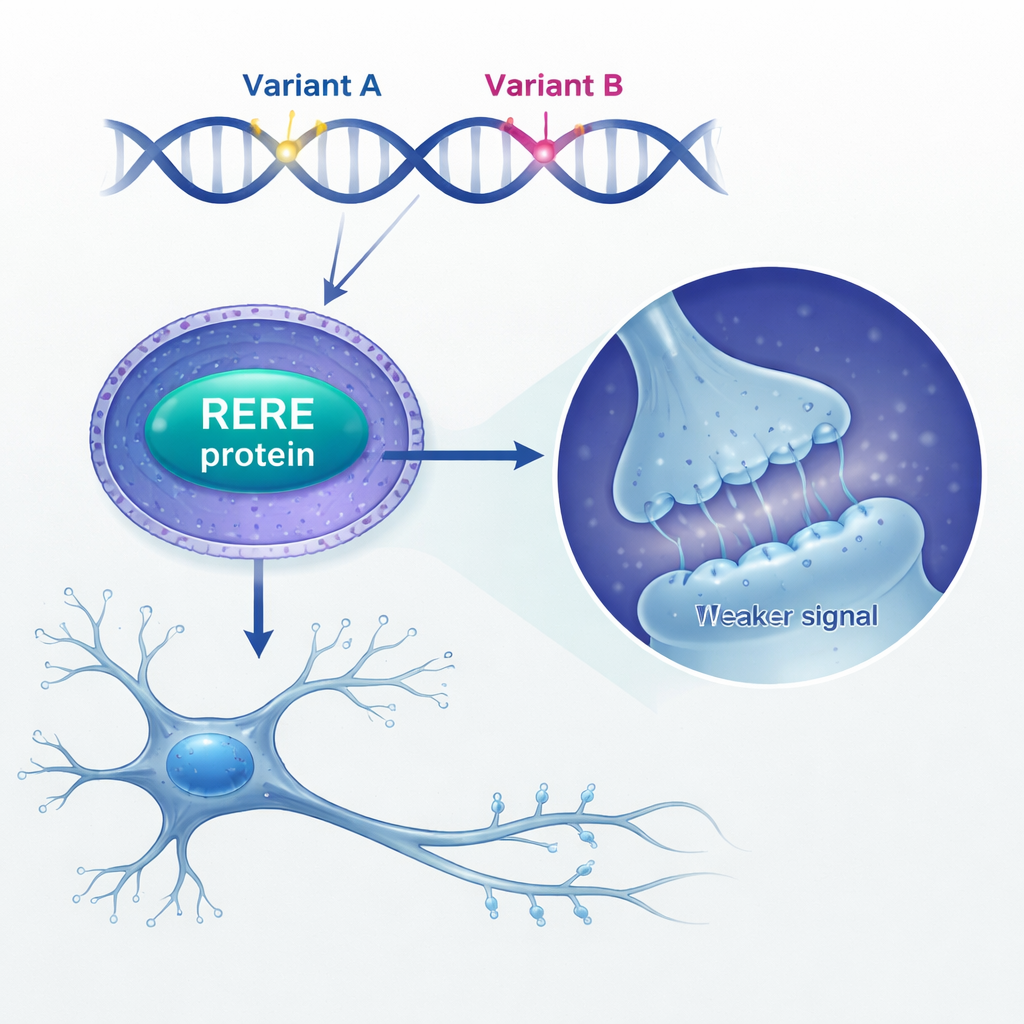
Alterando la “conversación” de glutamato del cerebro
Al mirar más detenidamente la actividad génica, el equipo encontró que la sobreexpresión de RERE perturbaba redes de genes implicados en el crecimiento de dendritas y en sistemas de señalización química mayores, especialmente la vía del glutamato. Surgió un objetivo clave: el gen GRIN2A, que codifica una subunidad crucial (GluN2A) de los receptores de glutamato de tipo NMDA, implicados desde hace tiempo en la esquizofrenia. Los autores mostraron que RERE se asocia con otras dos proteínas nucleares, RARB y RXRA, para unirse directamente al promotor de GRIN2A y suprimir su actividad. En neuronas con exceso de RERE, los niveles de GluN2A disminuyeron y los registros eléctricos revelaron corrientes sinápticas mediadas por NMDA más débiles, aunque la frecuencia de los eventos sinápticos no cambió. En otras palabras, se bajó el “volumen” de las señales excitatorias individuales.
Conectando las variantes de ADN con la función cerebral
Al entrelazar genética, biología molecular, cultivo celular y electrofisiología, este trabajo traza una cadena causal clara: las variantes de ADN de riesgo en 1p36.23 potencian elementos reguladores dentro del gen RERE, conduciendo a una mayor expresión de RERE en las células cerebrales. El aumento de RERE, a su vez, afecta el crecimiento y la maduración de las neuronas, altera la forma y el número de sus espinas sinápticas y debilita la señalización basada en glutamato a través de receptores NMDA —especialmente los que contienen GluN2A. Para un lector general, la idea principal es que cambios muy pequeños en el ADN pueden desplazar ligeramente la actividad de un único gen y, a lo largo de muchas células cerebrales y muchos años, esto puede desviar el desarrollo y la comunicación cerebral de forma que contribuya a la esquizofrenia.
Cita: Liu, Y., Wang, J., Yang, H. et al. Functional variants at 1p36.23 confer risk of schizophrenia through modulating RERE. Nat Commun 17, 1742 (2026). https://doi.org/10.1038/s41467-026-68449-6
Palabras clave: genética de la esquizofrenia, gen RERE, neurodesarrollo, señalización del glutamato, función sináptica