Clear Sky Science · es
Polarización de CO2 impulsada por campo eléctrico y bloqueo protónico bioinspirado desbloquean la reducción de CO2 en ácido fuerte sin cationes metálicos
Convertir un gas problemático en un ingrediente útil para combustibles
El dióxido de carbono (CO2) es el principal gas de efecto invernadero que impulsa el cambio climático, pero también es una posible materia prima para fabricar combustibles y productos químicos usando electricidad renovable. Uno de los mayores obstáculos es que el CO2 es obstinadamente poco reactivo, especialmente en disoluciones muy ácidas donde se forma gas hidrógeno no deseado en su lugar. Este estudio muestra cómo un nanomaterial de oro con una forma inteligente, recubierto por una capa bioinspirada, puede superar estos obstáculos y convertir el CO2 en monóxido de carbono (CO) de manera eficiente en condiciones ácidas severas, sin depender de sales metálicas disueltas que habitualmente provocan obstrucciones y residuos.

Por qué importa trabajar en ácido fuerte
La mayoría de los dispositivos que convierten eléctricamente CO2 operan en disoluciones neutras o alcalinas. Allí, sin embargo, el CO2 tiende a reaccionar con el medio y formar carbonatos y bicarbonatos, desperdiciando gran parte del gas y acortando la vida útil del dispositivo a medida que se acumulan sólidos. Realizar la reacción en ácido fuerte podría evitar estas pérdidas y aprovechar mejor cada molécula de CO2. El problema es que en ácido los iones de hidrógeno cargados positivamente están por todas partes y se combinan con facilidad para formar hidrógeno, compitiendo con el CO2 por electrones en la superficie del electrodo. Al mismo tiempo, las moléculas neutras de CO2 no se adhieren con facilidad a las superficies metálicas. Los autores se propusieron diseñar un catalizador y un entorno circundante que tanto atraigan y activen el CO2 como mantengan a raya los protones, todo ello en una solución ácida sin cationes metálicos.
Triángulos afilados de oro que sobrecargan el CO2
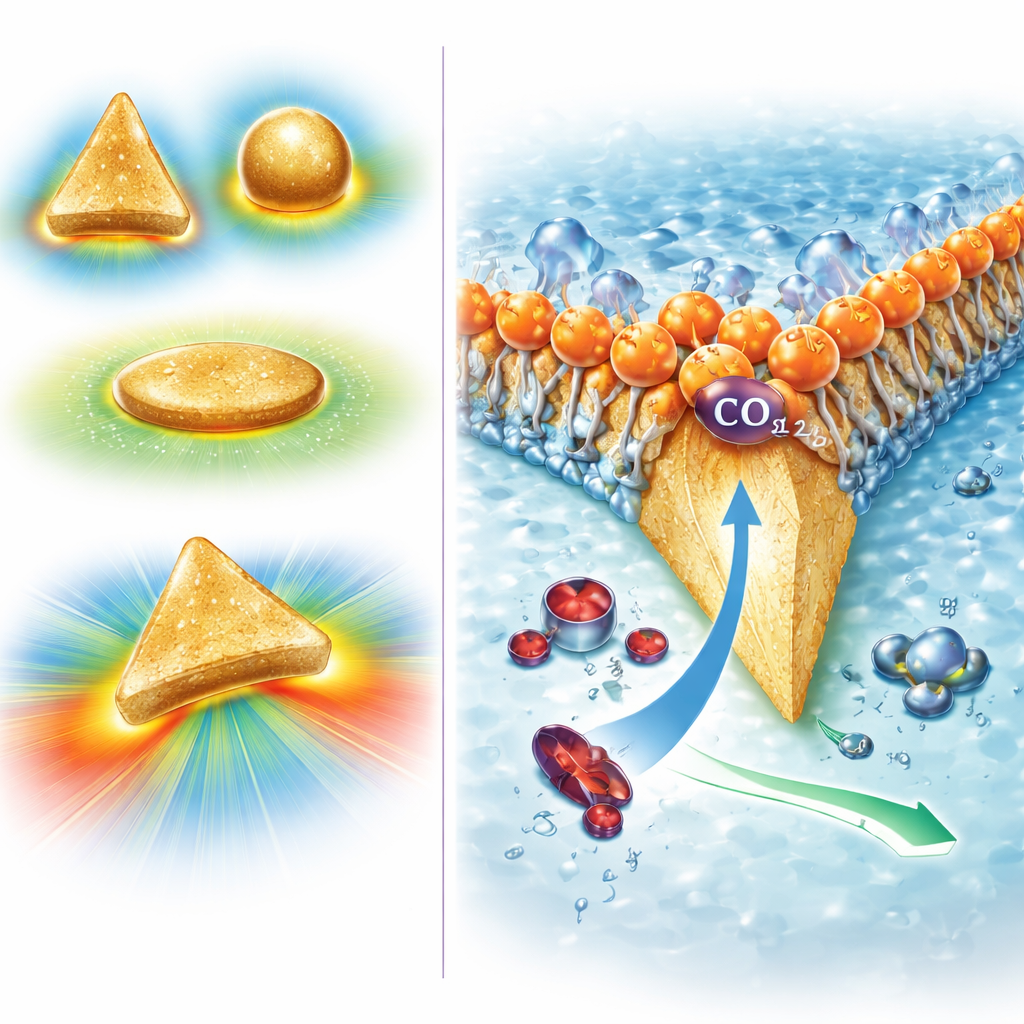
El equipo creó triángulos planos de oro diminutos de apenas unos 70 nanómetros de lado, con esquinas muy afiladas. Las simulaciones por ordenador mostraron que cuando se aplica un voltaje, la carga eléctrica se concentra en estas puntas afiladas, produciendo campos eléctricos locales extremadamente fuertes—aproximadamente diez veces más intensos que en partículas más redondeadas. Estos campos intensos distorsionan la nube electrónica de las moléculas de CO2 cercanas, transformándolas de especies no polares y simétricas en moléculas polarizadas con un dipolo medible. Esa distorsión estira y dobla ligeramente los enlaces carbono–oxígeno, lo que facilita que las moléculas se unan y se transformen en la superficie de oro. Cálculos y experimentos en conjunto indican que este efecto de campo hace que la adsorción del CO2 sea prácticamente espontánea y reduce la barrera energética para el paso clave inicial en su conversión a CO, de modo que la reacción avanza más rápido y con menor coste energético.
Un recubrimiento bioinspirado que bloquea protones
Para resolver el segundo problema—la formación excesiva de hidrógeno—los investigadores se inspiraron en las acuaporinas, proteínas en las membranas celulares de ciertos microorganismos acidófilos. Las acuaporinas permiten el paso de moléculas neutras de agua mientras bloquean protones mediante cargas positivas colocadas con precisión. Imitando esta idea, los autores recubrieron sus nanotriángulos de oro con una capa de un tensioactivo cargado positivamente llamado CTAC. Esta capa forma una cubierta blanda y ordenada cuyos grupos cabeza cargados repelen los protones entrantes pero no obstaculizan al CO2 neutro. Los experimentos mostraron que cuando está presente este recubrimiento catiónico, casi toda la corriente eléctrica se destina a producir CO en lugar de hidrógeno, mientras que el oro desnudo o recubierto de forma distinta produce mucho más hidrógeno. Los modelos computacionales confirmaron que la capa cargada ralentiza el transporte de protones, eleva el pH local justo al lado del catalizador y, por tanto, suprime la reacción secundaria.
Rendimiento que perdura
Cuando los triángulos afilados de oro con recubrimiento de CTAC se probaron en un electrolizador de flujo a pH 1, produjeron CO con casi un 100% de selectividad en un amplio rango de voltajes y siguieron funcionando durante al menos 100 horas a alta densidad de corriente. La eficiencia energética alcanzó alrededor del 60%, lo que es competitivo o superior al de muchos sistemas que dependen de sales metálicas en entornos menos ácidos. Las comparaciones con formas de oro más lisas y con versiones de los triángulos con puntas «redondeadas» mostraron que tanto la forma triangular bidimensional como, de manera crucial, las esquinas afiladas son necesarias para alcanzar este rendimiento. El trabajo demuestra una verdadera sinergia: los campos eléctricos potenciados por la geometría atraen y activan el CO2, mientras que el recubrimiento cargado bioinspirado moldea la química local para mantener alejados a los protones.
Qué significa esto para futuros dispositivos de energía limpia
Para el público general no especializado, el mensaje principal es que esta investigación ofrece una nueva receta para convertir CO2 en una materia prima útil en condiciones que antes parecían desfavorables. Al tomar ideas de la biología y explotar la física de las puntas afiladas, los autores muestran que es posible llevar a cabo la conversión de CO2 en ácido fuerte sin iones metálicos añadidos, evitando la acumulación de sales y mejorando el aprovechamiento del CO2. Si se escala e integra con energía renovable, tales catalizadores podrían ayudar a transformar el CO2 de un residuo en un bloque de construcción para combustibles y productos químicos con neutralidad de carbono, además de hacer los dispositivos electroquímicos más robustos y fáciles de operar.
Cita: Chen, L., Guo, Z., Huang, HZ. et al. Electric-field-driven CO2 polarization and bioinspired proton blocking unlock CO2 reduction in strong acid without metal cations. Nat Commun 17, 1734 (2026). https://doi.org/10.1038/s41467-026-68435-y
Palabras clave: Electrorreducción de CO2, electrolizador ácido, nanocatalizador de oro, potenciación del campo eléctrico, bloqueo de protones