Clear Sky Science · es
Mejora del knockout génico in vivo con alta especificidad usando sgRNAs multiplexadas de Cas12a
Editar genes de forma más fiable
La edición genética promete nuevas maneras de estudiar la biología, tratar enfermedades e incluso controlar plagas de insectos, pero en animales reales a menudo funciona con menos limpieza de la que sugieren los titulares. Muchas células eluden la edición o quedan solo parcialmente alteradas, lo que puede empañar los resultados experimentales y limitar su uso en el mundo real. Este artículo describe un nuevo método basado en CRISPR en moscas de la fruta que hace que los knockouts génicos sean más completos y precisos, ofreciendo un modelo para una edición del genoma más fiable en organismos complejos.
Por qué el CRISPR estándar a menudo se queda corto
Las herramientas CRISPR tradicionales, como Cas9, cortan el ADN en un punto elegido usando una sola o pocas ARN guía. En animales vivos, este enfoque enfrenta varios obstáculos. Algunas guías simplemente funcionan mal; algunos sitios diana son difíciles de alcanzar para la enzima; y la maquinaria de reparación celular con frecuencia “arregla” la rotura con cambios mínimos que dejan al gen todavía funcional. El resultado es un mosaico: células vecinas en el mismo tejido pueden portar mutaciones diferentes, o ninguna. Esa heterogeneidad dificulta ver qué ocurre cuando un gen está realmente inactivado y plantea un reto para aplicaciones como la terapia génica o los drives genéticos, que deben actuar de forma eficiente en la mayoría de las células.
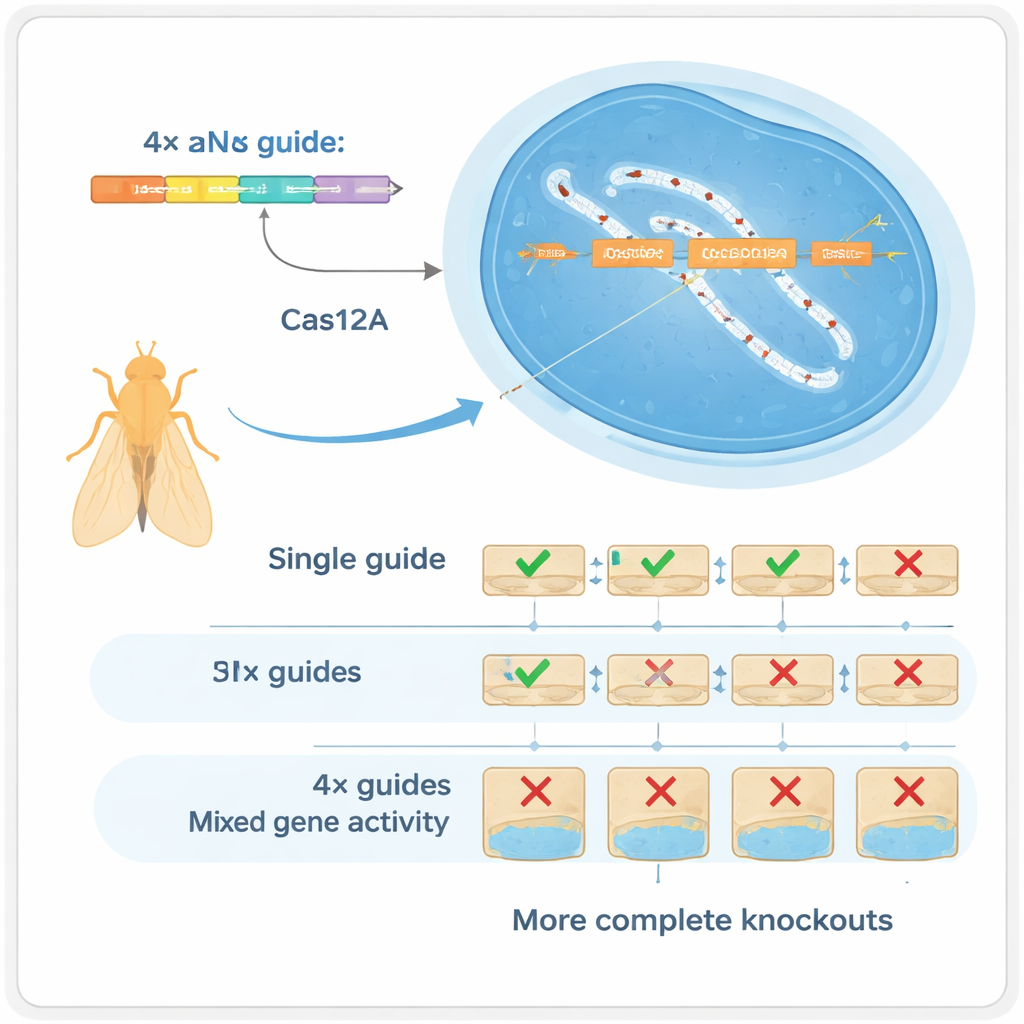
Cuatro guías son mejores que una
Los autores se decantaron por otra enzima CRISPR, Cas12a, que puede procesar matrices compactas de guías con mucha más facilidad que Cas9. Construyeron un kit para Drosophila en el que cada gen es atacado por una matriz de cuatro ARN guía, todos codificados en un único fragmento de ADN pequeño que puede producirse en masa. En pruebas cuidadosamente controladas, mostraron que usar cuatro guías por gen cambia drásticamente el tipo de cambios en el ADN: en lugar de pequeñas inserciones o deleciones en un único sitio, el sistema suele generar deleciones mayores entre sitios de corte que casi siempre destruyen la función génica. Esta “multiplexación” funciona en dos sentidos: si una guía falla, las demás pueden completar la tarea (redundancia), y cuando varias cortan a la vez pueden eliminar trozos mayores del gen (sinergia).
Alta eficiencia sin daño colateral adicional
Crear más rupturas en el ADN plantea preguntas obvias de seguridad. ¿Podrían múltiples cortes en una región borrar accidentalmente genes cercanos? ¿Podrían las guías fallar en otros lugares del genoma con más frecuencia? Para responder, los investigadores midieron la muerte celular, evaluaron efectos en genes vecinos e inventaron un ensayo ingenioso para visualizar eventos de reparación cromosómica denominado pérdida de heterocigosidad a lo largo de grandes tramos de ADN. Encontraron que agrupar cuatro cortes dentro de un mismo gen fue bien tolerado: no aumentó la muerte celular comparado con los enfoques convencionales con Cas9 y rara vez perturbó genes vecinos, salvo cuando una guía caía extremadamente cerca de un elemento regulador. Cribados a gran escala usando más de 2.000 guías en un tercio del genoma de la mosca mostraron que más del 99% de las matrices de guías estaban activas en su objetivo previsto, mientras que la actividad fuera de objetivo reproducible fue inferior al 1%, lo que indica una especificidad muy alta incluso en un montaje multiplexado.
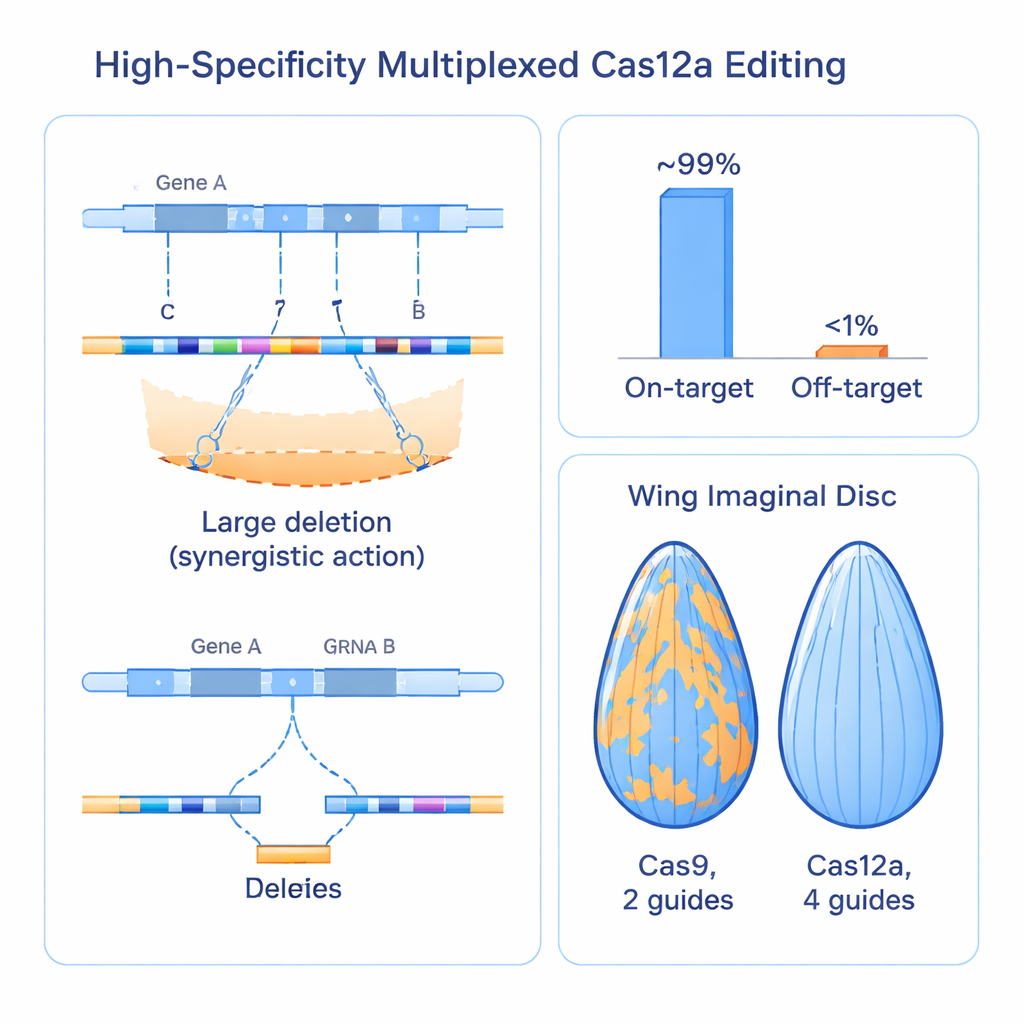
Superando a los sistemas Cas9 establecidos en tejidos reales
Para ver si estas mejoras moleculares se traducen en una biología más clara, el equipo comparó su sistema Cas12a con cuatro guías directamente frente a recursos basados en Cas9 ampliamente utilizados, apuntando a más de 100 genes en la mosca. En tejidos como el ojo, el intestino y la ala en desarrollo, el enfoque con Cas12a produjo efectos de pérdida de función más fuertes y uniformes que Cas9, que a menudo dejaba parches evidentes de tejido no editado y normal. Cuando usaron el tamaño del ala como medida cuantitativa, el nuevo sistema generó de forma consistente defectos de crecimiento mayores y más reproducibles para reguladores conocidos, revelando que algunos genes previamente catalogados como débiles o no esenciales en realidad habían sido pasados por alto porque las herramientas antiguas no los inactivaban lo suficiente. La mayor potencia del método incluso sacó a la luz un papel esencial previamente desconocido para un gen llamado trade embargo en el desarrollo y supervivencia del ala.
Qué significa esto para la futura edición génica
En términos sencillos, este trabajo muestra cómo convertir el CRISPR de un escalpelo a veces impreciso en un interruptor más decisivo para apagar genes en animales vivos. Al combinar Cas12a con cuatro guías por gen, los autores logran knockouts casi completos con efectos no deseados muy bajos, todo en un formato práctico de escalar a cientos de genes. Aunque desarrollado en moscas de la fruta, los principios subyacentes —usar múltiples guías para redundancia y sinergia, y comprobar cuidadosamente los efectos cromosómicos secundarios— son de aplicación general. Esta estrategia podría mejorar la investigación básica, afinar los cribados genéticos e informar diseños más seguros para futuras aplicaciones médicas y ecológicas de la edición genética.
Cita: Port, F., Buhmann, M.A., Zhou, J. et al. Improved in vivo gene knockout with high specificity using multiplexed Cas12a sgRNAs. Nat Commun 17, 877 (2026). https://doi.org/10.1038/s41467-026-68434-z
Palabras clave: CRISPR, Cas12a, knockout génico, Drosophila, especificidad en la edición del genoma