Clear Sky Science · es
Control del reclutamiento de la telomerasa y protección de los extremos por componentes independientes de shelterin
Cómo las células mantienen seguros los extremos de sus cromosomas
Cada vez que una célula se divide, las puntas de sus cromosomas—llamadas telómeros—se recortan un poco. Para evitar perder información genética vital, las células emplean una enzima especial, la telomerasa, y un conjunto de proteínas protectoras para mantener esos extremos. Este estudio explora cómo dos de esas proteínas, TPP1 y POT1, gestionan el delicado equilibrio entre permitir la entrada de la telomerasa para reconstruir los telómeros y mantener los extremos cromosómicos sellados y protegidos frente al daño.
El problema de los extremos cromosómicos que envejecen
Los telómeros actúan como las puntas de plástico en los cordones de los zapatos, evitando que los cromosomas se deshilachen o se confundan con ADN roto. Si la célula interpreta por error un extremo cromosómico como un daño, puede activar sistemas de reparación de emergencia que pegan cromosomas entre sí o impiden que las células se dividan. Al mismo tiempo, los telómeros deben abrirse ocasionalmente para que la telomerasa pueda alargarlos, especialmente en células madre que se dividen muchas veces. Los biólogos han imaginado desde hace tiempo que los telómeros alternan entre un estado «cerrado» protegido y un estado «abierto» que permite el acceso de la telomerasa pero conlleva el riesgo de señales de daño temporales. Si estos dos estados reflejan distintas formas físicas del telómero o realmente mecanismos de control separados ha sido una cuestión abierta.
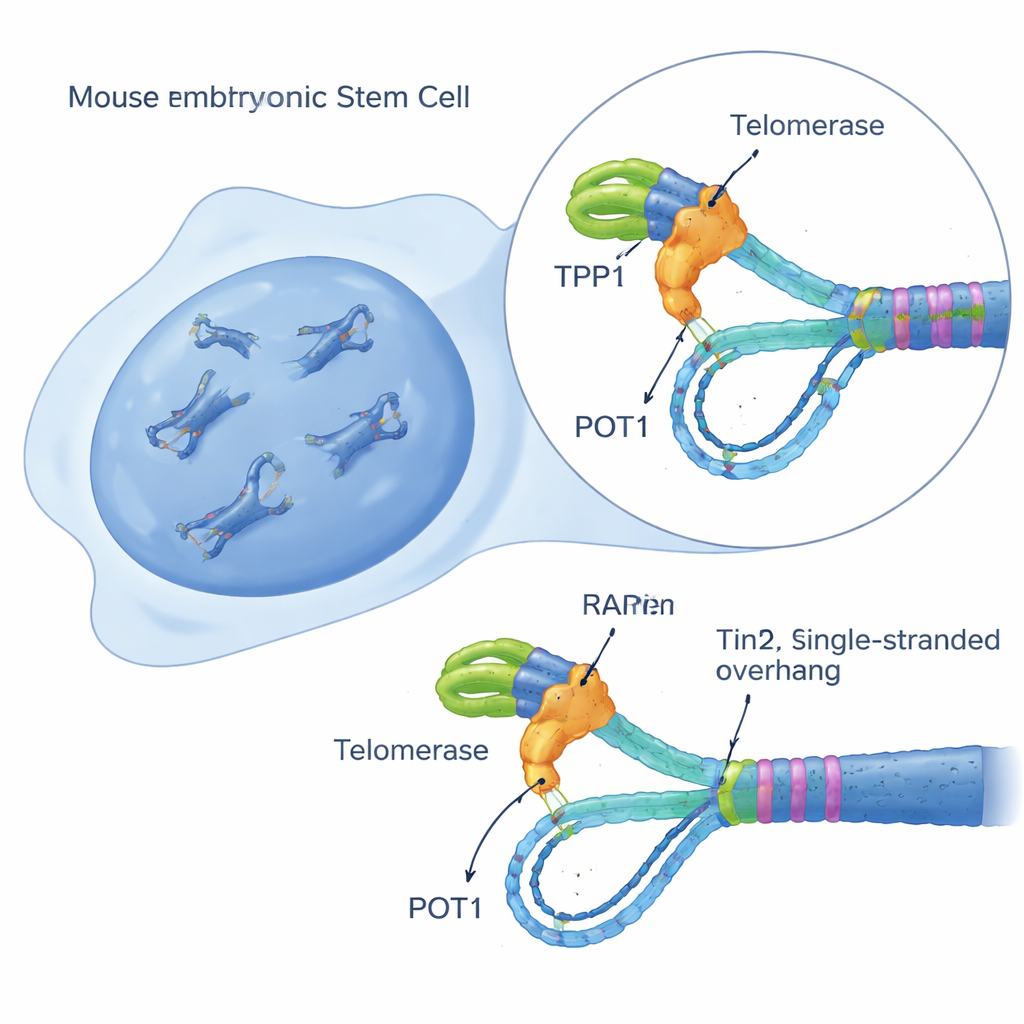
Construir un sensor de actividad de la telomerasa en una sola célula
Para desenmarañar este rompecabezas, los investigadores crearon una prueba sensible en células vivas, llamada iTAP (inducible Telomerase Activity Probing), en células madre embrionarias de ratón. Modificaron genéticamente las células para que produjeran una versión ligeramente alterada del ARN plantilla de la telomerasa solo cuando se les administraba el fármaco doxiciclina. Esta plantilla «mutante» provoca que la telomerasa añada una secuencia de ADN modificada en los telómeros que puede distinguirse visualmente del ADN telomérico normal. Mediante sondas fluorescentes, blots de ADN y un método de secuenciación que enriquece fragmentos teloméricos, el equipo pudo ver directamente, célula por célula, cuándo y dónde estaba activa la telomerasa. Crucialmente, este sistema no dañó el crecimiento celular ni provocó por sí mismo una respuesta de daño, lo que permitió mediciones limpias del comportamiento de la telomerasa en células por lo demás sanas.
TPP1 recluta la telomerasa, POT1 la frena
Con iTAP, los autores probaron cómo dos proteínas teloméricas clave, TPP1 y POT1, contribuyen a la acción de la telomerasa. Ambas pertenecen a un complejo mayor conocido como shelterin, que recubre los telómeros. Cuando eliminaron TPP1 usando herramientas de edición genética, las secuencias teloméricas mutantes casi desaparecieron, a pesar de que el ARN mutante de la telomerasa seguía produciéndose a niveles normales. Experimentos adicionales mostraron que TPP1 debe enlazarse físicamente con otro componente de shelterin, TIN2, para reclutar la telomerasa; interrumpir la conexión de TPP1 con TIN2 inhibió la actividad de la telomerasa. Sorprendentemente, romper la interacción de TPP1 con POT1 no tuvo ese efecto, y la eliminación de POT1 en sí no redujo la acción de la telomerasa. De hecho, las células sin POT1 mostraron un aumento modesto en la cantidad de secuencia mutante añadida, lo que sugiere que POT1 actúa normalmente como un freno—limitando la frecuencia con la que la telomerasa se asocia a los telómeros, en lugar de ayudarla.
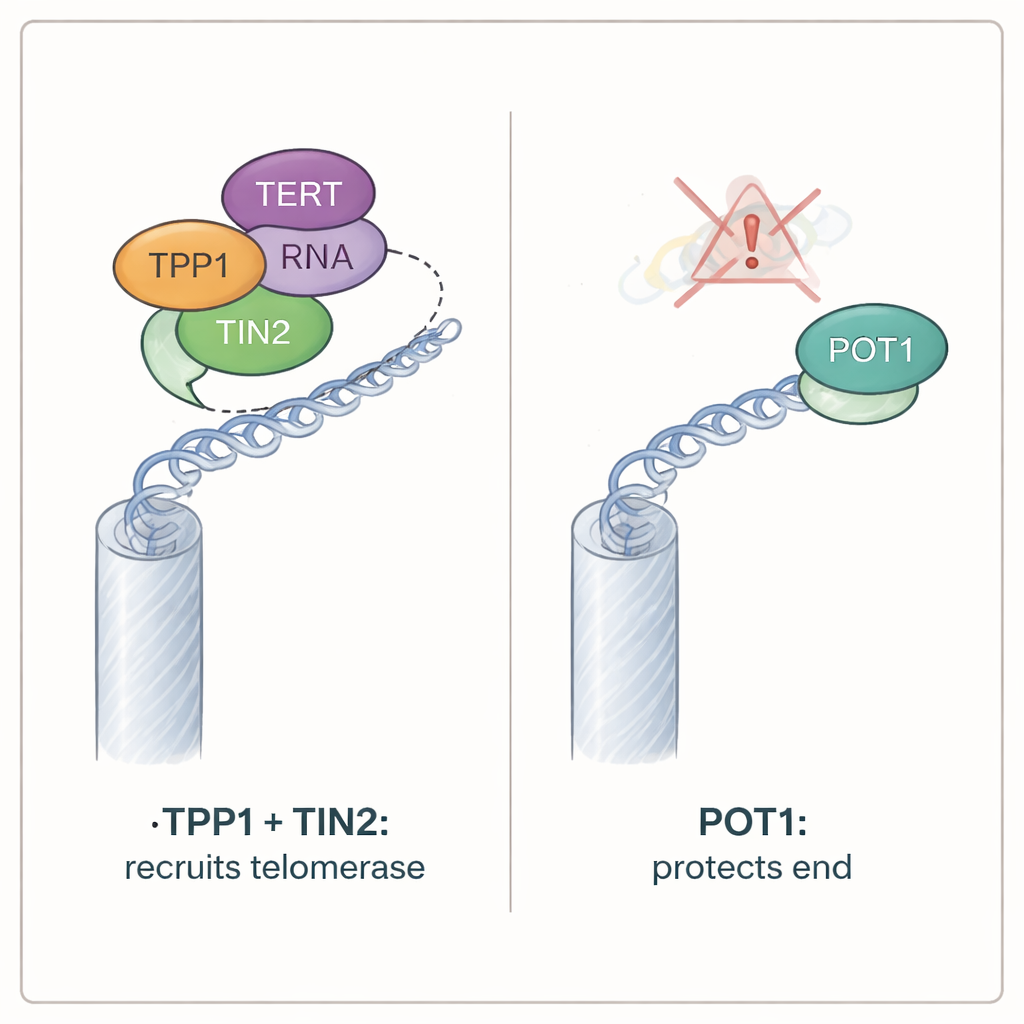
POT1 protege los extremos, mientras que TPP1 puede ser prescindible
Aunque POT1 no fue necesaria para el reclutamiento de la telomerasa, resultó vital para proteger los extremos cromosómicos. Las células que carecían de ambas versiones de POT1 en ratón dejaron de proliferar rápidamente y mostraron todos los signos de telómeros expuestos: marcadores de daño en el ADN se acumularon en las puntas cromosómicas, una enzima detectora de daño llamada ATR se activó y los extremos cromosómicos se fusionaron entre sí. En contraste, las células sin TPP1 continuaron creciendo y mostraron pocos indicios de estrés telomérico, a pesar de haber perdido la actividad telomérica normal. Pruebas adicionales mostraron que el papel defensivo de POT1 depende de su capacidad para unirse a la hebra simple sobresaliente en los telómeros. Proteínas POT1 mutantes que ya no podían agarrar ese ADN expuesto no lograron calmar las señales de daño, incluso si aún podían interactuar con TPP1. Por el contrario, variantes de POT1 que podían unirse a la sobrehendidura pero ya no se ligaban a TPP1 seguían protegiendo los extremos cromosómicos.
Una nueva visión modular del control de los telómeros
Estos hallazgos desmontan la imagen simplista de los telómeros alternando entre un único estado «abierto» para la telomerasa y un único estado «cerrado» para la protección. En su lugar, el estudio muestra que el reclutamiento de la telomerasa y la protección de los extremos están controlados por circuitos moleculares separables. TPP1, actuando a través de TIN2, es la principal puerta de entrada que trae la telomerasa a los telómeros, mientras que POT1 guarda de forma independiente el ADN expuesto en los extremos cromosómicos y mantiene a raya las respuestas al daño. Para el público general, la conclusión es que las células no dependen de un único interruptor universal en las puntas cromosómicas. Más bien, usan perillas separadas pero coordinadas—una para permitir la entrada de la telomerasa y otra para mantener los extremos seguros—para preservar la estabilidad del genoma a lo largo de la vida.
Cita: Sandhu, R., Tricola, G.M., Lee, S.Y. et al. Control of telomerase recruitment and end protection by independent shelterin components. Nat Commun 17, 1733 (2026). https://doi.org/10.1038/s41467-026-68433-0
Palabras clave: telómeros, telomerasa, células madre, daño en el ADN, protección de cromosomas