Clear Sky Science · es
Uso dinámico de alelos de genes ligados al X atenúa los fenotipos de enfermedades del neurodesarrollo en organoides cerebrales
Cómo el cromosoma X “silencioso” ayuda a proteger el cerebro
Cada célula de una mujer contiene dos cromosomas X, pero durante décadas los libros de biología han dicho que uno de ellos está mayormente apagado —como un libro de repuesto que se mantiene cerrado en una estantería. Este estudio muestra que, especialmente en el cerebro en desarrollo, ese X “silencioso” se parece más a una biblioteca de reserva dinámica. Puede activarse cuando hace falta, y esta flexibilidad adicional podría ayudar a explicar por qué muchos trastornos del desarrollo cerebral afectan con más gravedad a los varones que a las mujeres.
Un sistema de reserva oculto en el cromosoma X
En los mamíferos hembras, uno de los cromosomas X de cada célula se apaga temprano en el desarrollo para evitar una dosis doble de genes ligados al X. Sin embargo, los científicos llevan tiempo observando que algunos genes pueden escapar a ese apagado. El nuevo trabajo plantea una pregunta más profunda: ese escape, ¿es fijo o puede cambiar a medida que las células se desarrollan? Usando células madre humanas y tejidos cerebrales en miniatura llamados organoides, los investigadores siguieron qué copia de cada gen ligado al X —materna o paterna— se utilizaba a medida que las células maduraban de células madre a células nerviosas. Encontraron que muchos genes en el supuesto X inactivo se encienden y apagan de forma específica según la etapa y el tipo celular, en lugar de obedecer una regla simple de encendido/apagado.
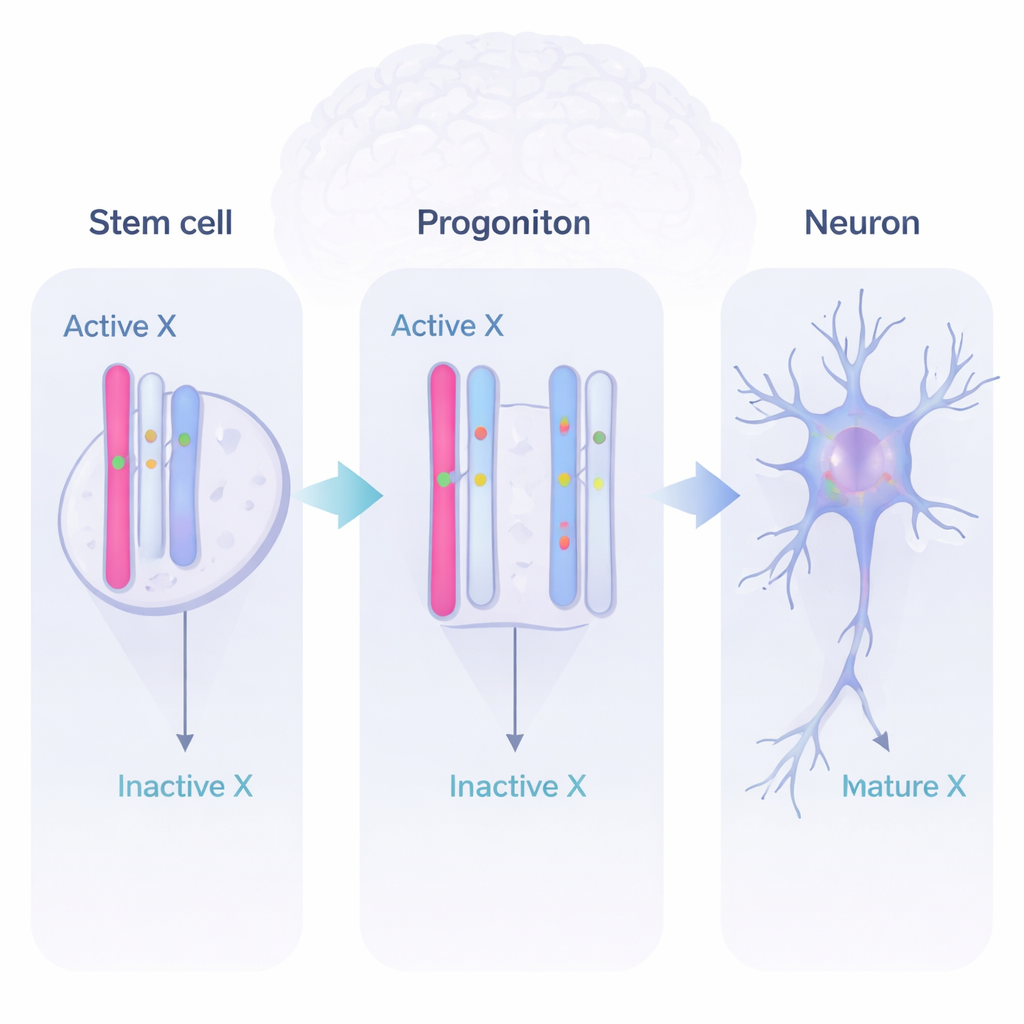
Uso dinámico de genes durante el desarrollo cerebral
Al leer el ARN (los mensajes producidos a partir de los genes) y distinguir entre las dos copias parentales, el equipo descubrió tres comportamientos principales. Algunos genes permanecieron en gran medida apagados en el X inactivo, como se esperaba. Otros fueron “completos escapistas”, activos desde ambas copias del X en todas las etapas. Y lo más intrigante: un grupo notable de genes fue dinámico. Esos genes estaban silentes en el X inactivo en las células madre, se activaban desde ambos cromosomas X en las células progenitoras neurales y en las neuronas tempranas, y después algunos se volvían a apagar más tarde. Esto demuestra que el X inactivo no es un cementerio estático de genes, sino un reservorio flexible del que el cerebro en desarrollo puede tirar cuando es útil contar con actividad génica adicional.
Patrones conservados y vínculos con trastornos cerebrales
Cuando los investigadores compararon sus datos humanos con estudios en ratón y con marcas químicas en el ADN de tejido cerebral fetal, hallaron que este escape dinámico de la inactivación del X se observa en otros mamíferos y está ligado a los estados de la cromatina —características del empaquetamiento del ADN que controlan con qué facilidad los genes pueden activarse. Los genes que se reactivaban tendían a agruparse en ciertas regiones del cromosoma X y mostraban firmas epigenéticas de ADN activo específicamente en tejido cerebral femenino. Importante para la medicina: estos genes reactivados dinámicamente eran inusualmente ricos en genes de riesgo conocidos para trastornos del neurodesarrollo, como la discapacidad intelectual y las condiciones del espectro autista, lo que sugiere que esta flexibilidad pudo haber evolucionado como un mecanismo protector.
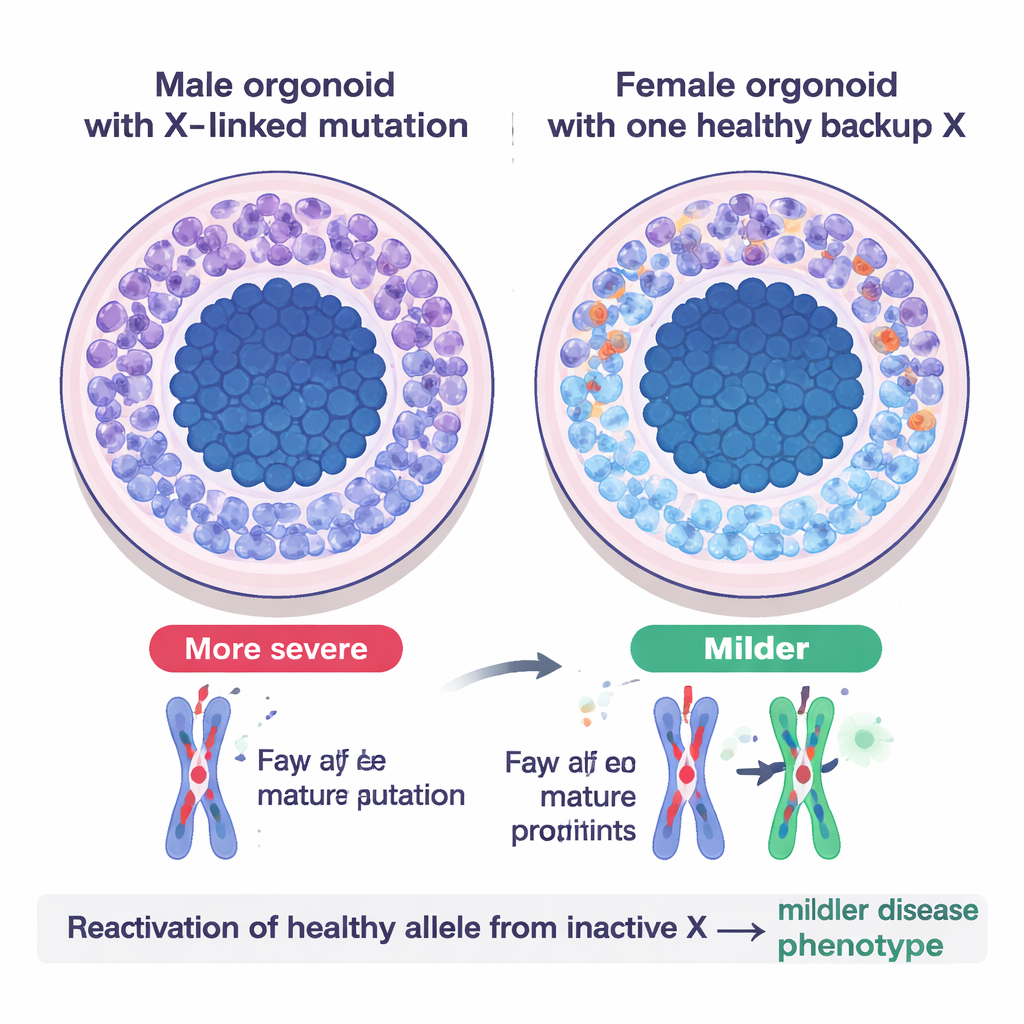
Una prueba en el mundo real: síndrome Opitz BBB/G
Para ver cómo funciona este sistema de reserva en la enfermedad, el equipo modeló el síndrome Opitz BBB/G, una condición ligada al X rara que afecta estructuras mediales del cerebro y con frecuencia causa retraso del desarrollo. El trastorno se debe a mutaciones dañinas en un gen llamado MID1 en el cromosoma X. En organoides cerebrales cultivados a partir de células de pacientes varones —donde sólo hay una copia del X— las neuronas eran escasas y las células madre neurales permanecían demasiado tiempo en un estado de división, reflejando la subcrecimiento cerebral observado en los pacientes. Los organoides femeninos con la misma mutación en su X activo, pero con una copia sana en el X inactivo, parecían notablemente más saludables: producían más neuronas y mostraban defectos menos graves. Cuando los científicos modificaron líneas femeninas para que ambas copias del X llevaran la mutación, los organoides desarrollaron problemas severos, similares a los masculinos, confirmando que el alelo sano previamente inactivo se había reactivado y estaba ayudando a compensar.
Qué significa esto para las diferencias sexuales en las enfermedades cerebrales
El estudio revela que el segundo cromosoma X “silencioso” en las mujeres no es simplemente lastre genético. Durante ventanas clave del desarrollo cerebral, genes seleccionados en este X inactivo se encienden en tipos celulares específicos, ampliando el conjunto de copias génicas funcionales. Para genes como MID1, que son cruciales para construir el cerebro, esta reactivación dinámica puede atenuar el impacto de mutaciones dañinas y producir síntomas más leves y variables en las mujeres. En otras palabras, los cerebros femeninos disponen de un sistema de reserva interno que puede ajustarse hacia arriba o hacia abajo con el tiempo, ayudando a explicar por qué muchos trastornos del neurodesarrollo ligados al X son menos frecuentes o menos graves en las niñas que en los niños.
Cita: Bertin, M., Todorov, H., Frank, S. et al. Dynamic allele usage of X-linked genes ameliorates neurodevelopmental disease phenotypes in brain organoids. Nat Commun 17, 599 (2026). https://doi.org/10.1038/s41467-026-68428-x
Palabras clave: inactivación del cromosoma X, organoides cerebrales, trastornos del neurodesarrollo, dosificación génica, diferencias sexuales en la enfermedad