Clear Sky Science · es
Shigella flexneri elude la inmunidad intracelular mediada por septinas mediante ADP-riboxanación de proteínas
Cómo algunas bacterias intestinales se escabullen de nuestro sistema de seguridad interno
La diarrea grave causada por bacterias del género Shigella sigue siendo un problema importante en todo el mundo, sobre todo entre los niños pequeños. Nuestras células no están indefensas: disponen de herramientas incorporadas que pueden atrapar y destruir microbios invasores. Este estudio revela cómo Shigella flexneri, una de las principales causas de disentería, emplea trucos moleculares para desmantelar una de esas herramientas, favoreciendo la difusión bacteriana de célula a célula en el intestino.
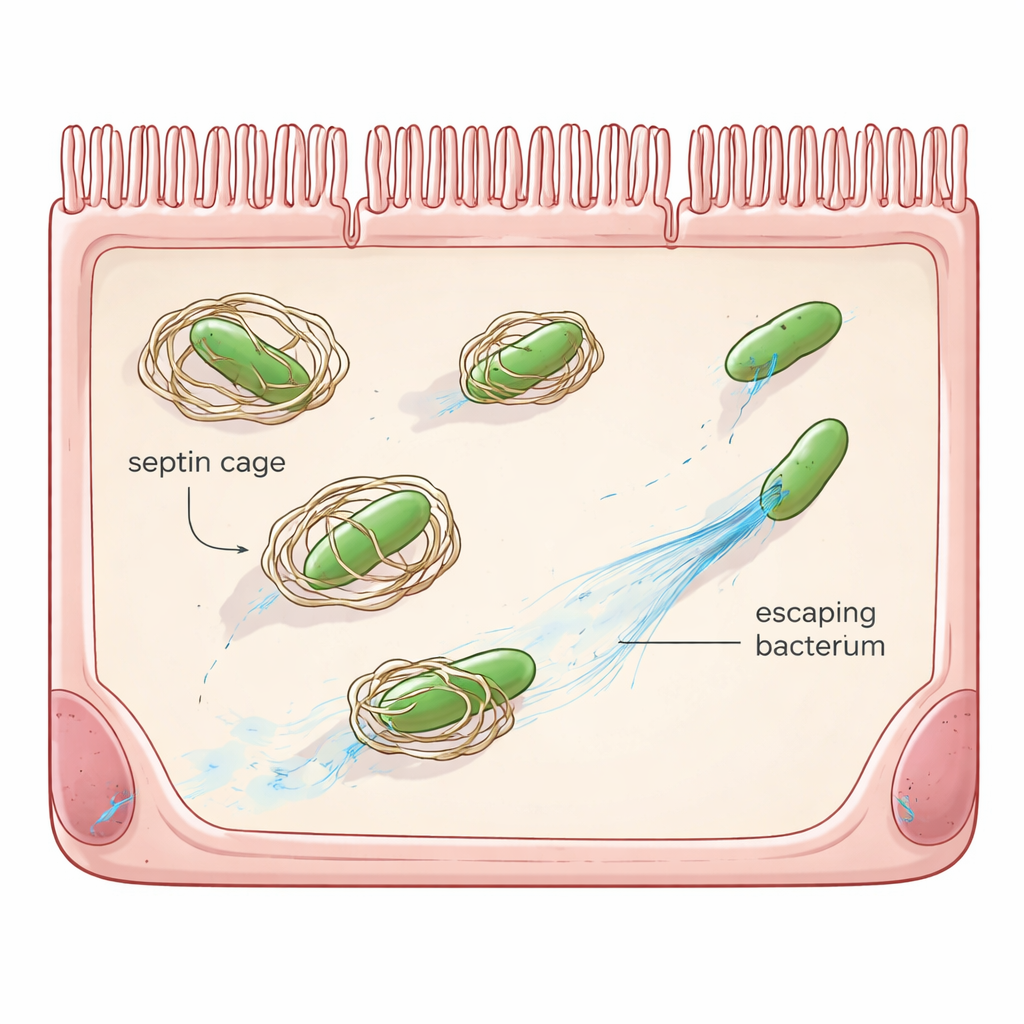
La defensa “hazlo tú mismo” de la célula
Más allá de los glóbulos blancos y los anticuerpos, muchas células ordinarias disponen de sus propios sistemas de emergencia, conocidos como inmunidad celular autónoma. Uno de esos sistemas depende de las septinas, una familia de proteínas andamiaje que forman anillos y estructuras en jaula. Cuando Shigella entra en una célula y escapa al interior gelatinoso, las septinas pueden ensamblarse alrededor de la bacteria, bloqueando su capacidad de moverse y marcándola para su destrucción por vías celulares de reciclaje. Trabajos anteriores mostraron que Shigella ya dispone de una contramedida, una proteína llamada OspG, que etiqueta a las septinas para su eliminación. Sin embargo, incluso cuando falta OspG, la mayoría de las bacterias siguen evitando quedar enjauladas, lo que sugiere que Shigella posee trucos adicionales.
Desenmascarando a un segundo saboteador bacteriano
Los autores dirigieron su atención a otro grupo de proteínas de Shigella, conocido como la familia OspC. Mediante un enfoque global de cartografía proteica en células humanas, buscaron proteínas del huésped que se modificaran químicamente en presencia de proteínas OspC. Junto a dianas ya conocidas implicadas en la síntesis proteica, encontraron que varias septinas, especialmente una llamada SEPT9, quedaban sistemáticamente marcadas. Pruebas bioquímicas detalladas mostraron que tres proteínas OspC pueden unir directamente una pequeña etiqueta rica en energía, derivada de la molécula NAD, a múltiples sitios en las septinas. Este cambio químico, denominado ADP-riboxanación, es una variante especial e irreversible de una modificación proteica más común.
Rompiendo el andamiaje proteico desde dentro
Para entender cómo esta etiqueta química debilita las defensas celulares, el equipo se centró en SEPT9. Las septinas normalmente forman cadenas ordenadas de ocho subunidades, que luego se alinean en filamentos y finalmente constituyen jaulas completas alrededor de las bacterias. Los investigadores descubrieron que una posición concreta en SEPT9, un aminoácido llamado arginina 561, es el principal sitio de ADP-riboxanación durante la infección. Trabajos estructurales y experimentos de reconstrucción con proteínas purificadas mostraron que este sitio se encuentra en una superficie de contacto crítica donde dos unidades de SEPT9 se encajan. Cuando esa arginina se modifica químicamente —o se sustituye por un residuo que imita la carga negativa añadida— las cadenas octaméricas se desmoronan en piezas más pequeñas y ya no pueden formar filamentos estables.
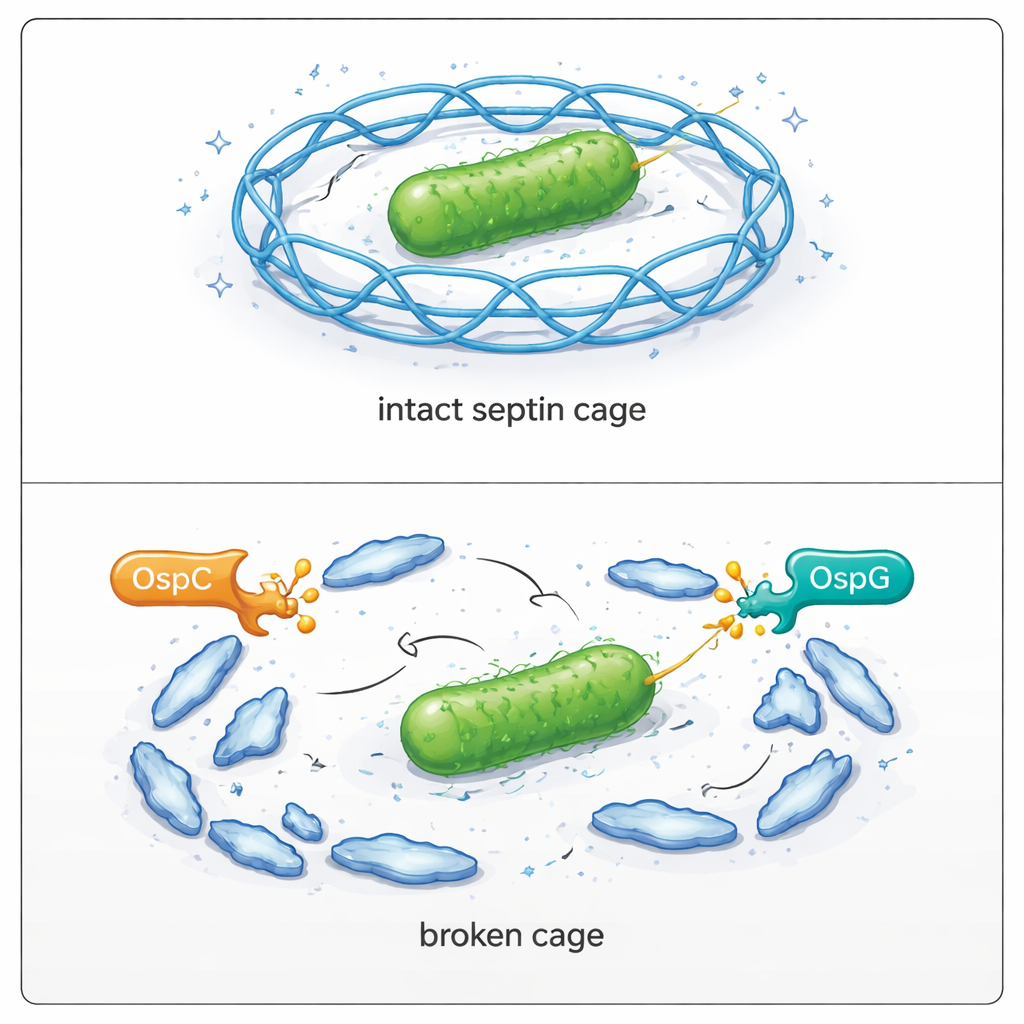
Viendo fallar las jaulas dentro de células infectadas
El equipo volvió a las células vivas para observar las consecuencias. En células humanas infectadas con Shigella normal, solo una minoría de bacterias quedaba dentro de jaulas de septinas. Cuando se eliminaron genéticamente todas las proteínas OspC, la fracción de bacterias enjauladas casi se duplicó. La eliminación de OspG produjo un efecto similar, y la eliminación conjunta de OspC y OspG aumentó aún más la formación de jaulas y perjudicó gravemente la capacidad de las bacterias para propagarse a través de una monocapa celular. La reintroducción de OspC activos en las cepas mutantes restauró su escape de las jaulas y su capacidad para replicarse y formar grandes placas. La microscopía confirmó que cuando SEPT9 no puede modificarse en la arginina 561, se incorpora a las jaulas de forma eficiente; cuando es alterada por OspC, la formación de jaulas alrededor de las bacterias cae drásticamente.
Qué significa esto para combatir Shigella
En términos accesibles, este trabajo muestra que Shigella porta un par combinado de herramientas moleculares diseñadas para abrir las rejas de una “cárcel” intracelular. OspC debilita directamente los bloques proteicos necesarios para construir jaulas de septinas, mientras que OspG favorece su eliminación vía otra ruta química. Juntas, estas estrategias permiten a las bacterias liberarse, moverse dentro de las células e invadir las vecinas. Entender estos mecanismos de escape precisos no solo profundiza nuestra comprensión de cómo funciona la inmunidad intrínseca celular, sino que también señala nuevos ángulos terapéuticos: fármacos que bloqueen OspC o protejan contactos clave de las septinas podrían ayudar a restaurar la capacidad natural de la célula para atrapar y eliminar este patógeno peligroso.
Cita: Tang, Z., Xian, W., Özbaykal Güler, G. et al. Shigella flexneri evades septin-mediated cell-autonomous immunity via protein ADP-riboxanation. Nat Commun 17, 1727 (2026). https://doi.org/10.1038/s41467-026-68425-0
Palabras clave: Shigella, jaulas de septinas, inmunidad celular autónoma, factores de virulencia bacteriana, ADP-ribosilación