Clear Sky Science · es
Productos naturales peptídicos dirigidos a ClpC1 desregulan diferencialmente el proteoma de Mycobacterium tuberculosis
Por qué importa desactivar los equipos de limpieza bacterianos
La tuberculosis sigue siendo una de las enfermedades infecciosas más mortales del mundo, y las cepas de Mycobacterium tuberculosis resistentes a fármacos dificultan cada vez más su tratamiento. La mayoría de los antibióticos existentes atacan la pared celular de la bacteria o su capacidad para generar energía y copiar material genético. Este estudio explora un punto débil muy distinto: el “equipo de limpieza” interno de la célula que mantiene la salud de las proteínas. Al comprender cómo nuevas moléculas derivadas de productos naturales perturban este sistema de mantenimiento, los científicos esperan diseñar futuros fármacos capaces de matar las bacterias de la tuberculosis de maneras nuevas y más duraderas.
El centro de mantenimiento de proteínas de la célula
Como todas las células vivas, la bacteria de la TB construye, pliega, repara y recicla constantemente sus proteínas. Un actor central en esta red de mantenimiento proteico es una gran máquina llamada complejo ClpC1–ClpP1P2. Una de sus partes (ClpC1) actúa como chaperona, reconociendo y atrayendo proteínas dañadas o innecesarias, mientras que la otra parte (ClpP1P2) las corta en fragmentos para su reciclaje. Este sistema es esencial para la supervivencia de la bacteria, especialmente bajo estrés, como calor o ataque por antibióticos. Varios péptidos naturales—ecumicina, ilamicinas (rufomicinas) y ciclomarinas—ya se sabe que se unen a ClpC1 y muestran fuerte actividad bactericida contra la TB, lo que sugiere que este complejo podría ser un objetivo farmacológico potente. 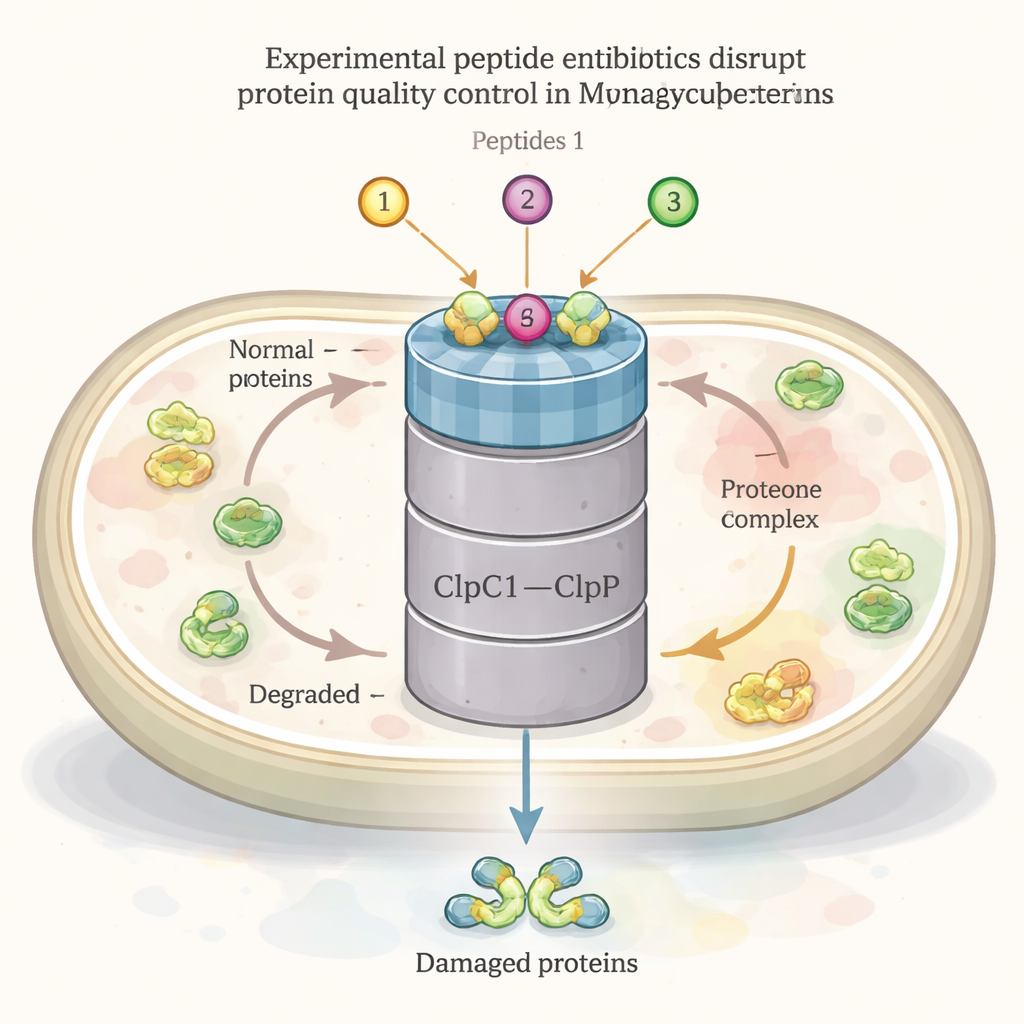
Tres fármacos emparentados, tres impactos distintos
Los investigadores examinaron un representante de cada una de las tres familias de péptidos: un análogo de ecumicina (Ecu*), ilamicina E (IlaE) y un derivado de ciclomarina (desoxiciclomarin, dCym). Aunque los tres se unen a la misma región de ClpC1, no se comportan igual dentro de la célula. Usando proteómica cuantitativa—un enfoque que mide miles de proteínas a la vez—encontraron que Ecu* causó la mayor perturbación, alterando significativamente los niveles de casi el 17% de todas las proteínas bacterianas. IlaE cambió alrededor del 12% y dCym alrededor del 7%. Solo 72 proteínas se vieron afectadas de forma consistente por los tres compuestos, y la mayoría de ellas disminuyeron en abundancia. Esto muestra que cada molécula empuja la máquina ClpC1 en una dirección distinta, remodelando el paisaje proteico celular de maneras particulares en lugar de simplemente “apagar la máquina”.
Obstruir la trituradora frente a cortar la energía
Para poner estos efectos en contexto, el equipo comparó los péptidos con bortezomib, un fármaco contra el cáncer que bloquea de forma amplia las enzimas degradadoras de proteínas. En las bacterias de TB, el bortezomib causó una acumulación general de muchas proteínas, como cabría esperar cuando las trituradoras se apagan. En contraste, los péptidos produjeron patrones más selectivos: algunos objetivos conocidos de ClpC1 se acumularon, otros se redujeron, y no se observó una inhibición global de toda la degradación proteica. Ensayos detallados con componentes purificados mostraron que cada péptido alteró cómo se procesaban sustratos específicos. Por ejemplo, los tres interfirieron con la destrucción de una proteína reguladora (PanD), pero solo Ecu* bloqueó la degradación de una proteína modelo desordenada, y solo dCym perjudicó la degradación de la proteína protectora frente al estrés Hsp20. Estas diferencias sugieren que la forma global y la flexibilidad de cada proteína objetivo influyen en cómo se ve afectada cuando ClpC1 queda “desajustado” por un compuesto dado. 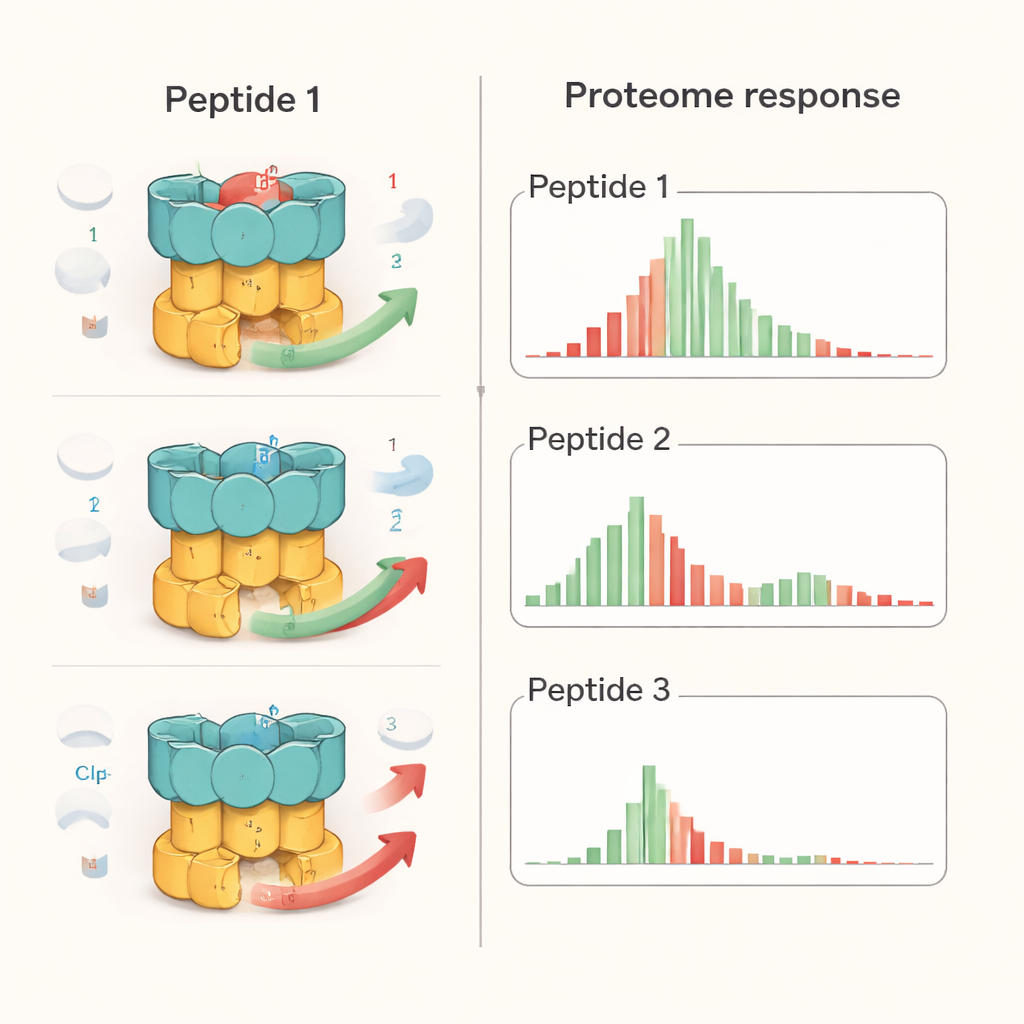
Respondedores al estrés y la auto-rescate bacteriano
La bacteria de la TB dispone de sistemas de respaldo para afrontar cuando el daño proteico supera a la maquinaria principal de limpieza. Uno de esos sistemas implica otra chaperona, ClpC2, que puede unirse a moléculas tipo ciclomarina y reducir su impacto en ClpC1. Este estudio encontró que, aunque los tres péptidos pueden unirse a ClpC2 en probeta, solo el derivado de ciclomarina (dCym) provocó realmente un aumento de los niveles de ClpC2 en bacterias vivas y se volvió más potente cuando ClpC2 se redujo experimentalmente. En contraste, Ecu* e IlaE siguieron siendo efectivos incluso cuando ClpC2 se reprimió, lo que sugiere que en gran medida evitan esta vía de auto-rescate. El equipo también descubrió una conexión fuerte y específica por compuesto con Hsp20, una pequeña proteína que ayuda a prevenir agregados dañinos: Ecu* (y en menor medida IlaE) provocó aumentos drásticos en los niveles de Hsp20, y Ecu* se unió directamente a Hsp20, revelando una nueva relación entre estos candidatos a fármaco y la red de respuesta al estrés de la célula.
Convertir el estrés en una ventaja terapéutica
Dado que el sistema ClpC1 es especialmente importante en condiciones adversas, los investigadores probaron los fármacos mientras las bacterias estaban sometidas a un estrés térmico leve, que aumenta la carga de proteínas mal plegadas. Bajo estas condiciones, tanto Ecu* como dCym se volvieron mucho más letales, alcanzando una toxicidad similar a la del bortezomib, aun cuando actúan de forma más selectiva. Esto demuestra que atacar con precisión la maquinaria de control de calidad de proteínas puede ser tan eficaz como apagar todas las proteasas principales, pero con un control potencialmente más fino. El trabajo también mostró que muchos de los cambios provocados por Ecu* en los niveles proteicos no se correspondieron simplemente con cambios en la actividad génica, subrayando que la perturbación de ClpC1 altera fundamentalmente la regulación postraduccional de las proteínas.
Qué significa esto para futuros tratamientos contra la TB
Para quienes no son especialistas, el mensaje clave es que las bacterias de la TB dependen de un sistema interno de limpieza y respuesta al estrés finamente equilibrado para sobrevivir. Los tres péptidos derivados de productos naturales probados aquí se enganchan a la misma máquina central, pero la empujan hacia modos distintos, provocando distorsiones diversas y muy específicas en la composición proteica de la bacteria. Importante: los compuestos tipo ecumicina e ilamicina evitan un mecanismo bacteriano de rescate incorporado que puede mitigar el efecto de la ciclomarina, y aun así paralizan al patógeno bajo estrés. Estas propiedades los convierten en andamios prometedores para futuros fármacos contra la tuberculosis, incluidos moléculas diseñadas que podrían forzar a las células de TB a destruir selectivamente sus propias proteínas vitales o bien integrarse en “quiméricos dirigidos a proteínas” para dirigir con precisión la autodegradación bacteriana.
Cita: Barter, I.K., Bedding, M.J., Leodolter, J. et al. ClpC1-targeting peptide natural products differentially dysregulate the proteome of Mycobacterium tuberculosis. Nat Commun 17, 1725 (2026). https://doi.org/10.1038/s41467-026-68423-2
Palabras clave: tuberculosis, control de calidad de proteínas, ClpC1, resistencia a antibióticos, antibióticos derivados de productos naturales