Clear Sky Science · es
Perfilado epigenómico simultáneo y medición de actividad reguladora mediante e2MPRA
Leer los interruptores ocultos de la célula
Cada célula de tu cuerpo contiene esencialmente el mismo ADN, pero una célula cerebral y una hepática se comportan de formas muy distintas. El secreto está en tramos cortos de ADN que actúan como reguladores tipo atenuador para los genes, subiéndolos, bajándolos o apagándolos. Este estudio presenta una herramienta nueva y potente, llamada e2MPRA, que permite a los científicos probar miles de estos interruptores a la vez mientras observan cómo se empaqueta y marca el ADN dentro de la célula: pasos clave para comprender el desarrollo, el riesgo de enfermedad y por qué algunas variantes genéticas importan y otras no.
De los mapas del ADN a su función
En la última década, los investigadores han trazado enormes mapas de interruptores regulatorios “candidatos”, conocidos como elementos cis-regulatorios. Emplean métodos que muestran dónde el ADN está menos compactado (cromatina abierta), qué proteínas están unidas y qué marcas de histonas adornan el ADN circundante. Esos mapas son impresionantes, pero en su mayoría son descriptivos: que una proteína se una o que aparezca una marca no demuestra que una secuencia controle realmente la actividad génica. Los ensayos tradicionales de reportero masivamente paralelos (MPRAs) pueden probar si miles de fragmentos de ADN aumentan o silencian un gen reportero, pero no nos dicen qué proteínas se unen allí ni qué cambios epigenéticos acompañan esa actividad.
Un ensayo doble para actividad y marcas epigenéticas
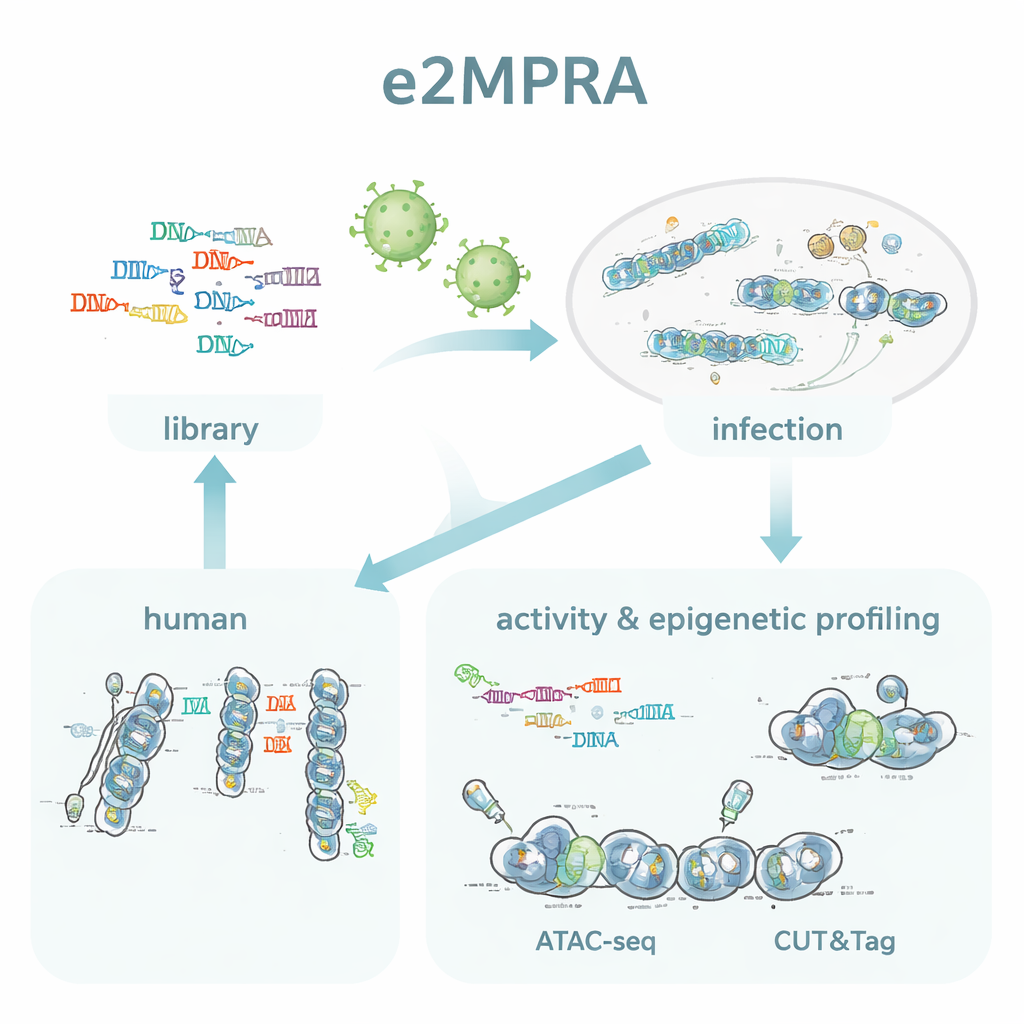
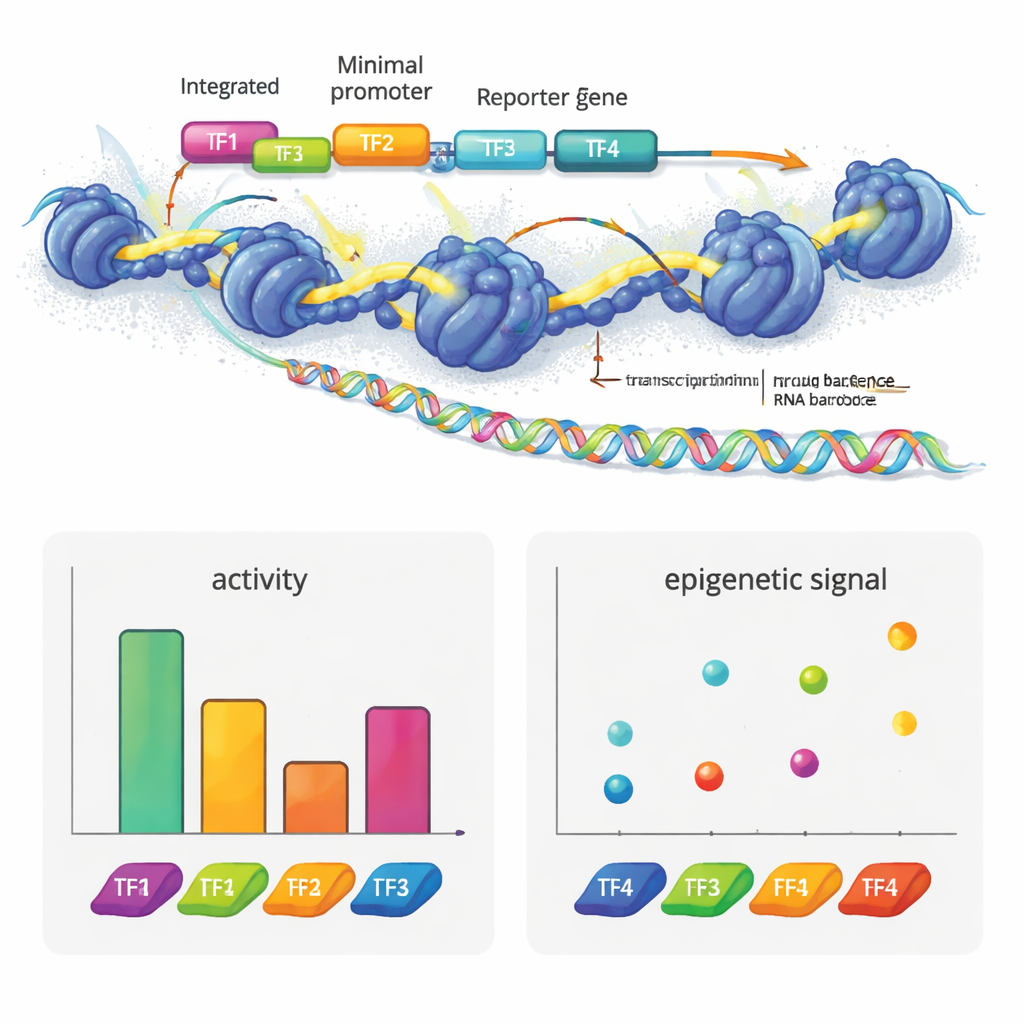
Los autores crearon e2MPRA combinando un MPRA lentiviral con dos técnicas epigenómicas, ATAC-seq y CUT&Tag. Primero construyen una biblioteca de ADN en la que cada secuencia reguladora candidata se enlaza a un código de barras corto y se coloca junto a un promotor mínimo y un gen reportero. Esta biblioteca se empaqueta en lentivirus y se integra múltiples veces en los genomas de células humanas en cultivo. Desde el mismo lote de células, leen los códigos de barras en el ARN para medir la actividad reguladora, y usan ATAC-seq y CUT&Tag para medir la apertura de la cromatina y una marca clave de histona (H3K27ac) específicamente en las secuencias insertadas. Al normalizar estas señales según la frecuencia con la que cada secuencia se integra realmente, obtienen mediciones paralelas de la “fuerza de encendido/apagado” y del estado epigenético de miles de elementos en un solo experimento.
Descifrar cómo funcionan conjuntamente los motivos de factores de transcripción
Para ver qué puede revelar esta tecnología, el equipo construyó enhancers sintéticos a partir de motivos conocidos de factores de transcripción usados en células hepáticas. Arreglaron estos motivos en distintos números y órdenes sobre plantillas de ADN neutrales. Algunos factores, como HNF1A y XBP1, se comportaron como activadores clásicos: añadir más copias aumentó la producción del reportero. Otros, como HNF1A y ONECUT1, impulsaron principalmente la accesibilidad de la cromatina, acorde con su papel de factores “pioneros” que abren regiones cerradas del ADN. PPARA mostró un patrón distinto, alterando fuertemente la cromatina y las marcas de histonas pero no la transcripción por sí solo, aunque cooperaba con otros factores para elevar la actividad génica. REST, un represor conocido, atenuó la actividad cuando se colocó junto a activadores. De forma llamativa, simplemente reordenar cuatro motivos podía cambiar sustancialmente la fuerza del enhancer, y los activadores tendieron a funcionar mejor cuando estaban más cerca del promotor, revelando una especie de gramática en la disposición de estos motivos.
Localizar bases sensibles en enhancers de pluripotencia
Los investigadores se centraron luego en enhancers importantes para la identidad de las células madre, examinando regiones unidas por los factores de pluripotencia POU5F1 (también llamado OCT4) y SOX2. Crearon bibliotecas de mutaciones densas en las que cada base de enhancers de 100 pares de bases se alteró sistemáticamente, junto con pequeñas ventanas de seis bases que se mezclaron aleatoriamente. Usando e2MPRA en células madre pluripotentes inducidas, pudieron ver qué mutaciones debilitaban o fortalecían la actividad del reportero y cómo afectaban la apertura de la cromatina y la acetilación. La alteración del motivo de unión POU5F1::SOX2 a menudo redujo tanto la actividad génica como las marcas epigenéticas, confirmando su papel central. En un enhancer bien estudiado cerca del gen POU5F1, también encontraron que cambiar un motivo YY1 aumentaba la transcripción pero reducía la apertura de la cromatina, lo que sugiere que algunos factores pueden promover un estado abierto a la vez que restringen la expresión.
Qué significa esto para los genes y la enfermedad
e2MPRA no reproduce a la perfección todos los matices del entramado 3D natural del genoma, pero ofrece una forma práctica de comparar miles de secuencias regulatorias y variantes bajo las mismas condiciones. Al acoplar una lectura funcional (con qué fuerza un segmento de ADN impulsa un gen) con lecturas epigenéticas (cómo se empaqueta y marca ese ADN), este método ayuda a revelar por qué ciertos motivos de factores de transcripción, combinaciones y posiciones son tan cruciales. A largo plazo, herramientas como e2MPRA pueden facilitar la interpretación de variantes genéticas no codificantes vinculadas a enfermedades, el diseño de enhancers sintéticos para terapia génica y la construcción de un “código regulador” más completo que conecte la secuencia de ADN con el comportamiento celular.
Cita: Zhang, Z., Georgakopoulos-Soares, I., Bourque, G. et al. Simultaneous epigenomic profiling and regulatory activity measurement using e2MPRA. Nat Commun 17, 1724 (2026). https://doi.org/10.1038/s41467-026-68422-3
Palabras clave: regulación génica, enhancers, epigenética, factores de transcripción, genómica funcional