Clear Sky Science · es
Las ligasas E3 de ubiquitina guardianas dirigen las desaminasas APOBEC3 asociadas al cáncer hacia la degradación para promover la integridad del genoma humano
Protegiendo nuestro ADN del fuego amigo
Nuestras células emplean enzimas potentes para dañar el ADN viral, ayudándonos a defendernos frente a infecciones. Pero algunas de estas mismas enzimas, si no se controlan, pueden dejar cicatrices en nuestro propio genoma y contribuir al cáncer. Este estudio revela cómo las células humanas vigilan estas enzimas riesgosas, mostrando un sistema de “control de calidad” incorporado que etiqueta las versiones peligrosas para su destrucción antes de que puedan reescribir nuestro ADN.
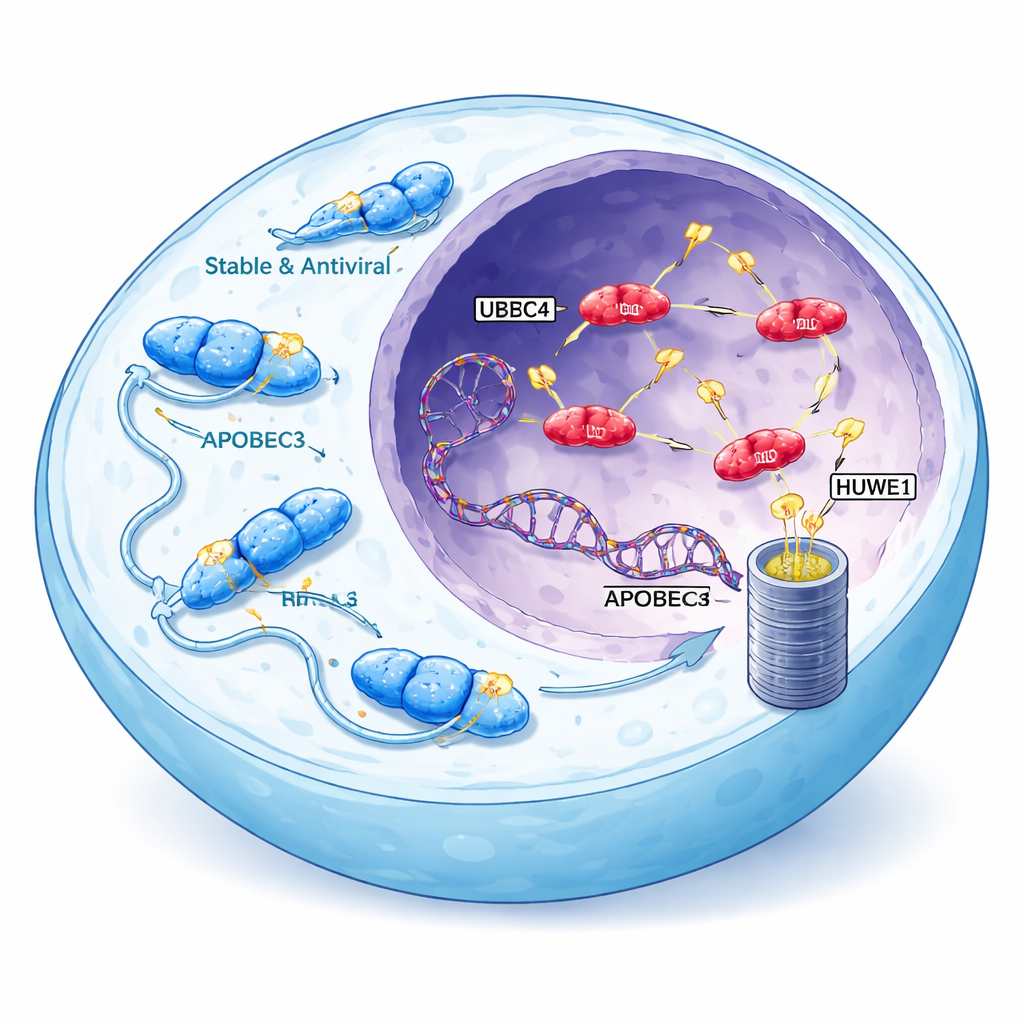
Combatientes contra virus que pueden volverse contra nosotros
La familia de enzimas APOBEC3 normalmente ayuda a defender contra virus como el VIH al alterar químicamente el ADN viral, provocando errores letales. Los humanos tienen siete variantes de APOBEC3, y tres de ellas —A3A, A3B y una forma de A3H llamada haplotipo I (A3H-I)— están fuertemente vinculadas a los patrones de mutación observados en muchos cánceres. Estas enzimas en particular pueden moverse al núcleo celular, donde residen nuestros cromosomas, e introducir racimos característicos de mutaciones en el genoma. Las firmas vinculadas a APOBEC aparecen en más de la mitad de todos los cánceres humanos, especialmente en tumores de mama, pulmón y vejiga, donde amplían el repertorio de cambios genéticos que los tumores pueden utilizar para adaptarse y resistir tratamientos.
Por qué las formas más peligrosas son curiosamente inestables
De forma curiosa, las enzimas APOBEC3 más asociadas al cáncer son también las menos estables. A diferencia de sus homólogas citoplasmáticas, que se acumulan a altos niveles y bloquean virus de manera eficiente, A3A, A3B y A3H-I se degradan rápidamente y suelen estar presentes en bajas concentraciones en el núcleo. Los investigadores razonaron que esta inestabilidad podría ser deliberada: si las células limitan activamente los niveles de proteínas APOBEC3 nucleares, cualquier fallo en ese control podría desatar ráfagas de mutagénesis. Usando A3H-I como modelo, mostraron que los APOBEC3 asociados al cáncer se destruyen principalmente por el proteasoma, la trituradora de proteínas de la célula, tras ser marcados con pequeñas “banderas” moleculares llamadas ubiquitina en múltiples sitios de aminoácidos.
Encontrando a los guardianes celulares
Para identificar la maquinaria responsable de etiquetar A3H-I y A3B, el equipo combinó cribado CRISPR con mapeo de proximidad proteica. Diseñaron células que brillan de manera diferente según la estabilidad de A3H-I y su variante inofensiva A3H-II, y luego alteraron sistemáticamente genes implicados en la degradación proteica. Tres ligasas de ubiquitina —UBR4, UBR5 y HUWE1— destacaron. Eliminar cualquiera de estas ligasas elevó selectivamente los niveles de la inestable A3H-I nuclear sin afectar a la estable A3H-II citoplasmática. Las mismas ligasas aumentaron de forma independiente los niveles de A3B endógena en líneas celulares de colon y del sistema inmune, y eliminar las tres a la vez produjo un incremento aditivo en la abundancia de A3B. Experimentos bioquímicos mostraron además que UBR5 y HUWE1 se unen físicamente a A3B y A3H-I y adhieren directamente cadenas de ubiquitina, mientras que UBR4 parece especializarse en alargar esas cadenas para hacer las proteínas más fácilmente desechables.
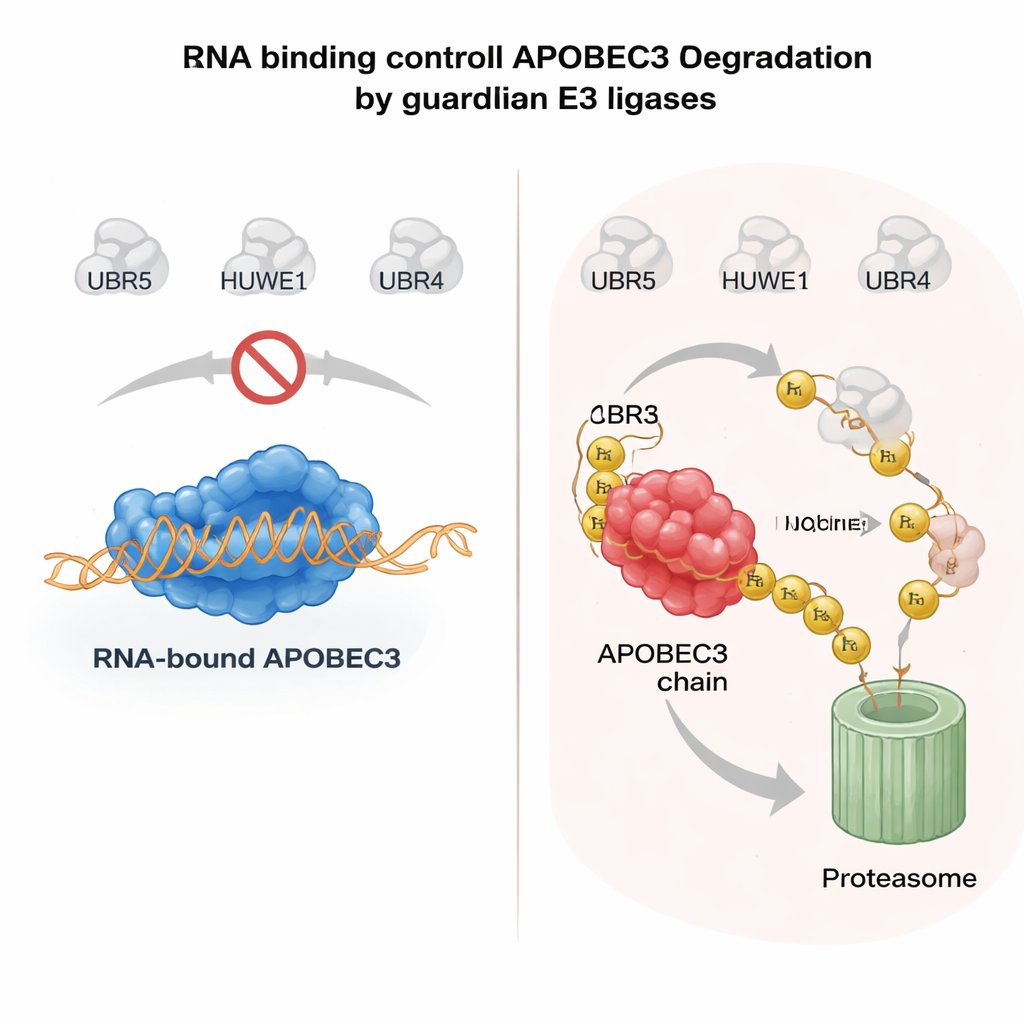
El ARN como cinturón de seguridad para enzimas riesgosas
¿Qué determina si una enzima APOBEC3 se salva o se destruye? Una pista clave provino de la forma en que las proteínas APOBEC3 se unen a moléculas de ARN en el citoplasma. Cuando A3H u otro miembro de la familia, A3G, se unen al ARN, tienden a permanecer en grandes complejos en el citosol y son relativamente estables. Mutaciones que debilitan la unión al ARN hacen que estas enzimas se desplacen al núcleo, pierdan a sus socios protectores y se vuelvan altamente inestables. Los autores mostraron que cuando las proteínas APOBEC3 no están unidas al ARN, UBR5 y HUWE1 reconocen superficies expuestas en la enzima, las marcan con ubiquitina y las dirigen a la degradación nuclear. En sistemas purificados, añadir RNasa para eliminar el ARN aumentó considerablemente la capacidad de estas ligasas para unirse y ubiquitinar a APOBEC3, confirmando que la unión al ARN actúa como un escudo molecular. Este mecanismo permite a las células mantener activas a las APOBEC3 antivirales en el citoplasma mientras eliminan con rapidez cualquier fracción no unida y peligrosa en el núcleo.
Cuando los guardianes fallan: vínculos con mutaciones cancerosas
Si UBR4, UBR5 y HUWE1 actúan como guardianes, su pérdida debería aumentar los niveles de mutación. Los investigadores probaron esto desactivando cada ligasa en células de cáncer de colon y siguiendo los cambios en el ADN a lo largo del tiempo mediante un método de secuenciación sensible que identifica “firmas” mutacionales. La eliminación de estas ligasas, particularmente en células que expresan A3H-I, amplificó los patrones de mutación específicos de APOBEC —precisamente el tipo encontrado en tumores humanos. Al extender el análisis a datos de pacientes, investigaron miles de genomas tumorales y hallaron que los tumores con mutaciones en UBR5 o HUWE1 presentaban una fracción significativamente mayor de firmas mutacionales vinculadas a APOBEC que los tumores con ligasas intactas, incluso tras ajustar por la carga mutacional global. Esto sugiere que ligasas guardianas defectuosas en pacientes pueden permitir que las APOBEC3 asociadas al cáncer actúen sin control y remodelen el genoma tumoral.
Qué significa esto para la atención del cáncer en el futuro
Para un público general, la conclusión es que nuestras células disponen de un sistema de vigilancia sofisticado para evitar que enzimas antivirales útiles saboteen accidentalmente nuestro propio ADN. UBR4, UBR5 y HUWE1 actúan como guardianes que detectan cuando las APOBEC3 ya no están unidas de manera segura al ARN y, sobre todo en el núcleo, las envían a la trituradora celular. Cuando este sistema de control se debilita —por mutaciones en las ligasas o por fármacos que bloquean la degradación proteica— la actividad de APOBEC3 puede alimentar el caos genético que impulsa la evolución tumoral y la resistencia al tratamiento. Comprender esta red de guardianes abre puertas a nuevos marcadores diagnósticos, como mutaciones en ligasas o niveles de proteínas APOBEC, y sugiere que ajustar con cuidado esta vía podría algún día ayudar a limitar las ráfagas de mutaciones nocivas en tumores sin comprometer nuestras defensas antivirales.
Cita: Schwartz, I., Budroni, V., Meyenberg, M. et al. Guardian ubiquitin E3 ligases target cancer-associated APOBEC3 deaminases for degradation to promote human genome integrity. Nat Commun 17, 1723 (2026). https://doi.org/10.1038/s41467-026-68420-5
Palabras clave: APOBEC3, estabilidad del genoma, ligasa de ubiquitina, mutagénesis en el cáncer, degradación de proteínas