Clear Sky Science · es
Patrón espacial de contractilidad por un gradiente de actividad mecanógeno autoorganizado subyace a la gastrulación de Drosophila
Cómo se esculpen los tejidos
Los embriones tempranos convierten de alguna manera hojas simples de células en formas tridimensionales complejas. Este estudio plantea una pregunta básica tras ese truco: ¿cómo coordinan las células dónde apretar y doblarse para que un tejido se pliegue en el lugar y dirección correctos? Al observar embriones de mosca con alta resolución, los autores descubren una señal química que se comporta como un “morfógeno mecánico”, que patrea directamente dónde las células se contraen para impulsar un evento de plegamiento crucial en el desarrollo.
Una onda que pliega el embrión
En la mosca de la fruta Drosophila, un paso clave en el desarrollo temprano es la gastrulación, cuando una capa plana de células se pliega hacia dentro para comenzar a formar el intestino. En la parte posterior del embrión, un parche de células llamado primordio del endodermo posterior inicia este proceso contrayéndose en sus caras superiores (apicales). Este pliegue inicial lanza una onda viajera de invaginación del tejido que barre hacia adelante a través de las células vecinas. Los autores muestran que esta onda depende de una señal llamada Fog, una molécula secretada que activa una familia de receptores conocida como GPCR, que a su vez enciende la maquinaria contractil de la célula formada por la proteína motora Miosina-II.
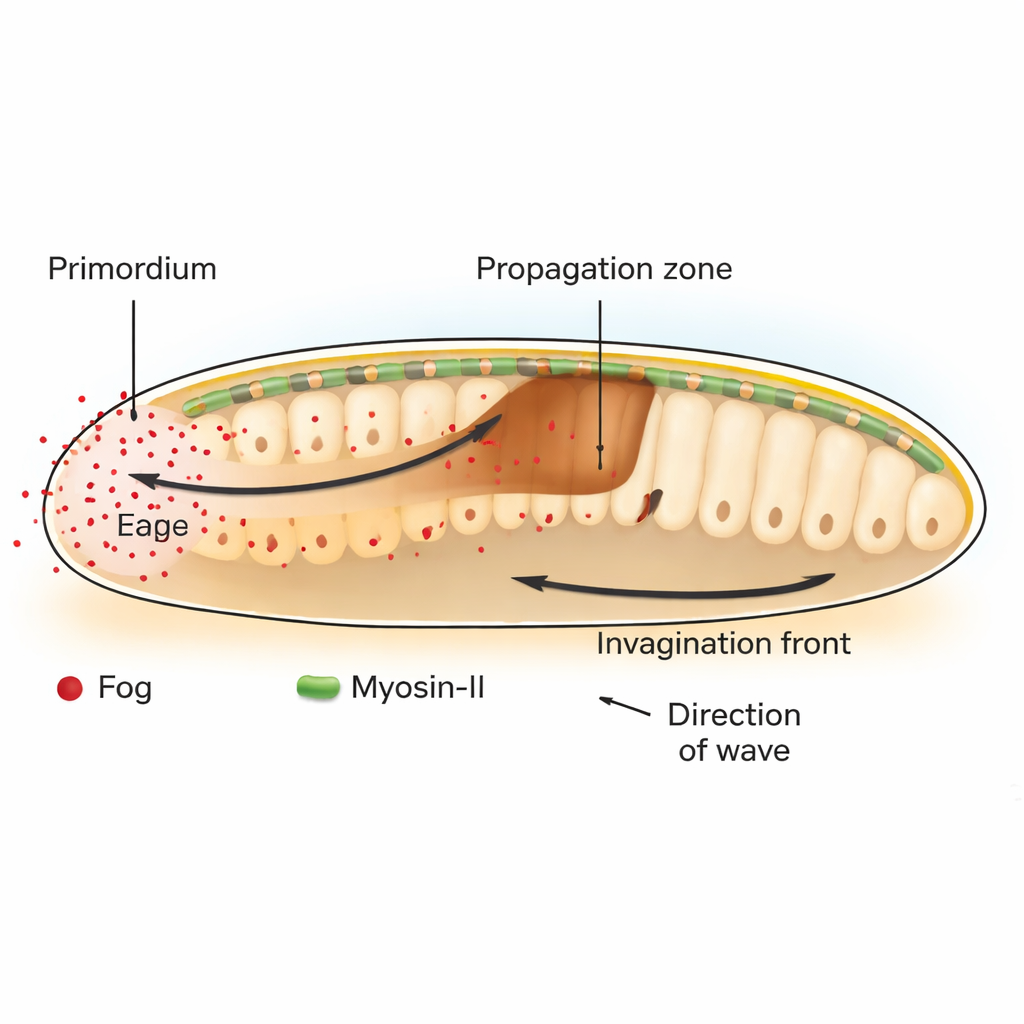
Un químico que patrea la fuerza, no el destino
Clásicamente, los biólogos del desarrollo se han centrado en los “morfógenos”, moléculas difusibles cuyos gradientes de concentración indican a las células qué identidad adoptar. Aquí, Fog se comporta de manera distinta. En lugar de cambiar qué tipo de célula se convertirá una región, Fog ajusta directamente cuán intensamente se contraen las células. Restaurando o bloqueando selectivamente Fog y su mensajero aguas abajo Gα solo en ciertas regiones, los investigadores demuestran que Fog producido en el primordio es tanto necesario como suficiente para desencadenar la activación de Miosina-II y el plegamiento del tejido a distancia en la zona de propagación adyacente. Cuando Fog está anclado de modo que no puede difundirse, solo las células productoras se contraen y la onda de invaginación se detiene tras una o dos filas celulares.
Un gradiente oculto en la superficie celular
Una idea natural es que Fog podría formar un gradiente clásico de concentración fuera de las células. Usando una versión de Fog marcada con fluorescencia y mediciones de fluorescencia sensibles, el equipo encuentra lo contrario: en la delgada capa de fluido entre el tejido y su cubierta (la membrana vitelina), Fog es notablemente uniforme. Sin embargo, la actividad de Miosina-II forma claramente un gradiente viajero pronunciado, más fuerte justo delante del pliegue avanzado y atenuándose a unas pocas diámetros celulares de distancia. La pieza que faltaba es que Fog no actúa como una señal de concentración en masa; en cambio, una pequeña fracción de Fog queda brevemente atrapada en la superficie celular, uniéndose a sus receptores GPCR y formando un gradiente de actividad ligado a la superficie aun cuando las moléculas libres de Fog permanecen uniformemente mezcladas en el fluido.
Receptores, endocitosis y adhesión moldean la onda
Los autores muestran que este Fog ligado a la superficie, junto con sus receptores, se autoorganiza en un patrón. Donde Fog encuentra repetidamente receptores, promueve el agrupamiento y la activación de receptores, lo que recluta más Miosina-II. Un proceso celular de “limpieza”—la endocitosis de GPCR—elimina entonces los complejos activos, evitando una activación descontrolada y ayudando a ajustar hasta dónde se propaga la señal. Cuando esta endocitosis se ralentiza genéticamente, el gradiente de Miosina-II se vuelve más alto y más ancho. Un segundo actor clave es un conjunto de moléculas de adhesión llamadas integrinas. A medida que el tejido se pliega, las células delante del pliegue presionan contra la membrana vitelina; este contacto activa localmente las integrinas, que a su vez aumentan la eficacia de la señalización Fog–GPCR. La región de fuerte implicación de integrinas coincide con la extensión del gradiente de Miosina-II, y sin integrinas la onda se vuelve débil y de corto alcance incluso si la señalización Fog está potenciada por otros medios.
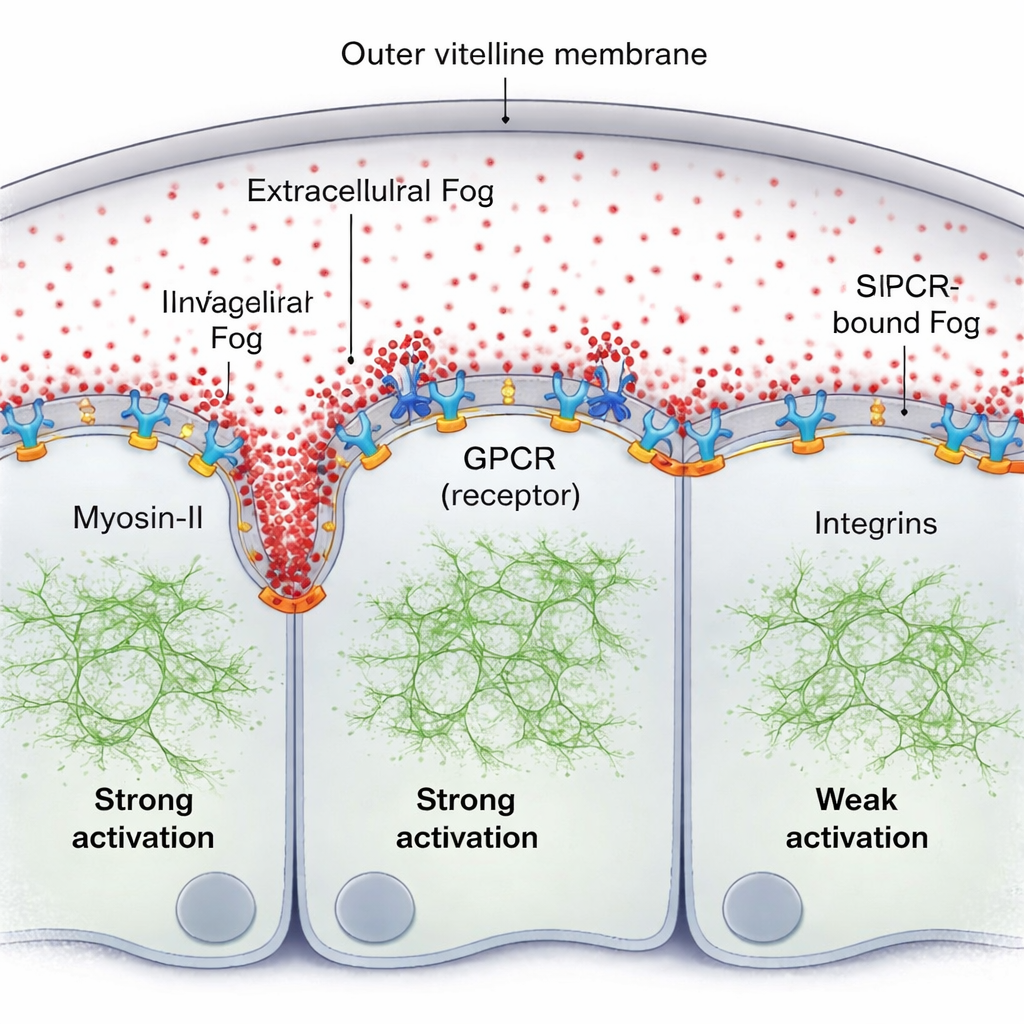
Un patrón mecánico auto-renovable
Para un no especialista, el mensaje principal es que el embrión no depende únicamente de mapas químicos preestablecidos para decidir dónde plegarse. En su lugar, construye un patrón móvil de actividad mecánica en tiempo real. Fog se difunde de manera uniforme, pero su acción efectiva queda esculpida en la superficie celular por el agrupamiento de receptores, la eliminación de receptores y la geometría cambiante del tejido conforme las células presionan contra su entorno. Esto crea un gradiente viajero autoorganizado de fuerza contractil que tira del tejido hacia dentro en una onda coordinada. El trabajo ofrece un ejemplo concreto de un largamente teorizado “mecanógeno”: una molécula difusible que patrea directamente las fuerzas físicas en un tejido, ayudando a explicar cómo los organismos vivos esculpen con tanta fiabilidad sus formas durante el desarrollo.
Cita: Mundhe, G., Dunsing-Eichenauer, V., Philippe, JM. et al. Spatial patterning of contractility by a self-organized mechanogen activity gradient underlies Drosophila gastrulation. Nat Commun 17, 1721 (2026). https://doi.org/10.1038/s41467-026-68418-z
Palabras clave: gastrulación, mecanógeno, embrión de Drosophila, mecánica de tejidos, señalización Fog