Clear Sky Science · es
Las configuraciones de los extremos de ADN dictan la formación del complejo sináptico durante el puenteo mediado por NHEJ
Cuando el ADN se rompe, las células deben reaccionar rápido
Cada día, el ADN de nuestras células sufre muescas, cortes y desgaste por el metabolismo normal y por factores ambientales. Entre las lesiones más peligrosas están las roturas de doble cadena, en las que ambas hebras de la hélice de ADN se rompen. Si estas roturas no se reparan con rapidez y precisión, las células pueden morir o, peor aún, evolucionar hacia el cáncer. Este estudio explora cómo la forma y la química exactas de los extremos rotos del ADN ayudan a determinar si una vía clave de reparación, denominada unión de extremos no homóloga (NHEJ), aproxima esos extremos de forma eficiente y con el menor número posible de errores.
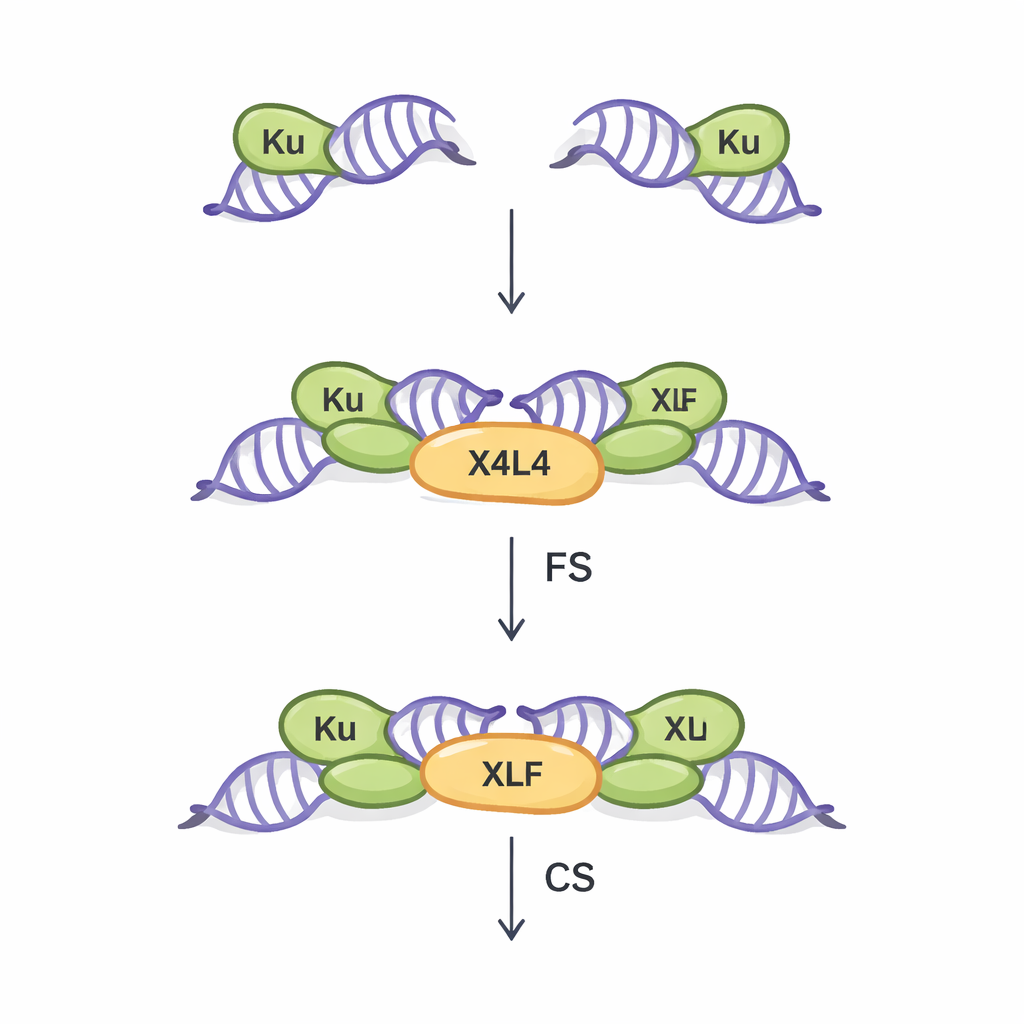
Dos maneras de reunir el ADN roto
La NHEJ es la ruta principal de reparación de las roturas de doble cadena en la mayoría de las células de nuestro organismo. Funciona sin necesitar una plantilla de ADN coincidente, lo que la hace rápida pero algo proclive a errores. El primer paso crucial en esta vía se llama sinapsis: el puente físico entre los dos extremos rotos del ADN para que luego puedan ser unidos. Trabajos anteriores, principalmente con extremos de ADN idealizados y planos, revelaron dos tipos de ensamblajes sinápticos. En el estado de “sinapsis flexible” (FS), los extremos se mantienen próximos y pueden moverse, buscando formas de parearse. En el estado de “sinapsis cerrada” (CS), los extremos se alinean extremo con extremo y están listos para ser sellados por una ligasa. Se sabe que tres proteínas nucleares —Ku, XRCC4–Ligasa IV (conjuntamente X4L4) y XLF— coordinan este proceso, pero no se comprendía bien cómo los extremos de ADN irregulares del mundo real influyen en qué estado sináptico se forma.
La forma del extremo y las coincidencias cortas dirigen la vía de reparación
Los investigadores usaron FRET de molécula única, una técnica basada en fluorescencia que rastrea distancias a escala nanométrica, para observar moléculas individuales de ADN mientras las proteínas de NHEJ las acercaban. Compararon extremos planos simples con extremos más realistas que portaban salientes cortas —pequeñas colas monocatenarias que potencialmente pueden emparejarse entre sí. Encontraron que cuando las salientes son complementarias, incluso por solo unas pocas bases, aumentan drásticamente la probabilidad de formar un complejo sináptico cerrado. De hecho, tres bases coincidentes de “microhomología” en la rotura fueron suficientes para que Ku y X4L4 por sí solos crearan un complejo CS estable, sin necesitar a XLF. Esto muestra que el propio ADN puede aportar parte de la energía y la guía que normalmente proporcionan las proteínas auxiliares.
Cómo pequeñas solapas del ADN ayudan a estabilizar el puente
Al analizar firmas FRET distintas, el equipo descubrió al menos dos variantes estructurales del estado sináptico cerrado para extremos con salientes. En una, las puntas mismas de las salientes se emparejan entre sí, formando una unión con muesca o con hueco. En la otra, las uniones donde el ADN bicatenario encuentra las salientes monocatenarias se alinean en línea, mientras que las salientes se pliegan hacia fuera como pequeñas solapas. Estas solapas siguen permitiendo el apareamiento de bases y mantienen los extremos en muy estrecha proximidad, lo que probablemente estabiliza el complejo y deja espacio para que las enzimas recorten o alarguen el ADN según sea necesario antes del sellado final. De forma llamativa, daños oxidativos comunes en las salientes, como la 8-oxoguanina, solo afectaron modestamente este proceso, lo que subraya la robustez de la NHEJ frente a ciertas formas de daño.
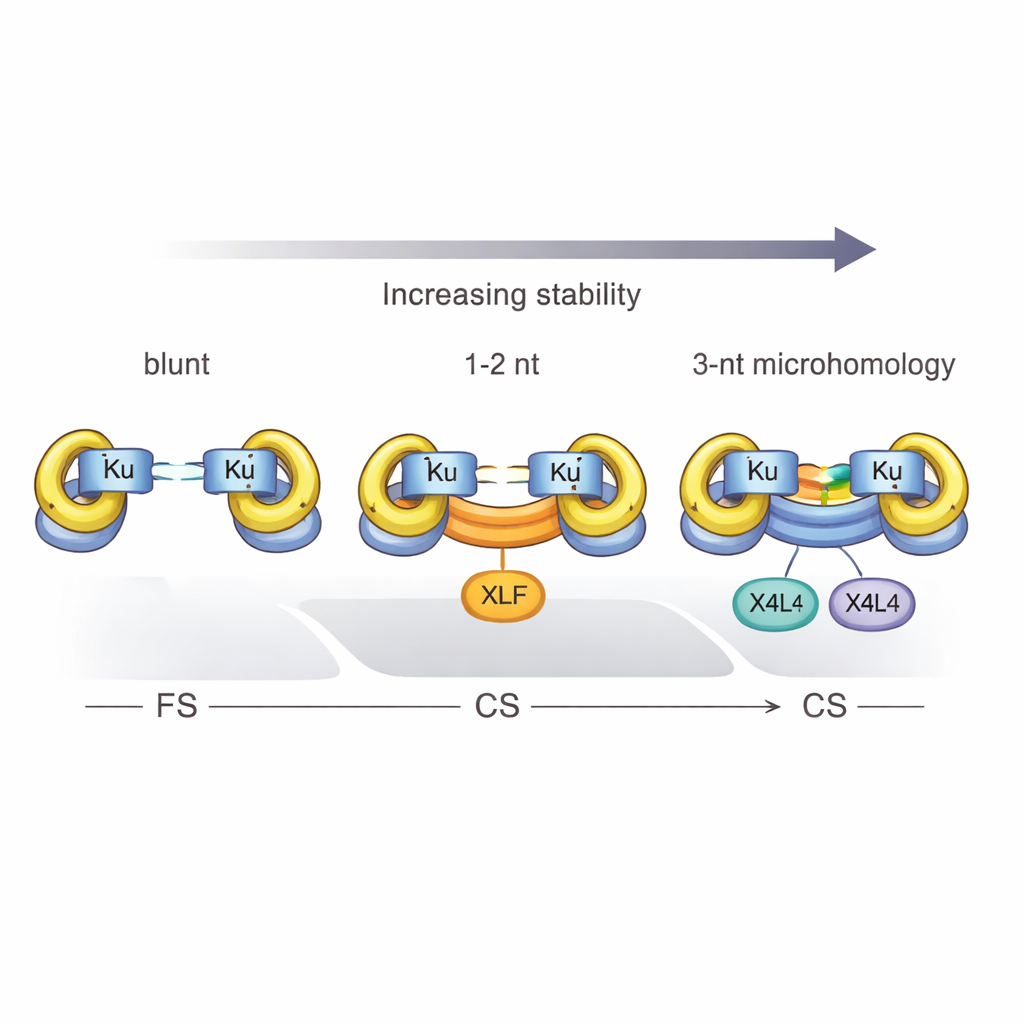
Proteínas, fosfatos y el poder del tres
El estudio también definió un umbral claro: se requieren al menos tres pares de bases complementarias para que Ku y X4L4 conviertan de forma fiable un complejo flexible en uno cerrado. Con solo una o dos coincidencias, el sistema suele estancarse en el estado flexible a menos que XLF se una para ayudar a abrazar los extremos. Los detalles químicos también importan. Cuando el ADN roto porta un grupo fosfato 5′ —una característica normal de muchas roturas fisiológicas—, la sinapsis se vuelve más eficiente y los complejos cerrados tienen más probabilidades de ser realmente ligados, convirtiendo un puente temporal en una reparación permanente. Sin embargo, este refuerzo por fosfato no puede reemplazar por completo el efecto estabilizador del apareamiento de bases en la rotura.
Por qué esto importa para la salud y la edición del genoma
En lenguaje cotidiano, este trabajo muestra que los extremos rotos del ADN no son víctimas pasivas esperando ser reparadas. Sus formas exactas, pequeños parches de secuencia coincidente y etiquetas químicas guían activamente cómo las proteínas de reparación agarran, alinean y reconectan esos extremos. Cuando hay tres o más bases coincidentes, los propios extremos de ADN ayudan a bloquear la rotura en una configuración lista para reparar, a veces haciendo opcionales ciertas proteínas auxiliares. Cuando tales coincidencias escasean, los factores proteicos adicionales se vuelven esenciales. Estos conocimientos ayudan a explicar por qué algunas roturas se remiendan limpiamente mientras que otras conducen a pequeñas mutaciones o reordenamientos. También ofrecen pistas para mejorar herramientas de edición del genoma como CRISPR, donde las roturas deliberadamente creadas son reparadas por la misma maquinaria de NHEJ. Al ajustar los extremos de esas roturas, los científicos podrían controlar mejor cómo se remodela el genoma.
Cita: Zhang, C., Jin, W., Jiang, Y. et al. DNA end configurations dictate synaptic complex formation during NHEJ-mediated end bridging. Nat Commun 17, 1720 (2026). https://doi.org/10.1038/s41467-026-68417-0
Palabras clave: reparación de roturas de doble cadena de ADN, unión de extremos no homóloga, sinapsis de ADN, microhomología, estabilidad genómica