Clear Sky Science · es
Un único cambio de valina a leucina interrumpe la unión al ADN de AP2-G de Plasmodium falciparum y revela el papel de GDV1 en la activación de ap2-g
Cómo los parásitos de la malaria toman una decisión crítica de vida o muerte
Los parásitos de la malaria que viven en nuestra sangre afrontan constantemente una decisión que cambia su vida: seguir multiplicándose dentro de un único huésped, o convertirse en una forma que pueda saltar al siguiente huésped a través de la picadura de un mosquito. Este estudio revela cómo un pequeño cambio en una proteína del parásito puede cerrar por completo esa fase infecciosa, lista para el mosquito, ofreciendo nuevos enfoques para bloquear la transmisión de la malaria.
La encrucijada del parásito
En el torrente sanguíneo, los parásitos Plasmodium falciparum se centran mayoritariamente en el crecimiento rápido, que provoca la enfermedad. Pero una pequeña minoría se transforma en formas sexuales llamadas gametocitos, las únicas etapas que los mosquitos pueden ingerir y transmitir. Durante mucho tiempo ha sido un misterio cómo solo algunos parásitos en una población hacen este cambio. Trabajos previos mostraron que dos proteínas del parásito, GDV1 y una proteína que se une al ADN llamada AP2-G, están en el centro de esta decisión. GDV1 ayuda a despertar el gen ap2-g, que normalmente está silenciado, y AP2-G a su vez activa un conjunto de genes que impulsan el desarrollo sexual. El estudio actual partió de explorar otra proteína, una quinasa denominada STK2, pero en su lugar tropezó con un hallazgo mucho más dramático en el propio AP2-G.
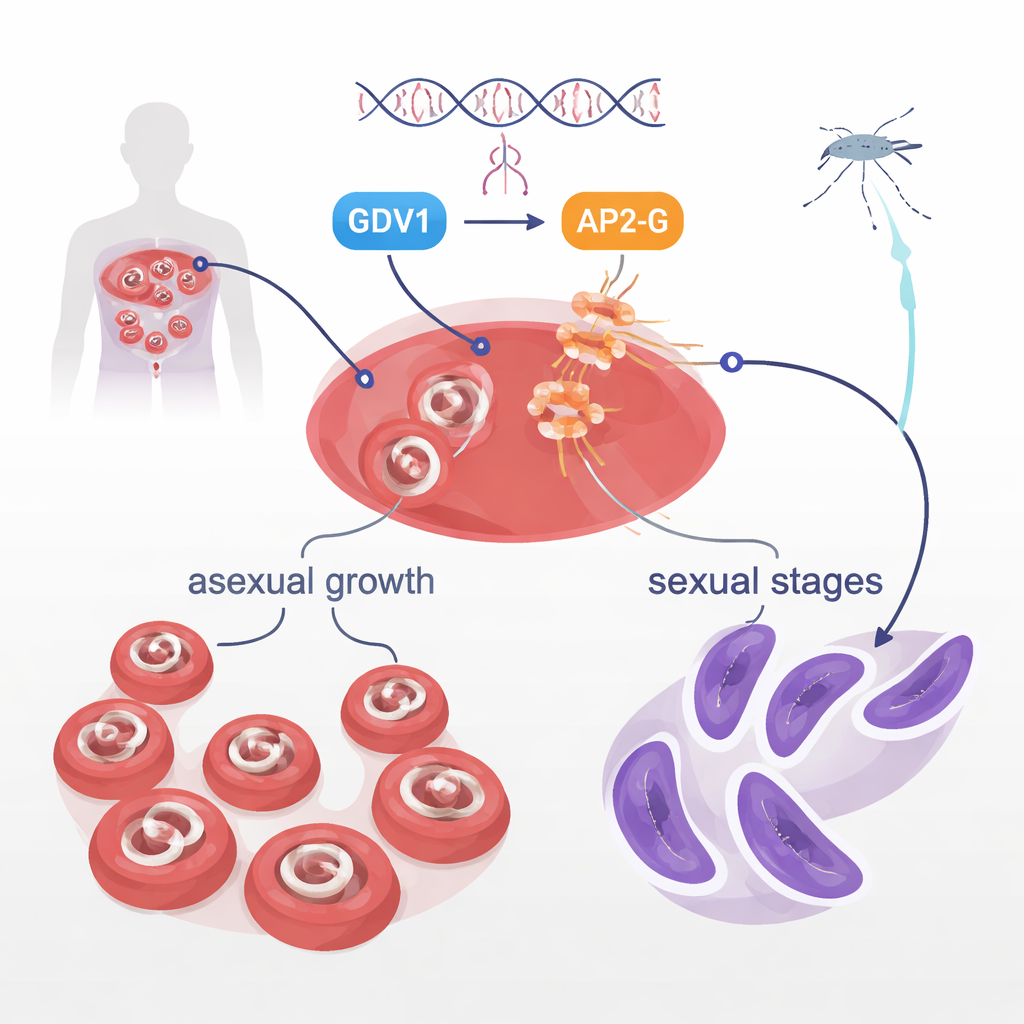
Un solo aminoácido que impide la transmisión
Al eliminar el gen stk2 en una cepa de laboratorio del parásito, los investigadores observaron que esos parásitos perdieron por completo su capacidad de producir gametocitos, aunque seguían creciendo asexualmente sin problema. Sorprendentemente, al repetir manipulaciones similares en otra cepa, los gametocitos se formaron con normalidad. La secuenciación del genoma completo reveló al culpable oculto: un único cambio de “letra” en el gen ap2-g, que intercambia un aminoácido, valina, por otro muy similar, leucina, en la posición 2163. Esta posición se sitúa al comienzo de la región que se une al ADN de AP2-G, la parte que físicamente agarra motivos específicos del ADN para activar genes. Ese diminuto cambio de valina a leucina fue suficiente para abolir la formación de gametocitos. Cuando los científicos introdujeron esta mutación en parásitos normales, los gametocitos desaparecieron; al revertirla de nuevo a valina, el desarrollo sexual se restauró por completo.
Cómo el cambio rompe la cerradura molecular
Para entender por qué este cambio sutil es tan devastador, el equipo combinó modelado por ordenador con experimentos de laboratorio. Las predicciones estructurales sugerían que reemplazar la valina por leucina desplaza y desestabiliza la forma precisa del dominio de unión al ADN de AP2. En ensayos in vitro con proteínas purificadas, el AP2-G normal se unía con fuerza a su secuencia de ADN preferida, un código corto que contiene el motivo “GnGTAC”. En cambio, la AP2-G mutante con leucina en la posición 2163 no pudo unirse a esa secuencia en absoluto. Sin una unión estable al ADN, AP2-G ya no podía activar su propio gen (un bucle de retroalimentación positiva conocido como autorregulación) ni activar docenas de genes aguas abajo necesarios para impulsar a los parásitos hacia la vía sexual. Funcionalmente, los parásitos mutantes se volvieron “estériles”: no podían formar las formas que infectan a los mosquitos, aunque seguían prosperando en los glóbulos rojos.
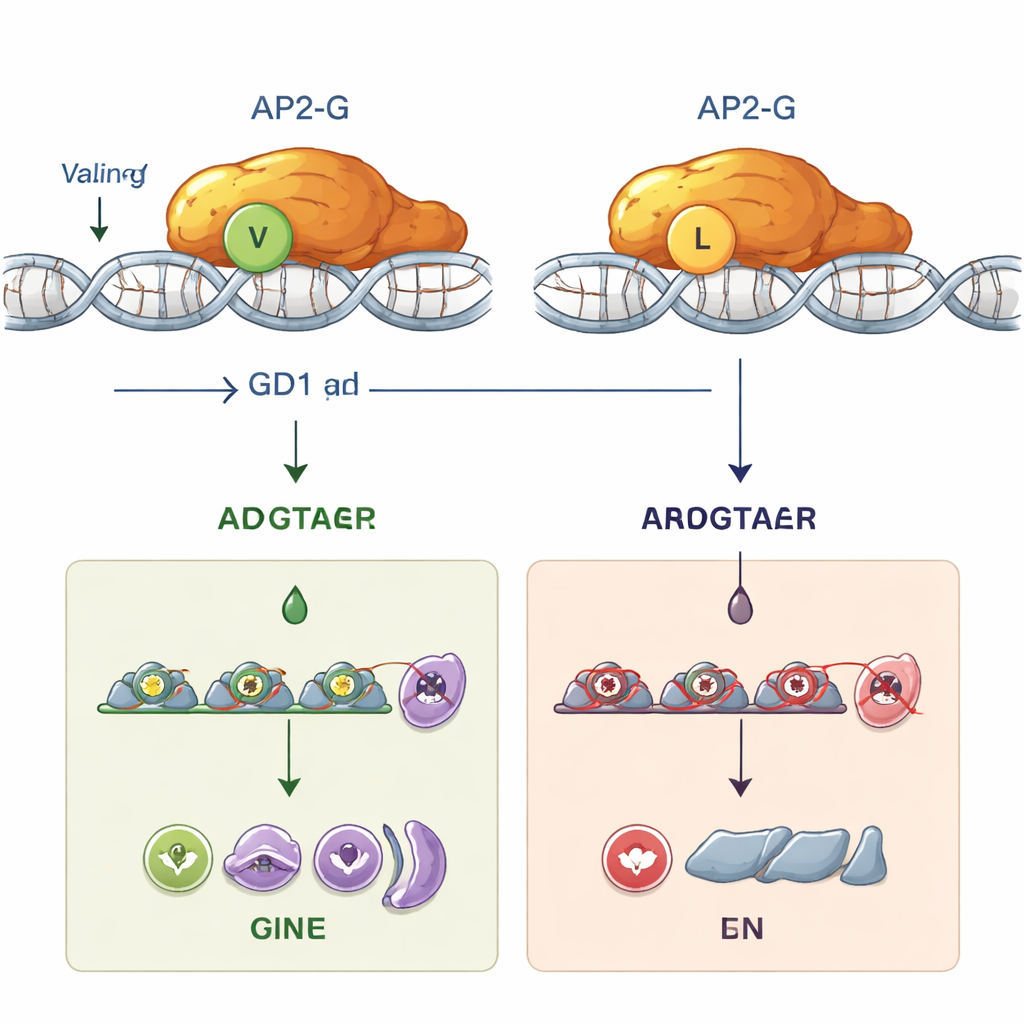
El papel oculto de GDV1 antes de que AP2-G asuma el control
La mutación también proporcionó a los investigadores una herramienta única: parásitos en los que el gen ap2-g puede activarse, pero AP2-G no puede unirse al ADN. Utilizando reporteros fluorescentes y luminiscentes, siguieron cuándo actúan los distintos actores durante el ciclo de 48 horas del parásito en los glóbulos rojos. Descubrieron que la proteína GDV1 aparece primero, temprano en una fase llamada esquizogonía, y es esencial para arrancar la expresión de ap2-g desde su estado silenciado. Esta activación temprana se produjo tanto si ap2-g codificaba AP2-G normal como la versión mutante. Solo más tarde, cuando se acumulaba suficiente AP2-G funcional, se desencadenaba el fuerte bucle de autoestimulación y la activación de otros genes “sexuales”. Un marcador clave, una proteína llamada MSRP1, se iluminó solo en parásitos con AP2-G funcional, proporcionando una forma práctica de distinguir parásitos comprometidos sexualmente en etapas tempranas y tardías. En las líneas mutantes con el cambio a leucina, GDV1 aún podía despertar ap2-g, pero la AP2-G defectuosa no pudo llevar el proceso adelante, por lo que el desarrollo sexual se estancó.
Implicaciones para detener la propagación de la malaria
Para un lector general, la conclusión es sencilla: los parásitos de la malaria dependen de una cerradura molecular extremadamente sensible para decidir si serán transmisibles. Este estudio muestra que cambiar solo un “diente” de esa cerradura—una única valina en la región que agarra el ADN de AP2-G—impide al parásito producir etapas infecciosas para mosquitos. Al mismo tiempo, aclara que otra proteína, GDV1, actúa antes como la llave que primero desbloquea el gen ap2-g silenciado, antes de que AP2-G potencie su propia producción y active un programa sexual más amplio. Al mapear esta secuencia de eventos y crear líneas de parásitos reporteras que se iluminan cuando ocurre cada paso, el trabajo proporciona herramientas potentes para cribar fármacos o factores humanos que interfieran con el compromiso sexual. A largo plazo, dirigir la región de unión al ADN de AP2-G o el paso de activación impulsado por GDV1 podría ser la base de nuevas estrategias que no solo curen la malaria en un paciente, sino que corten la cadena de transmisión por completo.
Cita: Prajapati, S.K., Dong, J.X., Morahan, B.J. et al. A single valine to leucine switch disrupts Plasmodium falciparum AP2-G DNA binding and reveals GDV1’s role in ap2-g activation. Nat Commun 17, 1719 (2026). https://doi.org/10.1038/s41467-026-68416-1
Palabras clave: transmisión de la malaria, Plasmodium falciparum, desarrollo de gametocitos, AP2-G, GDV1