Clear Sky Science · es
Mecanismos jerárquicos controlan la eliminación de la ARN polimerasa II atrancada por lesiones en el ADN
Cuando las máquinas que copian genes se topan con un obstáculo
Cada segundo, millones de diminutas máquinas moleculares llamadas ARN polimerasa II recorren nuestro ADN copiando genes a ARN. Pero cuando el ADN está dañado —por ejemplo por la luz ultravioleta (UV) del sol— estas máquinas pueden detenerse en seco. Si se acumulan copias atascadas, las células dejan de leer correctamente sus genes, algo especialmente peligroso para las neuronas y que puede conducir a enfermedades raras como el síndrome de Cockayne. Este estudio desvela, con detalle, cómo nuestras células detectan estas máquinas bloqueadas y las reinician o eliminan antes de que provoquen daño duradero.
Una nueva forma de observar los atascos celulares
Para entender cómo las células despejan las polimerasas bloqueadas, los investigadores construyeron una "cámara de tráfico" temporal para la transcripción. Usaron un fármaco que permite que las moléculas de ARN polimerasa II ya presentes sigan avanzando pero evita que se inicien nuevas, y luego generaron un pequeño parche de daño por UV dentro de cada núcleo celular. Siguiendo una etiqueta química específica en la forma activa de la polimerasa, pudieron observar qué tan rápido desaparecía de la zona dañada en comparación con el resto del genoma. Paralelamente, desarrollaron una prueba complementaria que analizaba la cantidad total de polimerasa activa en extractos celulares, revelando no solo cuándo la polimerasa abandonaba el ADN, sino cuándo la degradaba el sistema de eliminación de la célula.
Etiquetar las máquinas atrancadas para su eliminación
El equipo se centró en la reparación acoplada a la transcripción, un sistema especializado que repara las lesiones en genes que se están leyendo activamente. Emplearon una serie de líneas celulares humanas emparejadas, cada una carente de un factor de reparación distinto. Dos proteínas, CSB y CSA, surgieron como guardianes decisivos. Cuando falta cualquiera de ellas, la ARN polimerasa II se acumula y permanece obstinadamente en los sitios de daño, y la célula no logra degradarla. Bioquímicamente, estas células también fallaban en añadir pequeñas etiquetas de ubiquitina en un punto clave de la polimerasa. En contraste, las células que carecían de proteínas de reparación posteriores —las que recortan y reemplazan el ADN dañado— todavía despejaban la polimerasa con normalidad. Esto mostró que el marcado inicial con ubiquitina de la polimerasa atrancada es el desencadenante crítico para decidir su destino.
Dos equipos de limpieza: uno rápido y otro de respaldo
Una vez etiquetada la polimerasa, la célula puede escoger entre dos vías para eliminarla. La vía primaria y rápida depende de un gran complejo de reparación llamado TFIIH, y en particular de su subunidad helicasa XPD, que usa energía para desenrollar el ADN. Proteínas auxiliares, incluyendo ELOF1, UVSSA y STK19, llevan a TFIIH hasta la polimerasa atrancada y posicionan a XPD en el ADN justo por delante de ella. Usando nuevas pruebas en células de pacientes que portan una mutación que deja a XPD sin actividad helicasa, los autores mostraron que cuando XPD no puede abrir el ADN, la limpieza de la polimerasa se ralentiza de forma drástica, aunque el resto de la maquinaria de reparación esté presente. Esto indica que la acción mecánica de tracción de XPD es lo que normalmente "despega" la polimerasa de la lesión para que las enzimas reparadoras puedan alcanzar el sitio dañado.
Un plan B lento pero esencial
El estudio también reveló una vía de emergencia más lenta para despejar la polimerasa atrancada. Esta ruta depende de VCP (también conocido como p97), una proteína que reconoce las etiquetas de ubiquitina y puede extraer por la fuerza proteínas de la cromatina. En células sanas con TFIIH totalmente funcional, bloquear VCP solo tenía un efecto menor. Pero en células donde TFIIH faltaba, estaba mal posicionado o tenía XPD sin actividad, la eliminación de la polimerasa pasó a depender casi por completo de VCP. En estas situaciones, VCP aún podía extraer la polimerasa etiquetada del ADN, incluso cuando la reparación normal no podía continuar. De forma crucial, esta vía de respaldo seguía requiriendo cierto etiquetado con ubiquitina, lo que explica por qué las células que carecen de CSB o CSA —y por tanto de las marcas de ubiquitina— fracasaban en ambas rutas, la principal y la de apoyo.
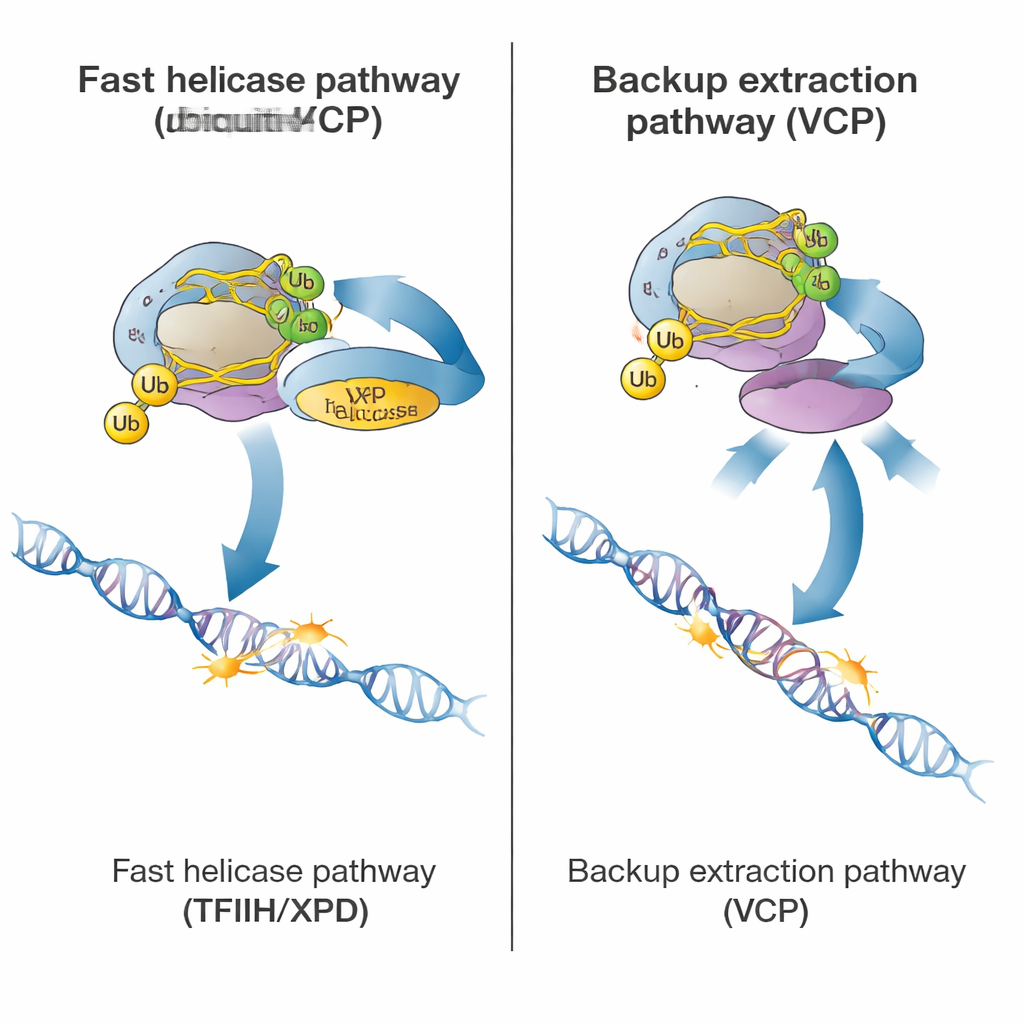
Por qué esto importa para la salud y la enfermedad
En conjunto, el trabajo describe un programa de seguridad jerárquico que las células emplean siempre que la ARN polimerasa II se topa con daño en el ADN. Primero, CSB y CSA marcan la máquina atrancada con ubiquitina. Si todo funciona correctamente, TFIIH y su helicasa XPD desalojan rápidamente la polimerasa para que la lesión pueda ser recortada y reparada. Si TFIIH no puede hacer su trabajo, VCP interviene para extraer la polimerasa y enviarla a degradación, evitando que obstruya la expresión génica aun cuando el daño en el ADN permanezca. Este marco ayuda a explicar por qué los defectos hereditarios en CSB o CSA causan problemas neurológicos particularmente graves: sin el marcado con ubiquitina, las células pierden tanto la ruta principal impulsada por la reparación como la ruta de extracción de respaldo, dejando polimerasas atrancadas en genes dañados y la transcripción bloqueada de forma crónica.
Cita: van der Meer, P.J., Yakoub, G., Tsukada, K. et al. Hierarchical mechanisms control the clearance of DNA lesion–stalled RNA polymerase II. Nat Commun 17, 1647 (2026). https://doi.org/10.1038/s41467-026-68413-4
Palabras clave: reparación del ADN acoplada a la transcripción, ARN polimerasa II, daño por UV, ubiquitilación de proteínas, síndrome de Cockayne