Clear Sky Science · es
Modificación de ADN por fosforotioato mediante sistemas BREX tipo 4 en el microbioma humano intestinal
Ajustes químicos ocultos en nuestras bacterias intestinales
En lo profundo del intestino humano, trillones de bacterias intercambian genes, combaten virus y reaccionan a la química de lo que comemos. Este estudio revela que muchas de esas microbios reescriben silenciosamente la columna vertebral de su propio ADN al sustituir átomos de oxígeno por azufre, creando una marca especial llamada fosforotioato. El trabajo descubre una versión nueva de este sistema, vinculada a un conjunto defensivo bacteriano denominado BREX tipo 4, y explora cuán extendidas están estas marcas de azufre en bacterias intestinales que pueden influir en la salud y la enfermedad.
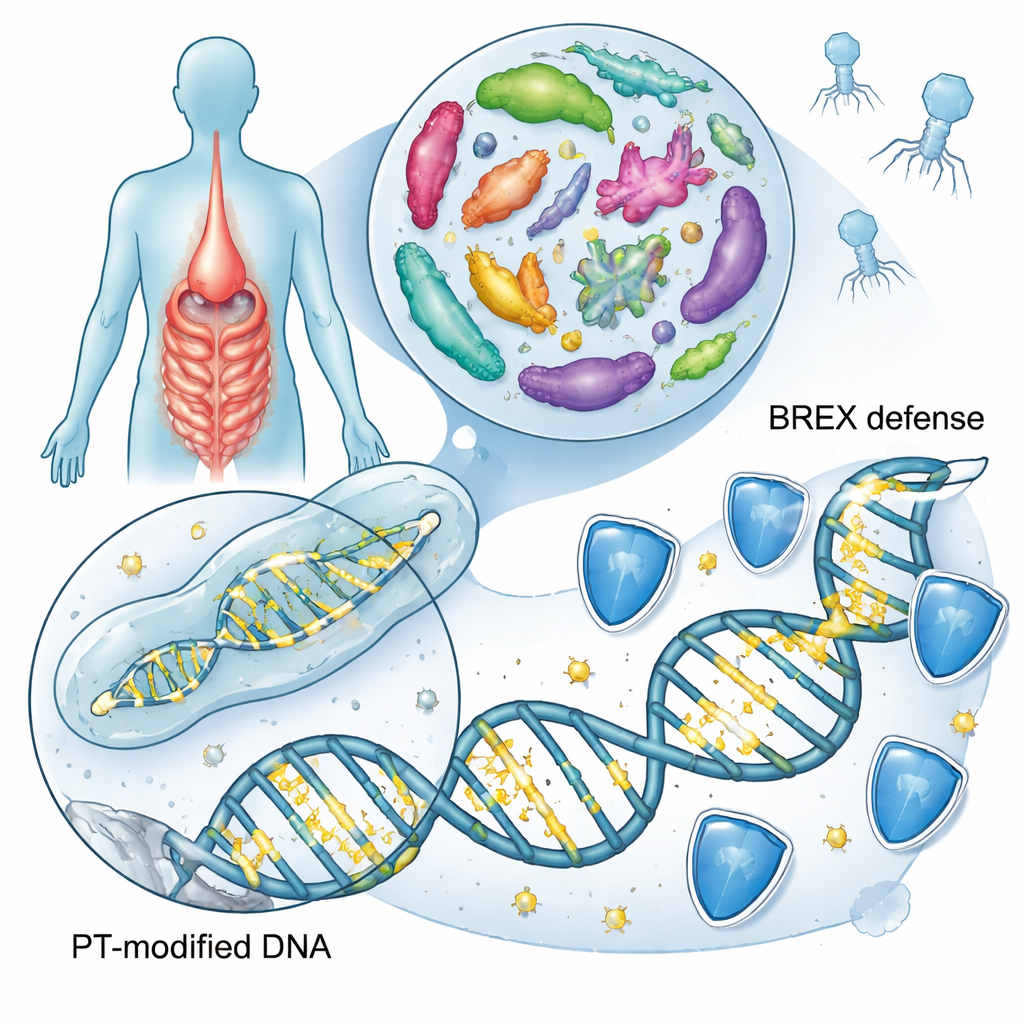
Un tipo distinto de marca en el ADN
La mayoría conoce las letras del ADN—A, T, C y G—modificadas por pequeñas etiquetas químicas como los grupos metilo, una pieza clave de la epigenética. Aquí el foco está en algo mucho más radical: algunas bacterias reemplazan uno de los átomos de oxígeno de la columna vertebral del ADN por azufre. Esta edición del esqueleto, conocida como fosforotioación, altera el comportamiento del ADN sin modificar el código genético. Estudios anteriores habían identificado dos familias principales de genes, llamadas dnd y ssp, que instalan estas marcas de azufre en aproximadamente una de cada diez especies bacterianas y arqueas. Estas marcas ayudan a las bacterias a reconocer su propio ADN, defenderse de virus invasores llamados fagos y, potencialmente, responder al estrés oxidativo y a la inflamación.
Buscando en miles de genomas intestinales
Para determinar cuán común es el ADN marcado con azufre en nuestros intestinos, los investigadores analizaron 13.663 genomas bacterianos procedentes de tres grandes colecciones de microbios humanos intestinales. Buscaron firmas genéticas clave suficientes para construir marcas de azufre: conjuntos de genes dnd, ssp o un conjunto candidato más reciente llamado brx, que forma parte de BREX, un sistema anti-fago conocido. Alrededor del 6,3% de los genomas intestinales portaba al menos uno de estos sistemas, principalmente en los grupos comunes del intestino Bacteroidota, Bacillota y Pseudomonadota. En comparación con un catálogo más amplio de bacterias de muchos ambientes, el intestino mostró un claro enriquecimiento de la versión BREX tipo 4, lo que sugiere que esta defensa basada en azufre está especialmente favorecida en el ecosistema intestinal.
Un nuevo sistema defensivo basado en azufre
Al examinar cómo se disponen los genes en los cromosomas bacterianos, el equipo observó genes similares a dnd anidados entre genes de defensa BREX, lo que apunta a que algunos sistemas BREX podrían instalar directamente marcas de azufre. Se centraron en un conjunto de cuatro genes centrales, brxP, brxC, brxZ y brxL, y mediante análisis de secuencia demostraron que BrxP y BrxC se asemejan a las proteínas que manejan azufre en los sistemas ssp. Experimentos en la bacteria intestinal humana Bacteroides salyersiae confirmaron la sospecha: cuando los investigadores eliminaron el gen brxC, el ADN modificado con azufre desapareció; cuando restauraron brxC en un plásmido, las marcas de azufre reaparecieron. También trasladaron genes clave de BREX a otra bacteria intestinal que normalmente carece de estos sistemas y demostraron que empezó a producir el mismo patrón de ADN con azufre, mostrando que la maquinaria BREX tipo 4 puede por sí sola crear marcas de fosforotioato.
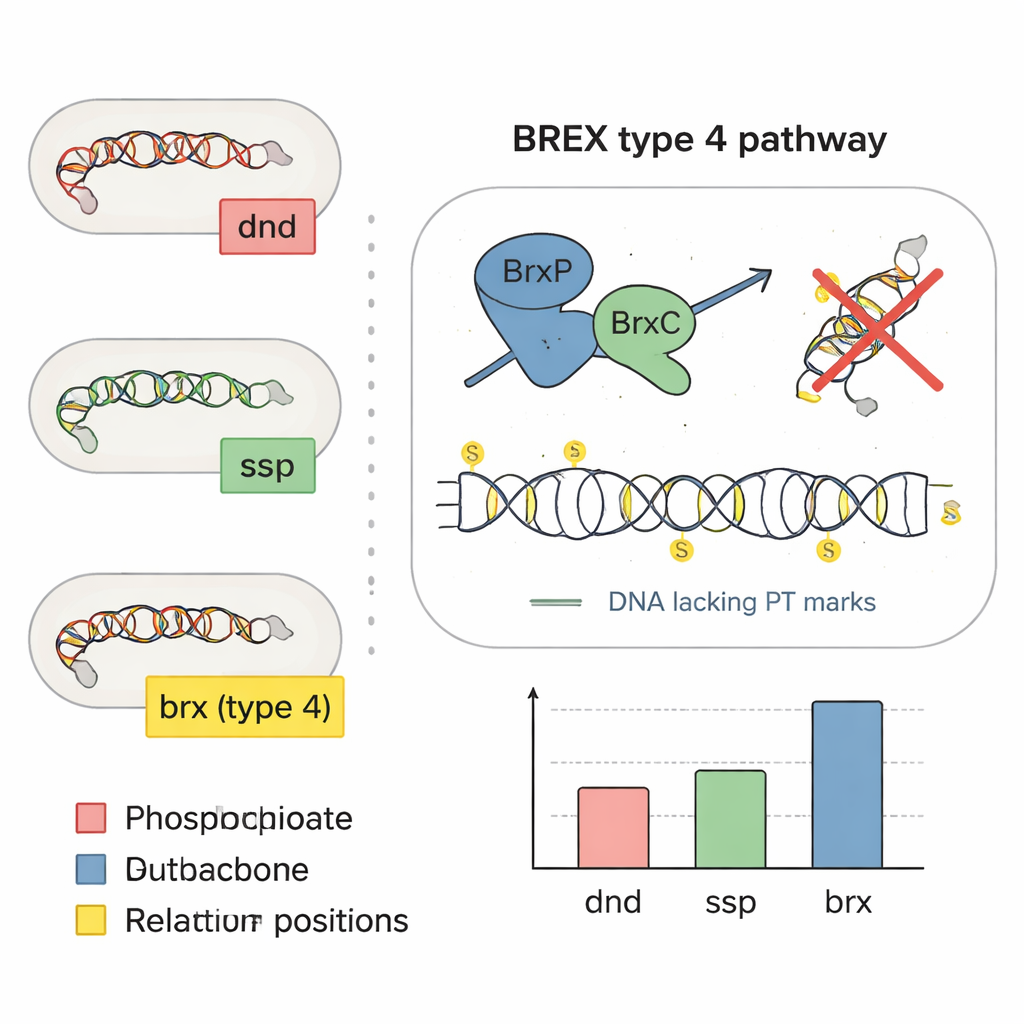
Cartografiar dónde cae el azufre en el genoma
Detectar las marcas de azufre es sólo la mitad de la historia; saber exactamente dónde aparecen a lo largo del ADN es crucial para entender su función. Los investigadores combinaron espectrometría de masas sensible con un método de secuenciación a medida llamado PT-seq, que corta selectivamente el ADN en sitios modificados con azufre y luego lee la secuencia circundante. Entre 226 aislamientos bacterianos intestinales, identificaron ocho dinucleótidos “bloqueadores” distintos que contienen azufre y, a partir de cepas representativas, determinaron motivos cortos completos donde tiende a ubicarse el azufre. Es intrigante que las bacterias con sistemas dnd, ssp o BREX produjeron conjuntos diferentes de patrones de azufre, como dialectos distintos del mismo lenguaje químico. Las marcas no estaban distribuidas al azar: se enriquecían en genes de ARN ribosómico y, en general, evitaban los comienzos y los finales de genes codificadores de proteínas, lo que sugiere que las bacterias podrían estar dirigiendo el azufre fuera de regiones de control sensibles.
Qué significa esto para nuestra salud
Para un público no especializado, estos hallazgos muestran que las bacterias intestinales no sólo viven de lo que comemos: reescriben activamente la química de su propio ADN de modos que influyen en cómo combaten virus y responden a las condiciones oxidantes que suelen acompañar a la inflamación. Al identificar BREX tipo 4 como un nuevo sistema que marca con azufre y al mostrar que alrededor de una de cada trece microbios intestinales porta alguna forma de maquinaria de fosforotioato, este trabajo sienta las bases para explorar cómo estas marcas inusuales del ADN influyen en la estabilidad del microbioma, la resistencia a infecciones y, posiblemente, el curso de enfermedades como la enfermedad inflamatoria intestinal. A largo plazo, comprender y quizá manipular estos sistemas epigenéticos basados en azufre podría ofrecer nuevas estrategias para ajustar el microbioma intestinal en favor de la salud humana.
Cita: Yuan, Y., DeMott, M.S., Byrne, S.R. et al. Phosphorothioate DNA modification by BREX type 4 systems in the human gut microbiome. Nat Commun 17, 1717 (2026). https://doi.org/10.1038/s41467-026-68412-5
Palabras clave: microbioma intestinal, epigenética bacteriana, fosforotioación del ADN, sistema de defensa BREX, bacteriófagos