Clear Sky Science · es
Visualización in situ de la heterogeneidad fenotípica y la morfología unicelular de Clostridioides difficile durante la infección intestinal
Por qué los microbios intestinales no se comportan todos igual
Clostridioides difficile, conocido a menudo como C. diff, es un patógeno hospitalario notorio que puede provocar diarrea grave y a veces potencialmente mortal tras la perturbación de la microbiota intestinal por antibióticos. Sin embargo, incluso cuando estas bacterias son genéticamente idénticas y comparten el mismo entorno, las células individuales pueden comportarse de forma muy distinta. Este estudio revela, con un detalle sin precedentes, cómo células individuales de C. difficile activan o desactivan la producción de toxinas e incluso cambian de forma mientras infectan el intestino del ratón, lo que ofrece pistas sobre por qué la enfermedad puede ser tan persistente y difícil de tratar.
Rastreando a un invasor intestinal peligroso en tiempo real
Para entender cómo actúan las células individuales de C. difficile dentro del organismo, los investigadores necesitaban una forma de verlas claramente en medio de la densa y diversa comunidad microbiana intestinal. Diseñaron cepas de C. difficile que brillan continuamente en colores vivos bajo el microscopio, usando proteínas fluorescentes especiales que no interfieren con la capacidad de las bacterias para crecer o causar la enfermedad. Al infectar ratones tratados con antibióticos con estas cepas fluorescentes y luego cortar y teñir el colon, pudieron localizar las posiciones exactas y los comportamientos de miles de células bacterianas individuales dentro de tejido intestinal intacto. 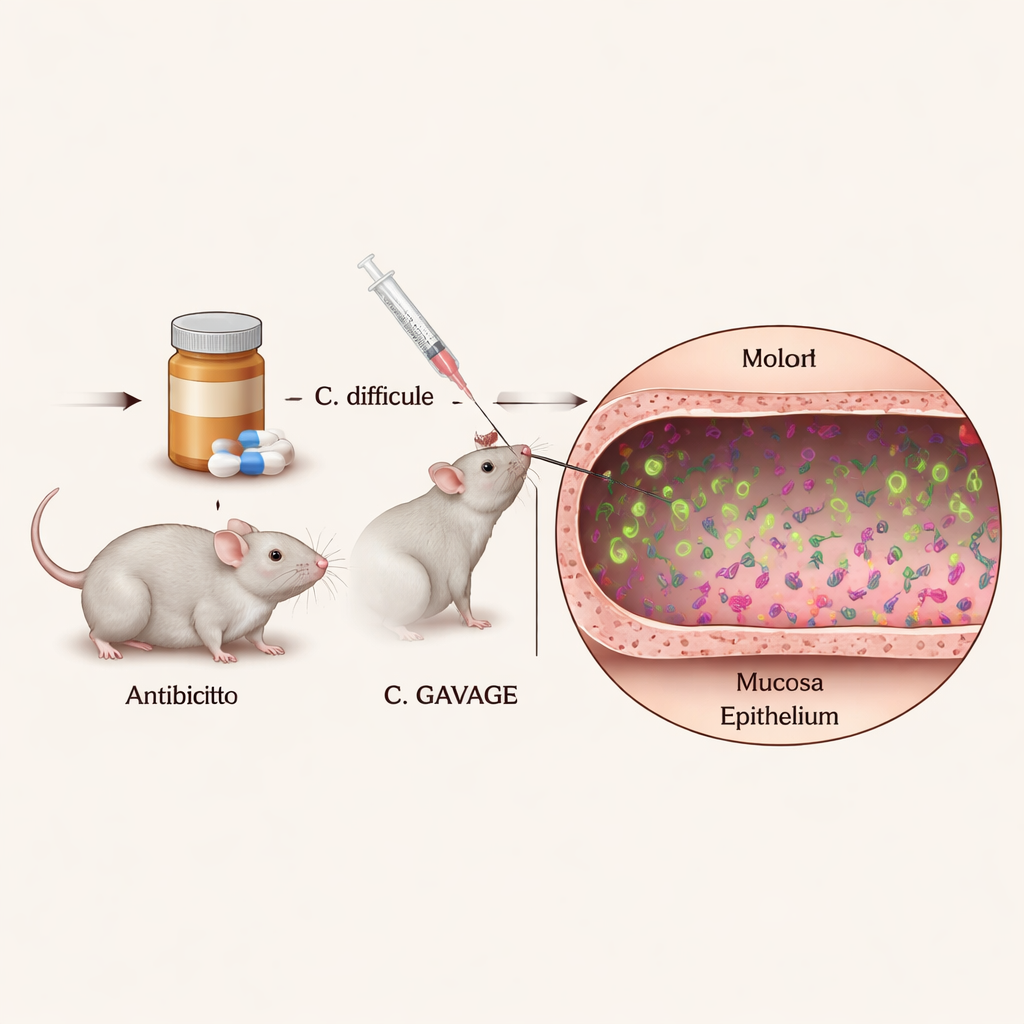
Dónde viven las bacterias en el colon
Las imágenes mostraron que la mayoría de las células de C. difficile se encuentran en el centro del contenido del colon, conocido como la luz (lumen), confirmando que el organismo es principalmente un patógeno “luminal” de libre flotación. Sin embargo, una minoría notable de células apareció consistentemente cerca de la capa de moco y directamente junto a la superficie epitelial—la delgada capa celular que recubre el colon y actúa como barrera frente al exterior. Esta subpoblación de contacto cercano no se había observado claramente antes en ratones convencionales con sistemas inmunitarios normales. Es importante destacar que las etiquetas fluorescentes diseñadas no debilitaron de forma apreciable a las bacterias en animales, lo que sugiere que las imágenes probablemente reflejan cómo se comporta C. difficile en una infección realista.
¿Quién produce toxina y dónde?
El equipo añadió entonces una segunda señal fluorescente que se activa solo cuando C. difficile pone en marcha sus genes de toxina. Las toxinas son las proteínas dañinas que lesionan el revestimiento intestinal y provocan los síntomas de la enfermedad, y son además lo que los médicos miden en pruebas de heces para diagnosticar la infección. Sorprendentemente, las bacterias no produjeron todas toxina a la vez. En cambio, solo una fracción de las células se iluminó como “toxina-ON” en un momento dado, tanto en fases tempranas como tardías de la infección. Esta fracción fue mayor en una cepa mutante diseñada genéticamente para sobreproducir toxina, pero incluso ahí no todas las células participaron. Igualmente llamativo, la posición de una célula—flotando en la luz, asentada en el moco o tocando el epitelio—no cambió de forma notable ni la frecuencia con que se producía toxina ni la intensidad con que se activaban esos genes. 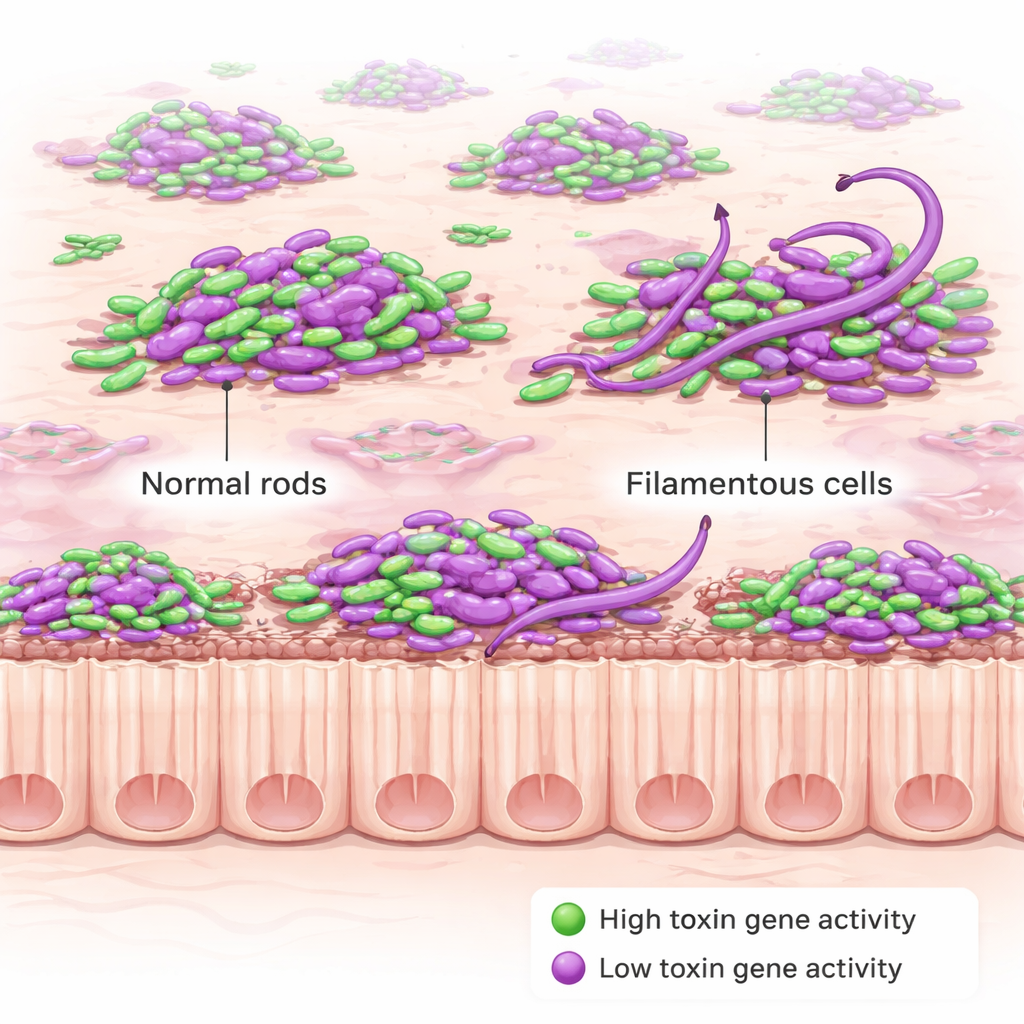
Células que cambian de forma bajo estrés
Mientras cartografiaban la producción de toxina, los investigadores encontraron un comportamiento nuevo y sorprendente. En ratones infectados con la cepa mutante que sobreproduce toxina, muchas células de C. difficile durante la fase aguda de la enfermedad se alargaron de forma inusual, convirtiéndose en filamentos curvados, algunos más de diez veces la longitud de los bacilos cortos normales. Esta morfología “en cuerda” apareció fundamentalmente durante la infección temprana y grave y disminuyó más tarde; no apareció cuando la misma cepa se hacía crecer en caldo de laboratorio. Eso sugiere que las condiciones estresantes del intestino inflamado—más que los cambios genéticos por sí solos—provocan esta remodelación tan marcada. Experimentos de seguimiento mostraron que la pérdida de una proteína reguladora llamada RstA, que controla tanto los genes de toxina como otras respuestas al estrés, contribuye a la formación de estos filamentos.
Qué significa esto para la enfermedad por C. diff
Para los no especialistas, el mensaje clave es que incluso una sola cepa de C. difficile actúa como una fuerza laboral dividida. Algunas células asumen el coste energético de producir toxina y dañar el intestino, liberando nutrientes que sus vecinas libres de toxina pueden explotar. Esta “división del trabajo” compartida puede ayudar a que la infección persista y rebrote, porque no todas las células son igualmente vulnerables a tratamientos que apuntan a la toxina o a bacterias en rápido crecimiento. El nuevo sistema de reporteros fluorescentes proporciona a los científicos una forma potente de observar, célula por célula, cómo C. difficile y microbios intestinales relacionados se adaptan a lo largo del tiempo y el espacio dentro del organismo. Esa visión podría, en última instancia, orientar terapias que no solo maten bacterias, sino que también deshabiliten los roles perjudiciales de subpoblaciones concretas que impulsan la enfermedad y su recurrencia.
Cita: DiBenedetto, N.V., Donnelly-Morell, M.L., Kumamoto, C.A. et al. In situ visualization of Clostridioides difficile phenotypic heterogeneity and single-cell morphology during gut infection. Nat Commun 17, 1716 (2026). https://doi.org/10.1038/s41467-026-68411-6
Palabras clave: Clostridioides difficile, microbioma intestinal, toxinas bacterianas, heterogeneidad fenotípica, imágenes fluorescentes