Clear Sky Science · es
Un nanosistema dirigido al inhibidor tisular de metaloproteinasas‑1 para una terapia continua espaciotemporal de la fibrosis pulmonar idiopática
Por qué importa la cicatrización pulmonar persistente
La fibrosis pulmonar idiopática (FPI) es una enfermedad pulmonar implacable en la que el tejido pulmonar normal, esponjoso, se reemplaza lentamente por tejido cicatricial rígido. Las personas con FPI se quedan sin aliento al realizar actividades cotidianas y la mayoría sobrevive solo unos años tras el diagnóstico. Los fármacos actuales pueden ralentizar la enfermedad en algunos pacientes, pero rara vez revierten las cicatrices existentes y con frecuencia provocan efectos secundarios. Este estudio explora una “nanoterapia” inteligente inhalada diseñada no solo para frenar la FPI, sino para eliminar activamente el tejido cicatricial y ayudar a que los pulmones se reparen.
El problema: cicatrices adherentes y estrés químico
En la FPI, los espacios donde el oxígeno normalmente pasa a la sangre se llenan de proteínas en exceso como el colágeno, convirtiendo los alvéolos flexibles en zonas rígidas. Los autores se centraron en una proteína llamada TIMP‑1, que actúa como un freno sobre las enzimas naturales que normalmente degradan el colágeno sobrante. Al examinar muestras de pulmones de pacientes y de ratones con cicatrización pulmonar inducida, encontraron que los niveles de TIMP‑1 eran varias veces mayores que en pulmones sanos y aumentaban en paralelo con la acumulación de colágeno. Al mismo tiempo, los pulmones dañados mostraron niveles elevados de especies reactivas de oxígeno (ROS), ‘chispas’ químicas que lesionan las células, y una pérdida de marcadores clave de las células que recubren los alvéolos. En conjunto, estos hallazgos apuntaron a un ciclo vicioso: demasiado TIMP‑1 frena la degradación de las cicatrices, mientras que el estrés oxidativo daña aún más la estructura pulmonar.
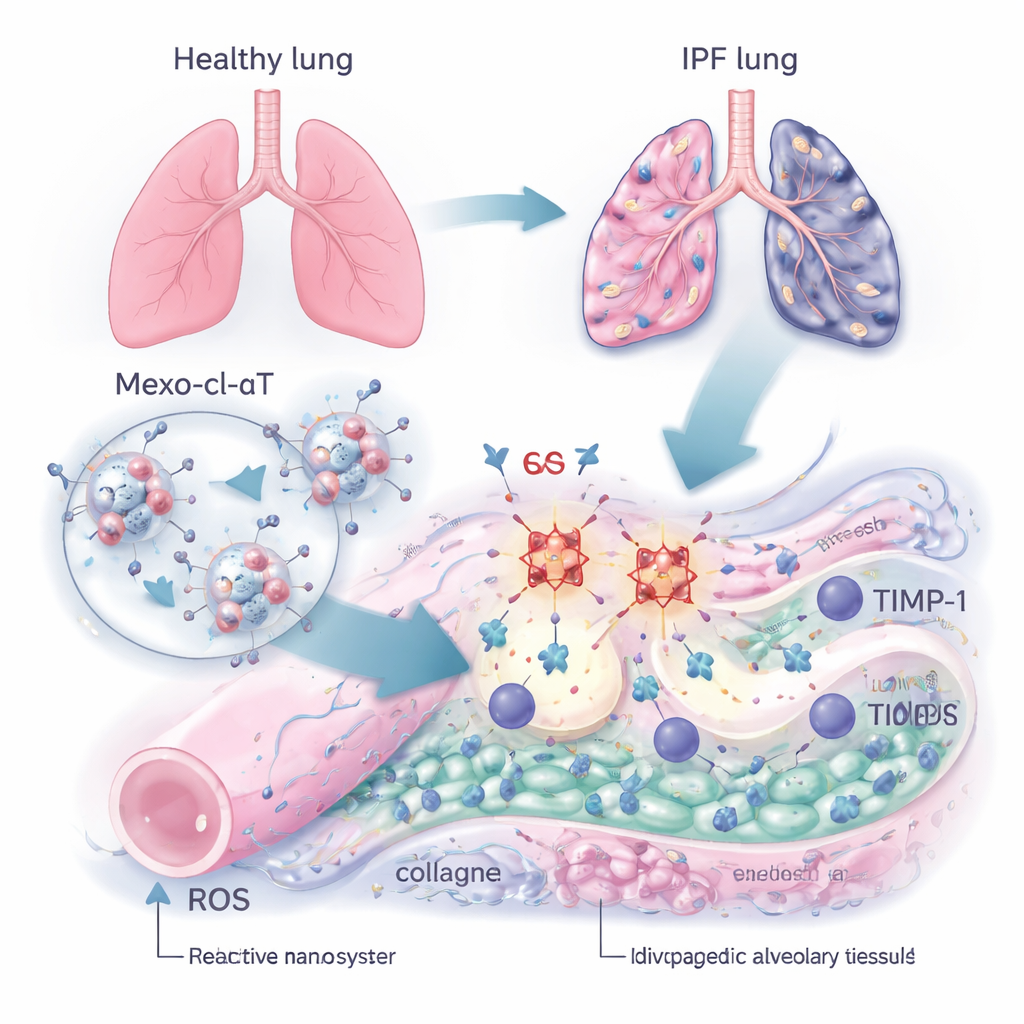
Un vehículo de entrega inteligente: pequeños paquetes de reparación
Para romper este ciclo, el equipo construyó una terapia a escala nanométrica llamada Mexo‑cl‑aT. Empezaron con exosomas: partículas naturales en forma de burbuja liberadas por células madre que ya se sabe que se dirigen a los tejidos lesionados y favorecen la reparación. En la superficie de estos exosomas acoplaron anticuerpos que se unen específicamente a TIMP‑1. La unión entre el exosoma y el anticuerpo se realizó mediante un enlazador químico especial que puede cortarse por ROS. En otras palabras, el agresivo entorno químico de un pulmón cicatrizado se usa como señal: cuando el exosoma llega a una región dañada rica en ROS, el enlazador se rompe, consumiendo parte de las ROS y liberando el anticuerpo justo donde TIMP‑1 está concentrado, mientras que el propio exosoma continúa promoviendo la reparación tisular.
Cómo se comporta y funciona el nanosistema
En estudios celulares, los investigadores mostraron que Mexo‑cl‑aT permanece estable en fluidos pero suelta rápidamente sus anticuerpos cuando se expone a niveles de peróxido de hidrógeno similares a los presentes en pulmones enfermos. Al mismo tiempo, reduce de forma pronunciada la cantidad de peróxido presente, confirmando su papel como eliminador de ROS. En modelos celulares que simulan la cicatrización, los anticuerpos liberados redujeron los niveles de TIMP‑1 y liberaron las enzimas que degradan el colágeno, mientras que el componente exosomal disminuyó la muerte celular, aumentó el crecimiento celular y aceleró el cierre de heridas tanto en células pulmonares como en células vasculares. En comparación con versiones cuyo enlazador no podía cortarse, el diseño sensible a ROS eliminó más colágeno y redujo el estrés químico de forma más eficaz, lo que subraya la importancia de la liberación controlada.
Pruebas en un modelo de fibrosis pulmonar avanzada
El equipo probó después la terapia en ratones con fibrosis pulmonar avanzada inducida por la droga bleomicina, un modelo elegido para imitar la FPI en estadios tardíos. Una sola dosis inhalada de Mexo‑cl‑aT permaneció en los pulmones durante días y retuvo más anticuerpo que una mezcla simple de sus componentes. Los pulmones tratados se veían más saludables a simple vista y al microscopio: los espacios aéreos se reabrieron, el grosor de las cicatrices disminuyó y el contenido total de colágeno casi volvió a la normalidad. Los marcadores de células activadas formadoras de cicatrices descendieron, mientras que las proteínas relacionadas con células sanas del revestimiento alveolar y vascular aumentaron. Las mediciones químicas mostraron que el tratamiento redujo drásticamente los niveles de TIMP‑1, restauró el equilibrio de las enzimas que eliminan colágeno y eliminó aproximadamente tres cuartas partes del exceso de ROS. Es importante señalar que las medidas de inflamación disminuyeron y los análisis de sangre y exámenes de órganos no revelaron toxicidad evidente.
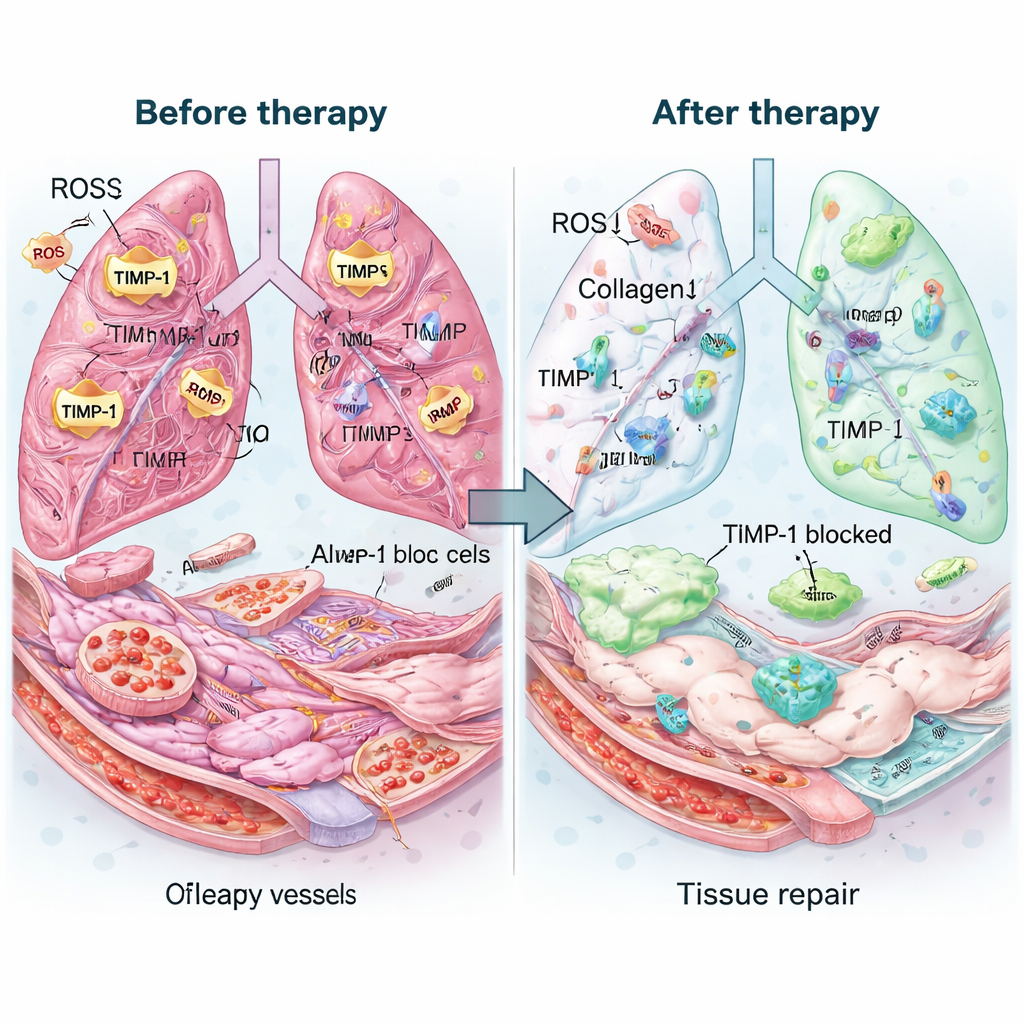
Qué podría significar esto para los pacientes
Para las personas que viven con FPI, este trabajo aún no ofrece una cura inmediata, pero presenta una estrategia prometedora. En lugar de limitarse a frenar el daño nuevo, el nanosistema Mexo‑cl‑aT pretende deshacer activamente las cicatrices existentes, calmar el estrés químico nocivo y apoyar la reconstrucción del tejido pulmonar frágil, todo en una forma inhalada y dirigida que concentra el tratamiento donde más se necesita. Aunque persisten desafíos como la producción de exosomas a gran escala y las pruebas en humanos, el estudio sugiere que las nano‑terapias de precisión ajustadas al entorno enfermo podrían algún día transformar el tratamiento de la cicatrización pulmonar persistente y, quizá, de otras enfermedades fibróticas.
Cita: Li, C., Lu, G., Chen, H. et al. A nanosystem targeting tissue inhibitor of metalloproteinase-1 for continuous spatiotemporal idiopathic pulmonary fibrosis therapy. Nat Commun 17, 1694 (2026). https://doi.org/10.1038/s41467-026-68398-0
Palabras clave: fibrosis pulmonar idiopática, cicatrización pulmonar, nanomedicina, terapia con exosomas, TIMP‑1