Clear Sky Science · es
Rejuvenecimiento mecánico de células madre senescentes y hueso envejecido mediante remodelado de la cromatina
Por qué importa mantener los huesos jóvenes
Al envejecer, nuestros huesos pierden gradualmente fuerza, volviéndose más delgados y frágiles. Esto aumenta el riesgo de fracturas, pérdida de independencia y dolor crónico. La mayoría de los tratamientos actuales se centran en fármacos que ralentizan la degradación ósea o añaden minerales, pero no reparan directamente el envejecimiento de las células madre que forman el hueso. Este estudio explora otro enfoque: usar fuerzas físicas cuidadosamente controladas —en lugar de medicamentos— para “rejuvenecer” las células madre formadoras de hueso envejecidas y mejorar la salud ósea y la capacidad física general en ratones mayores.
Cuando los constructores del hueso envejecen
En lo profundo de nuestros huesos viven las células madre mesenquimales de la médula ósea, los constructores maestros que pueden convertirse en células formadoras de hueso. Con la edad, estas células madre se dividen menos, forman menos hueso y muestran signos clásicos de envejecimiento celular, como daño en el ADN y señales inflamatorias. Los investigadores compararon células de donantes humanos jóvenes y mayores y hallaron que las células envejecidas no solo eran diferentes bioquímicamente: eran mecánicamente más débiles. Generaban menos fuerza interna de tracción, tenían andamiajes internos más flexibles y mostraban peor transmisión de señales mecánicas al núcleo celular. En el tejido óseo de ratones viejos se observó un declive similar: la red de hueso esponjoso estaba más adelgazada, las proteínas clave de señalización mecánica estaban reducidas y los marcadores de envejecimiento aumentados.
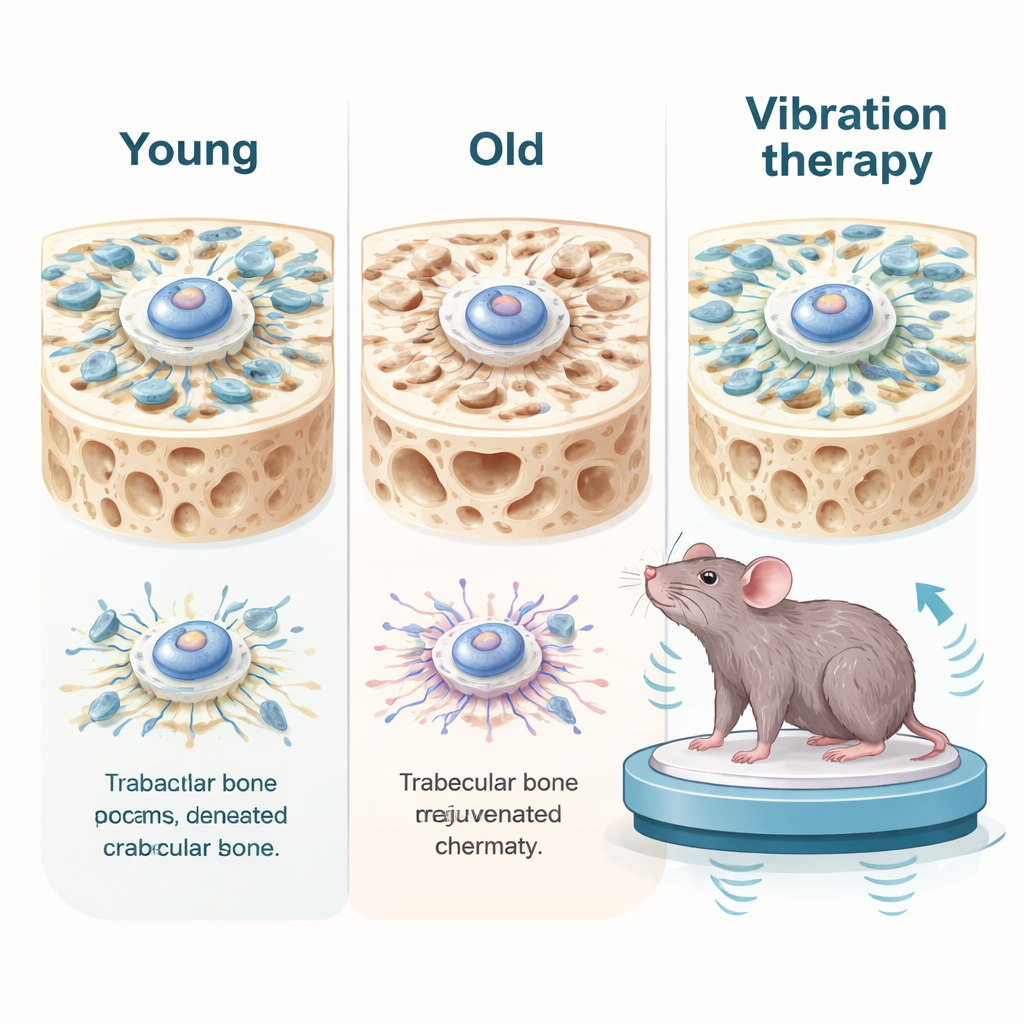
Tirar suavemente de las células para devolverles la juventud
El equipo preguntó entonces si restaurar la fuerza mecánica podría revertir estas características de envejecimiento. En cultivos, aplicaron estiramientos suaves a células madre senescentes o emplearon un fármaco que aumenta la actividad de los motores moleculares. Estos tratamientos reforzaron las fuerzas de tracción celular y mejoraron la organización del andamiaje interno. De forma notable, las células envejecidas empezaron a parecer y comportarse como más jóvenes: los marcadores de senescencia disminuyeron, el daño en el ADN se redujo y las células se multiplicaron con mayor facilidad. Lo contrario también fue cierto: cuando ablandaron el entorno bajo células jóvenes o debilitaron químicamente su maquinaria contráctil, las células entraron en un estado similar al envejecimiento, ralentizándose y activando marcadores de senescencia incluso en un gel 3D que mimetiza el hueso.
Cómo la fuerza comunica con los genes
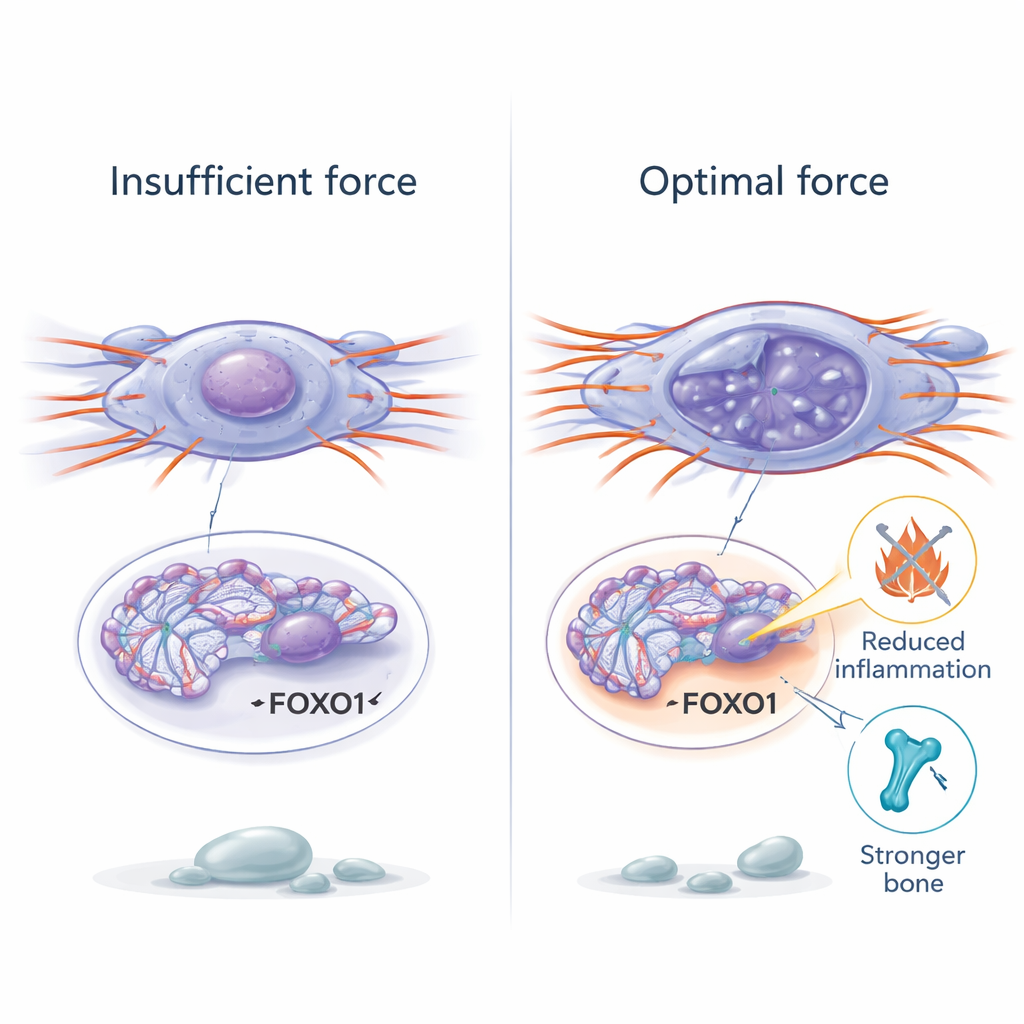
Para entender cómo las fuerzas físicas podían cambiar tan profundamente el comportamiento celular, los investigadores se centraron en la cromatina —la forma empaquetada del ADN dentro del núcleo. En las células madre viejas, la cromatina estaba más condensada y menos accesible, lo que dificultaba la activación de genes útiles. Restaurar la fuerza mecánica provocó que la cromatina se relajara localmente, aumentando marcas químicas asociadas con ADN abierto y activo. Mediante un ensayo genómico de accesibilidad de la cromatina, el equipo encontró que la estimulación mecánica suave abría regiones próximas a genes implicados en el control del envejecimiento. Un gen, llamado FOXO1, destacó por ser especialmente sensible a la fuerza. Cuando aumentaba la fuerza, la región de ADN de FOXO1 se volvía más accesible, su actividad aumentaba y las células se volvían menos senescentes. Bloquear FOXO1 eliminó los beneficios de la estimulación mecánica, revelándolo como un interruptor clave que vincula la tensión física con programas genéticos de resiliencia y reparación.
Encontrar el punto óptimo de la terapia mecánica
Los investigadores probaron luego la estimulación mecánica en ratones vivos. Animales mayores se colocaron sobre una plataforma de vibración de baja intensidad en sesiones diarias cortas durante un mes, mientras que otros tuvieron las patas traseras descargadas mediante suspensión por la cola, imitando una inactividad extrema. En los ratones envejecidos, la vibración suave potenció la señalización mecánica en el hueso, redujo marcadores de envejecimiento e inflamación y reconstruyó parcialmente la red de hueso esponjoso. También mejoró la fuerza de agarre, la resistencia al ejercicio, tareas relacionadas con la memoria y disminuyó la inflamación en sangre, hígado y riñones. Sin embargo, cuando la vibración se aplicó de forma continua sin días de descanso, los beneficios desaparecieron e incluso se invirtieron: la estructura ósea empeoró, el daño en el ADN aumentó y la inflamación se elevó. En estudios celulares, estiramientos excesivamente fuertes o frecuentes causaron roturas de ADN y devolvieron a las células a la senescencia, demostrando que la fuerza mecánica puede sanar o dañar dependiendo de la dosis.
De imitadores de ejercicio a tratamientos futuros
Para el público general, el mensaje central es que nuestras células no solo responden a hormonas y químicos: también “escuchan” atentamente las fuerzas físicas. En este trabajo, los autores muestran que una estimulación mecánica moderada y bien calibrada puede reactivar las células madre óseas envejecidas, abrir programas genéticos protectores como FOXO1, reconstruir hueso debilitado y calmar la inflamación crónica en ratones mayores. Al mismo tiempo, muy poca o demasiada fuerza acelera el desgaste celular. Estos hallazgos sugieren que terapias mecánicas diseñadas con cuidado —quizá regímenes específicos de ejercicio o dispositivos seguros basados en vibración— podrían algún día complementar los fármacos para mantener los huesos, y posiblemente otros tejidos, más sanos por más tiempo.
Cita: Liu, X., Ye, Y., Li, Z. et al. Mechanical rejuvenation of senescent stem cells and aged bone via chromatin remodeling. Nat Commun 17, 1684 (2026). https://doi.org/10.1038/s41467-026-68387-3
Palabras clave: envejecimiento óseo, estímulo mecánico, rejuvenecimiento de células madre, remodelado de la cromatina, FOXO1